
# 热门搜索 #
圣诺制药:深耕核酸导入技术,创制核酸干扰新药
{{detail.short_name}} {{detail.main_page}}
{{detail.description}} {{detail.round_name}} {{detail.state_name}}
 提供支持
提供支持在不久前的一个行业动态和进展介绍会上,圣诺制药集团公司创始人陆阳博士,向与会的同行们展示了RNA药物进展现状与前景。
仅就小核酸(寡核酸)药物而言,整个领域发展到今天,已经极大地超过了几年前的市场,预期达到30亿美元。 而随着更多的这类创新药物被相继批准进入临床使用,更多的跨国药企在这一领域的大量投入和更多的临床研究品种的推进,小核酸创新药物将在未来几年展现出蓬勃发展的趋势。特别是由于Medicines公司和Alnylam公司合作的以PCSK9为靶向的核酸干扰创新药Inclisiran的临床三期试验效果显著,获得临床应用批准的可能性极高,已表明核酸干扰药物极有可能在未来成为靶向药物的主力军之一。 而陆阳博士和他创立领导的圣诺制药(Sirnaomics)正是在核酸干扰新药创制领域辛勤耕耘,坚持不懈,在中美两地已经开展多项临床试验的创新企业。
陆阳是中山大学生物系77级本科生,1987年取得博士学位后赴美在马里兰大学和乔治城大学从事博士后研究。他在1993年进入美国生物制药工业界,成为世界首家基因治疗公司Genetic Therapy(后被诺华Novartis收购)的资深研究员和实验室负责人,步入了他从事基因治疗及核酸药物研发创制的职业生涯。“2000年,我与一位诺华的同事共同探讨了通过基因导入系统进行功能基因组鉴定的创业可行性, 而这个想法很快得到了诺华管理层的认可。”陆阳博士回忆道。在诺华基金(Novartis Venture)、当地政府创业基金和机构投资以及天使投资人的支持下,陆博士作为联合创始人共同创立了Intradigm(因确达生物)——一家专注核酸药物研发创制(RNA干扰)的生物技术公司。

圣诺制药陆阳博士
Intradigm是陆阳的首次创业和国际上最早进入核酸干扰新药创制的企业之一。作为公司的研发负责人,陆博士也是国际上最早进入到这个领域的研究者和创业者之一。在此后的几年里,核酸干扰技术被《科学》杂志评为十大科学成就之首(2002),核酸干扰药物领域的旗舰企业Alnylam成立(2002),Andrew Z. Fire和Craig C. Mello两位科学家因为发现核酸干扰技术获得诺贝尔生理学或医学奖(2006)。
陆阳博士领导的Intradigm研发团队在世界上首次应用核酸干扰药物治疗眼部新血管增生导致的疾病(AJP, Dec. 2004),并在动物模型中应用siRNA纳米导入技术成功地抑制肿瘤生长(NAR, Dec. 2004),并和中国的科学家们合作成功地在灵长类动物模型中应用核酸干扰技术抑制SARS病毒(Nature Medicine, Sept. 2005)。由于在核酸干扰技术领域的先行优势和突出成绩,Intradigm于2006年获得基因泰克基金等机构的收购,并在后来通过反向加盟在伦交所上市(2009)。
在离开Intradigm公司后不久(2007年),陆阳博士开始二次创业,在美国马里兰州创立了圣诺制药(Sirnaomics, Inc.)并担任CEO,继续深耕RNAi新药创制领域。次年,陆博士携海归团队回到国内,在苏州Biobay创立了苏州圣诺,作为圣诺制药在中国的研发中心和临床试验的协调基地。苏州圣诺一经创建,就获得了2008年苏州工业园区的创业领军人才专项,为圣诺在中国迅速发展奠定了坚实的基础。
在Fire教授与Mello教授通过线虫(C. elegans)模型研究中发现双链RNA可以实现对相应基因序列有效沉默(RNAi)的基础上,美国麻省理工学院(MIT)的Tuschl博士等发现了RNAi的诱发机制和小干扰核酸(siRNA)的结构特点。上述的共同发现为后来核酸干扰药物的研发创制提供了坚实的应用技术和作用机理的保证。而在如何推动核酸干扰技术成为新的药物治疗手段的过程中,导入技术成为这类药物是否成功的关键。圣诺从成立的那天起,就一直着力于导入技术的开拓。应用多肽纳米导入技术以及肿瘤靶向和肝细胞靶向的导入技术,圣诺目前已经建立了一个完善的核酸干扰新药创制平台,并有一系列全球新候选药物处于临床和临床前的不同阶段。
然而在圣诺制药创业的早期,由于核酸干扰新药创制领域的低谷状态和全球金融危机的影响,整个RNAi领域原有的合作跨国药企,如默沙东、罗氏和辉瑞等巨头纷纷退场,而刚成立数年的圣诺制药也面临巨大压力。“那个时候,公司面临如何穿过死亡之谷的挑战,资金链紧张,候选药物项目需要寻求合作伙伴。” 陆阳博士告诉动脉网。而恰当其时,广州香雪制药正在向创新药领域发展,向圣诺抛出橄榄枝。 圣诺制药与香雪制药达成合作协议(2010),由圣诺提供技术和专利,香雪提供资金,共同在中国开发核酸新药STP705(科特拉尼),用于增生性瘢痕治疗。基于和香雪的合作并借助国家大力推动“十二五重大专项”的契机,圣诺于2012年在广州生物岛成立了国内第二家分公司——广州纳泰生物,作为集团在国内的核酸药物制剂生产基地。
核酸干扰药物成药的关键在于是否能将沉默目标基因表达的siRNA药物成功地递送到靶向细胞内。2018年,全球首款RNAi新药Onpattro在美国获批上市,该药物使用的是纳米颗粒(LNP)导入技术。 而最近成为第二个获批上市的RNAi 药物Givlaari 使用了N-乙酰半乳糖胺(GalNAc)-siRNA耦合导入技术。虽然GalNAc技术目前被业内认可为一种安全有效的载体系统,但由于其应用仅限于肝细胞疾病,整个核酸干扰药物研发领域开始探索应用更为广泛siRNA导入系统。
圣诺制药使用独创的组氨酸-赖氨酸共聚多肽纳米颗粒导入技术(PNP)来保护和运送siRNA。PNP由分支的组氨酸赖氨酸聚合物(HKP)组成,通过将siRNA闭合包裹在多肽纳米颗粒内,保证siRNA不被肾脏过滤清除,然后在血液循环逐渐地被靶细胞所摄取。进入靶细胞后,组氨酸基团发生质子化并允许有效负载释放到细胞质中。,其后siRNA可以诱导靶向基因沉默。由于PNP由天然氨基酸组成,其降解物天然无毒;这就同时克服了药物的靶向性和稳定性障碍。圣诺的研究成果表明,PNP既可应用于局部给药,也可应用于全身给药。而在全身给药时,可以通过多肽纳米颗粒来强化渗透性和滞留(EPR)效应,提供siRNA对肿瘤微环境中关键靶点的沉默,来影响并抑制肿瘤生长。由于PNP可同时携带多个siRNA,因此递送多个siRNA让其在同一靶向细胞中产生协同的基因沉默效应,可以提高RNAi的药物疗效。在肿瘤和纤维化疾病的治疗应用中,这个多肽纳米导入系统具有明显优势。
自成立以来,圣诺制药已构建了丰富的核酸干扰创新药物产品线,治疗领域覆盖多项肿瘤和纤维化疾病。其中,与广州香雪制药共同开发的领先候选药物STP705利用双靶标核酸抑制剂和多肽聚合物类纳米导入制剂治愈增生性疤痕的临床试验申请于2016年11月和2017年4月先后获得了美国FDA和中国药监局的许可。其后,STP705治疗胆管癌(CCA)和非黑素瘤皮肤癌(NMSC)又在美国FDA获得了临床许可,其中NMSC已于今年3月在美国启动二期临床试验,预计在明年年初公布试验结果。STP705还获得了美国FDA授予的多项孤儿药资格认定,可借助政策法规的绿色通道,快速推进临床并在美获得新药批准。
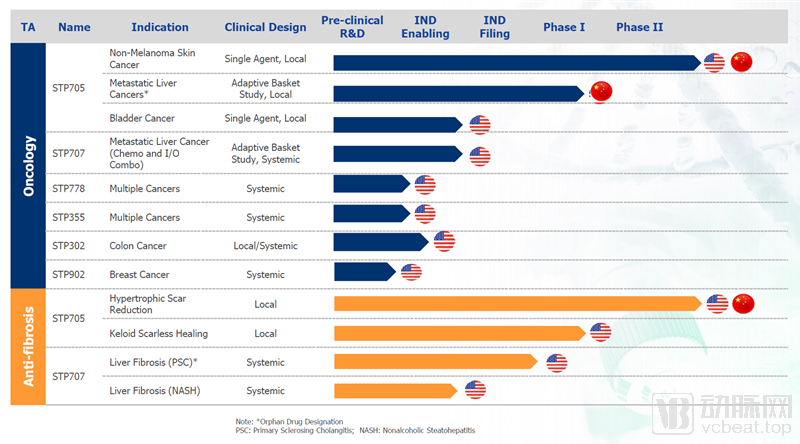
圣诺制药研发管线
今年4月,圣诺制药完成了共计4800万美元的C轮融资,由广州的越秀产业基金和香港的华润正大生命科学基金领投。作为全球领先的专注于核酸干扰(RNAi)药物研发和产业化开发的生物医药企业,以及全球唯一能够在中美同时推动RNAi临床研究的研发平台,圣诺现正在积极推进上市前的新一轮融资的进程,计划在不远的将来登陆国际资本市场。 “作为一个专注核酸干扰新药创制在国际上和亚洲的头部企业,圣诺制药将大力推进基于多肽纳米导入技术和GalNAc等其他导入技术的核酸干扰药物的研发创制,在肿瘤免疫治疗和纤维化疾病治疗等领域走在世界前列,为亟待解决的临床病患急需提供更为有效安全的治疗手段”,陆阳博士如是说。
如果您想对接动脉网所报道的企业,请填写表单,我们的工作人员将尽快为您服务。