人类社会每一次大的技术进步往往是来自于对微观世界有了更深入的理解和掌控。
以微米或纳米度量的微球,是生物制药、体外诊断等领域不可或缺的核心基础材料,有着极大的制备和应用难度,曾被《科技日报》列为35项“卡脖子”关键核心技术领域之一,也在生物和药物领域获得越来越多的关注。
传统的微球制备以釜式反应为主,将原料和试剂投入反应釜中,通过控制转速、温度和反应时间,以获得目标微球产物,整个过程是在一个宏观的反应环境下进行的。这种制备方式相对简单,经过多年发展已进入成熟的商业化应用阶段。但微球制备是微观层面的反应,将成球过程放大来看,往往伴随着复杂的物理剪切和化学合成,宏观的釜式反应无法精确调控这样的微观过程。
近年来,伴随着行业的发展,微球进入了越来越多的细分领域和赛道,需求端对微球性能和制备工艺提出了更高的要求,釜式反应这一微球制备技术1.0愈来愈难以满足产业需求,也就催生出了新的制备技术。
以中科森辉马光辉院士团队为代表的膜乳化技术受到的关注最多,通过压力将原料从膜孔挤出形成微球,一定程度上改善了微球的粒径分布,但膜本身性能和产能的问题限制了其产业化脚步。全球范围内如日本SPG、英国Micropore等上述公司牢牢掌握着上游膜材供应。这一技术又被称为微球制备技术2.0。
与此同时,一种新的微球制备技术在学术界广泛流行,其在复杂结构、高均一微球制备和操控方面可谓独步江湖。这种技术有一个响亮的名字——微流控,我们称之为微球制备技术3.0。
微流控的早期概念可以追溯到19世纪70年代采用光刻技术在硅片上制作的气相色谱仪,而后又发展为微流控毛细管电泳仪和微反应器等。微流控的重要特征之一是微尺度环境下具有独特的流体性质,如层流和液滴等。借助这些独特的流体现象,微流控可以实现一系列常规方法所难以完成的微加工和微操作,因此受到无数科学家的青睐。
尽管微流控作为一种技术在微球制备方面具备显著优势,但在产业界却很少被关注到。其中最大的问题在于微流控制备微球的产能问题。单个通道的微流控芯片每小时的微球生成量不超500μl,这一通量能够满足科研需求,但却无法满足动辄几千上万升的工业化场景。解决这一难题,需要从通量上下功夫。而这就是阿卡索生物一直在做的事情。
全球首款千级通道微流控芯片,突破高集成度瓶颈,打造微流控平台型生产工具
阿卡索生物成立于2021年5年,公司创始团队是三个年轻人,有着相同的标签,【清华大学】【八字班】。
在创立阿卡索之前,通过一次偶然的机会,团队接触到微球产品,看到了单分散微球的商业价值。凭借出色的专业判断,他们敏锐地意识到,如果能有一种平台化的制备技术,能同时解决微球制备过程中微观控制和宏观量产这一矛盾,无疑将具备巨大的商业价值。
很快他们就将目光投向了微流控技术,并找到了有着多年微流控放大研究经验的华东理工大学张莉教授合作,开始共同开发超高通量微流控芯片。彼时,张莉教授已成功研发出八十通道数的高通量微流控芯片,如何向更高通量、更高集成度芯片进发,诸多的工程和技术问题摆在团队的面前。
首先,如何在一块芯片上实现海量微球发生器的高度集成,需要建立一套数学模型,以便通道内的流阻分布能满足海量微球发生器的流量/流速保持一致。
其次,需要构建特殊的管路和微球发生器,包括流道分布、管路尺寸和结构、微球发生器结构及涂层方案。
此外,相较于微流控检测芯片,作为微球制备平台,对芯片材质的选择和加工提出了更高的要求。一般的PDMS材质因无法耐受高温和有机溶剂只能被淘汰,团队选择了更高强度的玻璃材质。而这无疑又带来了芯片刻蚀和键合上的巨大挑战。
这里面涉及到物理、材料、化学、结构等多个学科的专业知识,是一项复杂的跨学科工程实践。最终,经过不懈努力,阿卡索生物克服重重难关,终于成功实现了国内首个工业级高性能微流控生产平台,掌握了从芯片设计到加工制造的全套工程能力,于今年8月成功推出全球首款千级通道微流控芯片,并基于此顺利实现高均一微球的量产制备,真正意义上实现一套方案同时兼顾“单分散”和“工业级产能”。

公司总经理蒋涛提到:“阿卡索生物超高通量微流控芯片技术的实现具有重大的历史意义,真正解决了微流控产业化应用的技术瓶颈,构建了微流控从学术界到产业界的桥梁。并且这一技术属于平台型技术,能够适配多种微球体系,解锁多种微球应用场景。”
谈到公司愿景,蒋涛提到,“希望公司能凭借在超高通量微流控技术的突破和积累,构建一种生命科学新工具,给整个行业带来一些影响和变革。”
聚焦高均一、单分散,发力三大高潜力细分市场
基于高性能微球的规模化制备能力,阿卡索生物已在纯化填料、药物缓释、医美微球等多个细分品类,形成基于流动化学的连续相生产能力,实现产能的规模化提升。
色谱填料
在生物医药领域,分离纯化作为核心生产环节,直接决定了药品的纯度和质量,也是主要生产成本所在。单克隆抗体生产中,下游分离纯化环节成本即占据整个生产成本的65%以上。
色谱/层析技术几乎是生物制药分离纯化的唯一手段,高纯度、高活性的生物制品制造基本都依赖于色谱/层析分离技术。基于此,色谱填料是决定药物分离纯化效率和产品质量的关键因素。
目前,我国用于生物大分子药物或有机小分子药物分离纯化的色谱填料/层析介质微球等核心材料基本依赖进口,可替代进口产品的高性能国产化微球材料具有巨大市场潜力。据市场数据推算,2020 年中国色谱填料市场规模为 7~10 亿美元,即 50~70 亿人民币,未来还将持续增长。
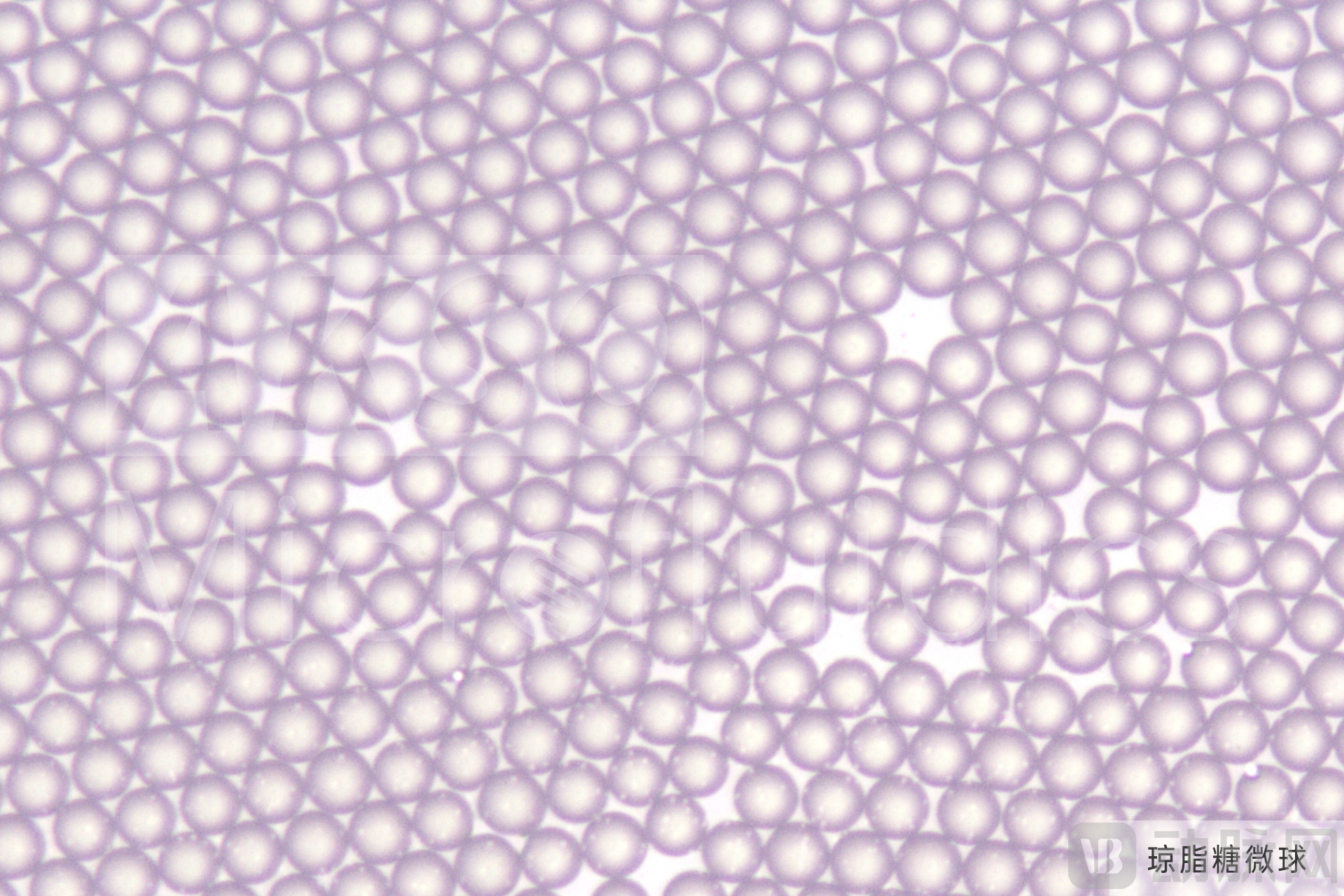
在色谱填料领域,阿卡索生物致力于提供单分散填料解决方案。“公司将主打琼脂糖软胶填料,通过高均一、单分散这一特点建立差异化竞争优势。同时结合微流控平台技术优势,同步布局软硬胶管线,集中少量SKU,形成品牌效应。“蒋涛说。
药物缓释
微球缓释制剂是目前适用范围最宽,作用周期最长的长效注射剂。微球将药物包埋或吸附在聚合物分子的表面,通过皮下或肌肉注射进入体内后,通过载体表面快速释放、药物扩散、聚合物溶蚀降解等方式实现药物缓慢释放,大大延长药物的半衰期。
据头豹研究院数据,2019-2021年中国微球缓释制剂行业市场规模由47亿元增长到65亿元。未来,伴随着多个原研药专利过期,本土企业将加紧布局微球缓释制剂领域,中国微球缓释制剂市场规模将呈现快速增长趋势。预计2024年中国微球缓释制剂行业市场规模将增长至116亿元。
阿卡索生物的微球缓释制剂最大的优势首先是粒径均一,通过调节连续相和分散相流速,精确控制微球粒径,CV值可做到<5%,单分散性好。其次是高包封率、药物损耗低,独立成球,包封率>98%。

制备均一、高包封率、缓释均匀的微球缓释制剂是各大研发药企的核心诉求,阿卡索生物希望与主流微球缓释制剂研发药企合作研发,提供CDMO服务,助力更多微球缓释制剂上市。
医美微球
在医美领域,童颜针的核心成分为聚左旋乳酸(PLLA)微球,注射进入人体之后可与人体相融,可以分解吸收,并且通过分解出来的乳酸刺激人体胶原纤维合成,增加组织容量、改善皮肤纹理、达到抗衰、紧致的作用。
相较于玻尿酸,童颜针的填充是依靠身体自身细胞,因此效果更加自然持久。效果最佳的PLLA 微球粒径应控制在 20~50µm 之间,并保证大小和均一的稳定性。
据兴业证券数据,2021年下半年童颜针才开始合规销售,预计未来2年翻倍增长,2025年将达到约20亿元的市场规模,2040年超百亿,CAGR近30%。
当前,制备均一、高安全性的PLLA 微球存在技术壁垒,阿卡索生物有机会通过原料供应或其他合作形式,与具备下游能力的厂家达成合作。

阿卡索生物希望通过自主研发的超高通量微流控芯片技术,去解锁更多的应用场景,实现真正意义上的工业化生产应用。希望可以加强外部合作,利用创新的高性能微球制备工艺,在药物微球、医美微球领域,与CDMO公司和对高性能微球有兴趣的伙伴一起,往产品方向做进一步延伸。
立足于未来,阿卡索生物将对超高通量微流控芯片进行进一步拓展,一是在尺度维度上的拓展,实现微观介观全尺度覆盖。二是芯片深度的拓展,致力于更高的集成度,以解锁更多的工业化场景。三是研发更多的生物、化学制备、发酵与合成体系,解锁更多应用场景。
“目前在国内,微流控用于检测是非常多的,但是还没有出现将其用于智能制造的头部企业。未来,我们希望能够成为国内乃至国际上将微流控用于智能制造的领军企业。”蒋涛说。





























