大学时,我无法预见当时所发之事的联系。如今回首,我才发现一切都很明了。无人能够预知未来,只有回头看时我们才能发现它们的因果。你们得相信,直觉,命运,因果,这些点滴会连接起未来的道路,会给你信心去跟随自己的意愿。哪怕当时不被看好,我们也不应止步,只有这样,才能有所成就。
——摘自2005年乔布斯于斯坦福大学毕业典礼中的演讲
“现在往回看,我过去所走的每一步似乎都有关联,但当时的我肯定无法预知多年后的发展。那时候我只是觉得自己能够通过参数测量和算法开发,将DNA分子之间的反应热力学、动力学都准确地预测出来。但是它们具体能解决什么问题,我那时并不知道。我只觉得如果先解决了这些科研难题,顺着脉络,一定能够找到它们的应用领域。”呈源生物(RootPath)联合创始人兼CEO陈曦博士告诉动脉网。
带着将科研成果应用于产业的信念,陈曦博士一路从Ultivue(一家源于哈佛大学尹鹏实验室科研成果的生物技术公司),到巢生资本,再到呈源生物,“其实这些经历都是一次创业旅程中的不同时期,在这个过程中,我首先要在不同场景下批判地认识自己的特殊才能,再找到可以施展这一才能的‘战场’,然后在这个专属战场中‘招兵买马’,打赢战争,实现自我价值的最大化。”
如今,陈曦博士带领着呈源生物已经把这场战争打到了比较有意思的阶段,而这些成果或将改写基因合成与细胞治疗行业的未来,让我们一起来看。
创始人具备IT+BT+风投背景,
公司在杭州+广州+波士顿均有布局
大学时期,陈曦博士就基于自身的交叉背景,参与了贺林院士实验室的课题组,并用1年时间以第一作者的身份在《德国应用化学》杂志发表了DNA计算机领域的论文。
毕业后,陈曦博士前往得克萨斯大学奥斯汀分校,师从著名合成生物学家、Aptamer发明人Andrew D. Ellington,继续生物化学领域的深造,“当时发了很多论文。一开始我也很开心,但是随着发表的论文逐渐增多,我觉得它们更像是束之高阁的‘阳春白雪’。这些成果既没有加深人们对科学的理解,也没有解决实际的应用问题。”
带着将“阳春白雪”应用于产业的想法,陈曦博士毕业后前往了波士顿,进入了哈佛大学Wyss研究所,师从著名分子工程、生物学与信息科学专家尹鹏,开启了博士后研究工作。完成博士后研究工作之后,陈曦博士作为创始成员先后进入了Ultivue、巢生资本,在生物技术风险投资和研发、管理等方便都积累了丰富的经验,为创办呈源生物打下了基础。
也正得益于在巢生资本的工作经历,与大多数科学家基于成果去做转化不同,呈源生物的成立契机是相反的。在从事风投行业期间,陈曦博士会先关注医药行业中存在的痛点和需求,并发现了在如今发展迅猛的免疫细胞治疗领域中,人们迫切需求低成本、高通量的基因合成,“基因合成的基础技术和我本身擅长的DNA分子热力学、动力学、生物物理学等领域刚好吻合,所以呈源生物也就顺理成章的成立了。”
发布呈源定制基因库,
成功将基因合成价格降低七成
不仅呈源生物的联合创始人陈曦博士出自巢生资本,公司本身也由巢生资本在2017年孵化成立。成立初期,呈源生物获得了巢生资本带来的各方资源和资金的助力。但在接下来的几年,公司仍能得到各方资本的青睐,凭借的则是自身的实力和具有前景的市场。
在2018年到2021年间,呈源生物先后完成了三轮市场化融资,累计金额约6000万美元,获得了红杉资本、火山石投资、百度风投、经纬创投、元禾原点、鼎晖投资、云九资本、弘毅投资等数家知名产业投资机构的加持。
在资金和团队的双重助力下,呈源生物在短短几年内完成了PathFinderTM核心技术平台的搭建,并于2023年10月9日成功向市场推出了呈源定制基因库(以下简称定制基因库),将目前基因从头合成的价格从人民币0.6 - 1元/bp,降至每bp价格范围为0.2元至0.38元,价格最多可降低七成,这也是目前已知全球范围内的最低价格。
在讲述这一基因合成领域的重磅创新产品之前,我们需要先厘清本文所述的基因合成的概念和范围。
基因合成是一个很广泛的概念,从单个引物的合成、到寡聚核苷酸池(oligo pools)合成,再到几kb甚至几十、几百kb的基因、基因簇的合成,都属于这个广义的范围。但目前行业内目光最为聚焦的领域,通常是指0.5-3kb这个范围的基因合成。这也是本文所指的基因合成,其成本主要来源于三个环节:
①“从无到有”环节:客户会给到企业一封包含本次合成基因序列的电子邮件,企业首先需要根据这份完全数字化的信息,从无到有地在固相载体上去合成目标短片段。这个过程中,人们需要一个碱基、一个碱基地搭载,“这里每一步都可能出现错误。所以从无到有的合成方法,最后只能搭100—200个碱基,远远达不到0.5-3kb(500-3,000bp)这个基因长度。”
②“组装纠错”环节:在这一环节中,企业会将上一步得到的短片段组装成0.5 – 3 kb的长片段。因为从无到有这个环节的错误率可能高达1%,所以在拼接过程中,还需要进行适当的纠错,将错误率从1%这个数量级降低至1‰以下。
③“扩增筛选”环节:在组装完成后,企业需要将这些合成的基因克隆进大肠杆菌进行扩增,再筛选出具有完全正确基因序列的菌落,最后将从这些菌落中扩增出的目的基因交付给客户。
“在基因合成流程中,人们大多把目光集中在了第一个环节。实际上,这三个环节的成本比例大体相当,如果只专注于第一点,就算将它的成本降到0,也还有2/3的价格没有降下来。在基于微阵列的寡聚核苷酸池(oligo pools)出现之后,第一个环节的技术发展已经足够成熟,商业化价格也足够便宜了。我们应该将目光放在后面两步。”陈曦博士告诉动脉网。
在后面两个环节中,使用 “看得见的手”( 包括机器手)去对这些DNA片段进行操作需要大量的酶、耗材,将产生巨大的成本。所以呈源生物选择了利用“看不见的手”——即DNA序列本身。呈源生物的核心技术是在充满上千条不同序列的溶液中,让DNA分子根据自己的序列自组装成长基因。其难点在于如何让同一试管中的几百个正确反都应都高效进行,并且避免所有的错误反应。
解决问题的关键在于DNA序列的设计,如密码子使用、断点选择等。这个过程需要一个非常定量、准确的仿真算法对DNA杂交、连接反应进行计算机模拟。 “基于仿真算法的设计在其他的工业学科中都是标配,但在生物学里却极少使用,其核心在于人们一直怀疑计算机能否对生物学过程准确模拟。”陈曦博士分析。
陈曦博士在学术界花了10年力图改变人们对生物计算的看法。通过数年研究,他成功证明了DNA折叠、杂交、酶促连接等过程完全可以在仿真算法中得到到足够精细、准确的预测。在这样的仿真算法的赋能下,呈源生物证明了他们可以达到高通量和低成本的基因合成效果。简而言之,呈源生物利用自主研发的探路者DNA组装(PathFinder DNA Assembly)技术,实现了在同一反应器中完成上千条基因的平行组装并有效纠错,大大降低了组装成本。
在错综复杂的基因合成、基因库合成市场中,呈源生物的定制基因库有三个亮眼之处:
①与市面上一些预先确定好序列的模式动物或人类cDNA文库不同,呈源生物可以根据客户的需求去定制基因,并保证价格的实惠。
②与基于随机序列的基因库不同,呈源生物会准确地根据客户提供的序列合成目标基因。这些序列可能来自于公开数据库,也可能来自于单细胞免疫细胞测序或者AI设计。
③由于传统基因合的高成本,客户往往将其作为补充工具,在不得不从头合成的情况下偶尔合成小量基因。而呈源基因库的低成本使得客户可以将其作为主力工具,开展需要合成成百上千个定制基因的研究。
以目前市面上其他基因从头合成的价格人民币0.6 - 1元/bp为例,这意味着,合成含有1000个平均长度为1.5kb基因的基因库将花费人民币90万至150万元,远超大多数研发项目的经费。使用定制基因库,在不同的交付周期、合成通量下,每bp价格范围为0.2元至0.38元,合成同样的基因库的价格可压缩至30万元,能大幅降低客户研发成本。
虽然呈源生物的技术大胆而新颖,但其最终交付形式与传统的基因合成相同,即经大肠杆菌菌落挑选后的、序列验证过的质粒,确保了产品的质量。此外,呈源生物还可提供多种质粒载体选择,包括pUC19、pET和pcDNA等标准载体,同时也支持客户提供的载体。其插入基因的长度范围为450 bp到2.5 kb,可以满足绝大部分科研项目的需求。此外,如果基因库中的基因为抗体基因,呈源生物还能够以极具竞争力的价格提供抗体蛋白表达、纯化和表征服务。
更广阔的未来:
其细胞疗法已将患者肿瘤直径缩小46.5%
呈源生物专注基因合成技术的契机来自于当前细胞疗法在实体瘤中的困境。CAR-T只能识别细胞表面的抗原,而TCR-T虽然可以识别细胞内的抗原,但HLA配型困难,且肿瘤容易通过丢失HLA等位基因逃逸。而且两者都有安全性隐患。
相比之下,完全自体来源且具有多克隆特性的TIL疗法有着先天优势。其领先产品(美国Iovance的lifileucel)已经接近FDA批准。然而,传统TIL产品的制备过程是一个“盲操作”。人们无法控制哪些T细胞克隆能在制备过程中能被扩增,也无法扭转T细胞的耗竭状态。
呈源生物的创始团队意识到,如果能将TIL中的肿瘤识别性TCR预测甚至实验鉴定出来,并将其转入外周血T细胞中,就可以将充满不确定性的“盲操作”变成一个完全可控的过程,并且可以保证良好的T细胞状态。但这一流程对TCR基因合成成本要求极高,当时没有现成的技术可以解决这一问题。呈源生物便接受了这一挑战,要从根源上解决基因合成的成本问题。
目前,呈源生物已经完成了合成型TIL的技术开发和可行性验证,并且建立了数条针对实体瘤的合成型TIL治疗管线。其核心管线已在IIT中完成了多例实体瘤患者的治疗。安全性、药代动力学等数据都展示了合成型TIL的优势,研究人员还在多个病人中观察到了肿瘤缩小。有一例病人的CT结果显示其肿瘤直径之和缩小了46.5%,并且达到确认部分缓解(confirmed partial response, cPR)的标准。下一步,呈源生物将积极申报IND,在注册临床中证明该疗法的安全性、有效性。
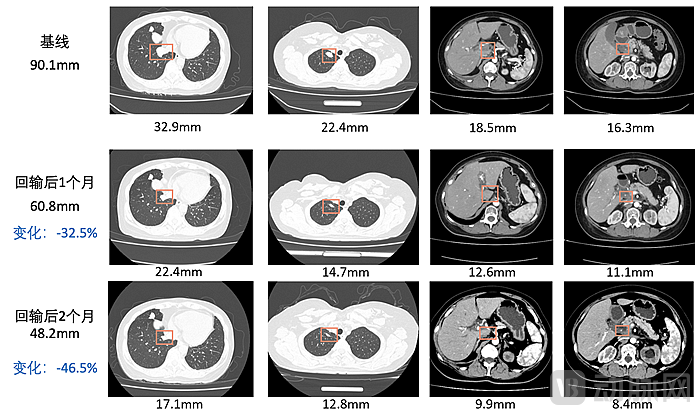
回输后患者肿瘤直径缩小46.5%,图源呈源生物
提及未来发展,陈曦博士表示,“下一步,呈源生物将平行布局定制基因库产品以及细胞疗法。在细胞疗法方面,我们还会采取多种商业化路径,通过自主研发、合作开发、产品授权等各种方式,以最快的速度,为患者带来安全、有效的产品。”期待呈源生物在高通量、低成本的基因合成领域中,持续作出突破,为行业带来更可及的疗法。





























