近两年,国产医用内窥镜行业高速发展。
据《2023年医用内窥镜行业研究报告》数据显示,2021年—2022年间,内镜行业不仅出现“吸金巅峰”,融资总额达以往4年间总和的近2倍,而且国家亦持续围绕技术创新、注册拿证、国产替代和临床应用规范给出相关细化文件。
资本与政策的双重助力下,我国传统可重复使用内窥镜正迅速缩小与国际水平的距离,从模仿走向创新。而在复合内窥镜领域,国产厂商更是展现出强大竞争力。共聚焦显微内镜、荧光内窥镜等技术领域已跑出国产黑马,且技术能力在国际上处于领先水平。如今,国产医用内窥镜的市场份额占比已由2020年的10%增加至2022年的26%,平均年度增长率超60%。
中国国际医疗器械博览会CMEF(秋季)作为国内最大的医疗器械展,每年都会展出全国乃至世界的先进医疗器械设备。透过展会情况,已能够明显感知到以上趋势。
今年已有越来越多的医用内窥镜企业开始带着自己的解决方案亮相会场,并逐渐开始在医疗市场中独当一面。此次展会上医用光学领域参展企业已有60余家,其中国产厂商占据了大部分展区,且产品在品类、质量和创新性上都足以满足临床需求。
从行业发展角度来看,国内医用内窥镜市场无疑已步入国产品牌崛起的下半场,而国产医用内窥镜的崛起亦成必然。例如在共聚焦显微内镜领域,中国便跑出了首家(共聚焦)显微内镜企业,实现了高端医疗装备领域的自主创新和技术突破,中国“智”造开始逆风翻盘、异军突起,在全球高端医疗装备产业,迎来一道来自中国医疗企业的靓丽风景。
国产医用内窥镜多点开花,共聚焦显微内镜重磅新品CMEF首发亮相
尽管在可重复使用内窥镜领域,我国发展起步晚于海外近百年,但随着20世纪80年代,沈大医用内窥镜等第一批医用内窥镜企业的成立,国产医用内窥镜质量已快速追赶,并拉开国产替代的序幕。
根据众成医械研究院数据,目前国产可重复使用内窥镜已有近750 款获得 NMPA 医疗器械注册证,已连续两年保持超 24%的年度增长率。此外,2020 年至 2022 年三年间,国产医用内窥镜在全国医疗机构的销售总金额与占比逐年增加,平均年增长率高于全国的销售额增长率达65%。可见,无论在产品品类、质量与创新性,还是商业化落地上国产可重复使用内窥镜均得到了长足发展,市场前景广阔。
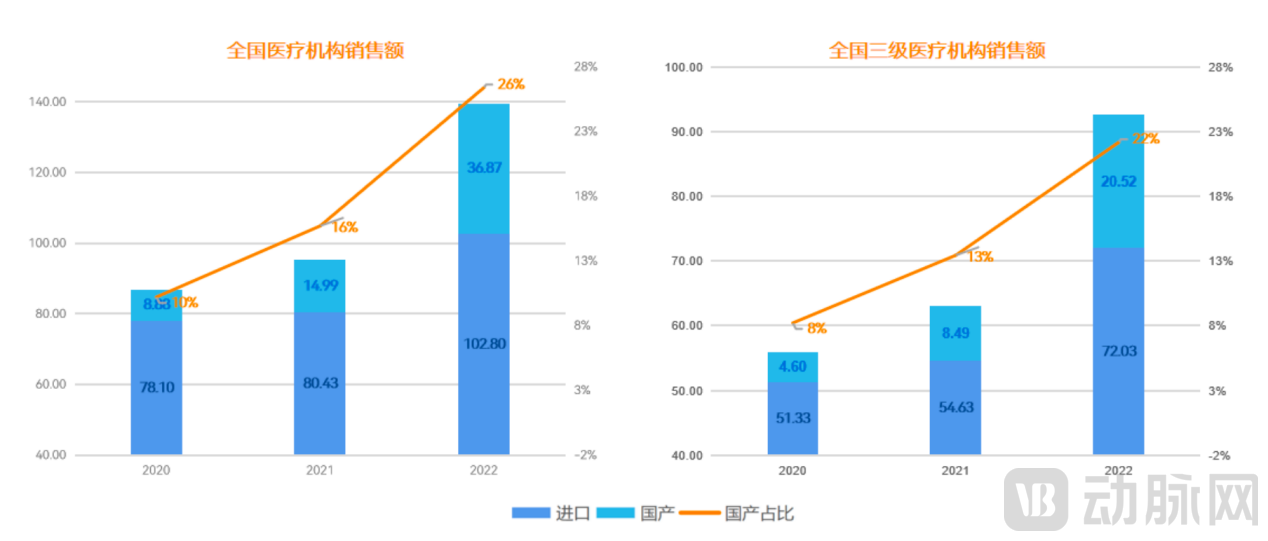
2020年—2022年国产医用内窥镜与进口医用内窥镜销售额情况(亿元)
资料来源:众成医械研究院,蛋壳研究院制图
值得一提的是,目前国产厂商们不仅接连在可重复使用内窥镜上取得了突破,而且还不断作出技术突破与创新。
例如目前热度较高的4K医用内窥镜细分赛道便发展迅速,涌现迈瑞医疗、开立医疗、远赛医疗等企业,逐步打破技术封锁,缩小与海外产品差距。而在相较传统可重复使用内窥镜技术研发难度,以及生产制造难度更高的复合型内窥镜领域亦呈现出良好发展势头,已有多项技术处于国内领先水平,让国产内窥镜在国际市场拥有一定话语权。
前不久连续获批3张国家药监局医疗器械注册证(倍晰®超细探头式共聚焦显微内镜系统(pcles)、电子内窥镜图像处理器、一次性使用胆胰管内窥镜导管)的精微视达,再次打破了垄断,为中国共聚焦行业发展添上浓墨重彩的一笔,在全球市场打响了中国高端医疗设备的品牌。
据悉,精微视达拥有全球最大的共聚焦显微内镜规模化生产制造中心,唯一连续牵头共聚焦领域两项国家级重点研发项目,并持续打造了多个中国首创、国产唯一、世界领先的共聚焦显微内镜产品,屡屡成为行业标杆和典型,且产品已在临床得到广泛应用。此次,精微视达将首度携全线高端医疗设备重磅登陆CMEF,展示这些自主可控的中国智造。
全球第二、国内唯一,精微视达产品覆盖多学科临床应用场景
共聚焦显微内镜是一项分辨率可达微米级别,并且具有光学切片能力的高端内窥镜技术。结合光学系统和独特算法,可实现超高分辨能力和超小观测端尺寸,并在体内实时显示与病理活检高度一致的细胞图像。
利用这种新型内镜诊断技术,在诊断中可实现无创光学活检及靶向精准活检、减少漏诊,同时提高诊断率、助力病理诊断;在治疗中可实现精准描绘手术切缘、切除多点病灶;在术后随访监测中,能降低术后残留及复发发生率,是内镜和微创诊疗的重要发展趋势。
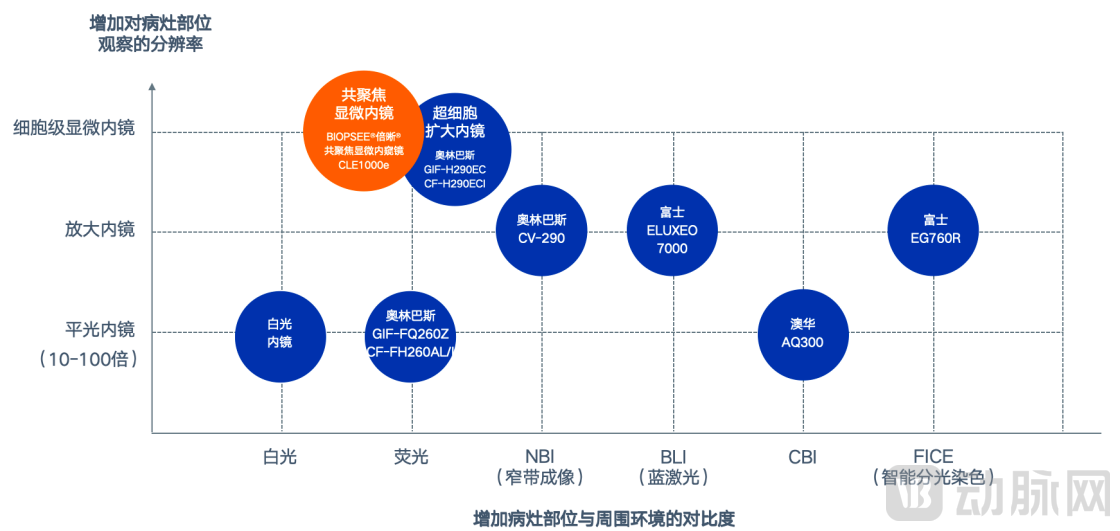

内镜技术发展趋势
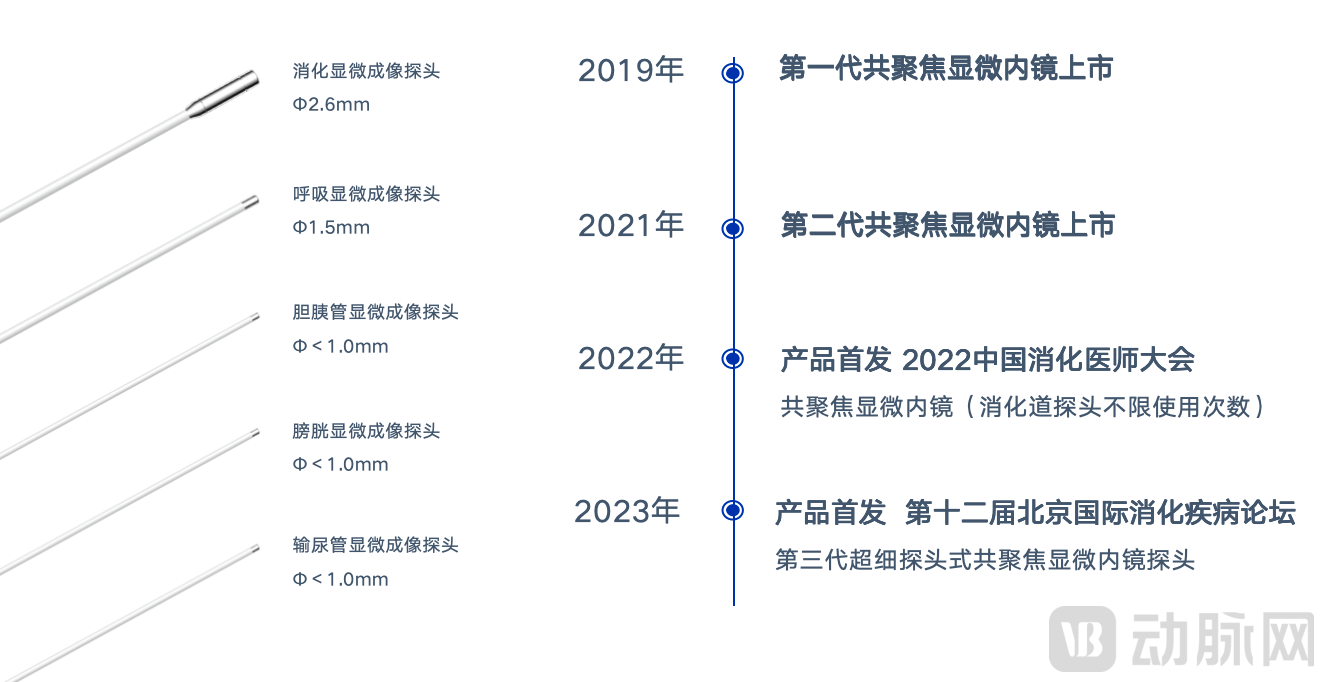
精微视达作为中国(共聚焦)细胞级内镜领先企业,自2014年成立以来便围绕“可视化活检产品线、诊疗通道产品线、早期肿瘤治疗产品线”三大产品管线进行产品开发及规模化生产,并于2019年斩获国内首张共聚焦显微内镜医疗器械注册证。
此后,企业保持创新研发活力,通过上下游联动,链接全产业链合作伙伴,助力产品核心技术快速突破,在2021年完成了第二代倍晰®共聚焦显微内镜的获批上市,并于2022年成功申报“十四五”国家重点研发专项“荧光共聚焦显微内镜核心部件研发”。今年更是连拿3张国家药监局医疗器械注册证,实现产品覆盖食管、胃、小肠、结肠、胆道、胰管等消化系统领域,膀胱、前列腺等泌尿系统领域,支气管、肺部等呼吸系统领域全系列应用场景。
在本次CMEF上,精微视达将展出的BIOPSEE®倍晰®超细探头式胆道共聚焦显微内镜系统、BIOPSEE®倍晰®超细探头式泌尿共聚焦显微内镜系统、BIOPSEE®倍晰®探头式消化道共聚焦显微内镜系统、FUSIONTM发现TM融合式胆道共聚焦显微内镜系统这4款产品,是该企业成功突破核心技术,并打通产品研发和生产关键环节的最好例证。


随着产品线的不断完善,精微视达进入大规模产品落地阶段。
已启动临床研究40+项,推动共聚焦显微内镜临床应用普及
事实上在此之前,精微视达已在全国多地开展共聚焦显微内镜试用、专业教育及培训活动。自2022年5月筹建营销团队以来,通过建立完善的售后服务体系、售后培训体系和医学服务体系等形式,半年时间内企业便累计实现消化领域区域学术样板医院的全覆盖,开展临床研究40+项,累计受益患者人数5000+。
其中,Biopsee®倍晰®已在全国140+家头部医院使用,于北京友谊医院、上海长海医院、南京鼓楼医院、上海仁济医院、北京清华长庚医院等多家全国top50医院完成装机。
但精微视达并未止步于此,而是保持产品研发、临床应用,以及市场落地共同推进。
如今,企业不仅通过完善的培训体系、充足的临床应用示范等形式推动技术普及,而且还以医工结合为导向,推动技术应用创新。例如,为让共聚焦显微内镜更好地服务临床,精微视达于上月新启动了40个临床研究项目全国招募计划,支持40家医院应用共聚焦显微内镜进行临床研究,将“临床研究项目”延伸至更大范围。
结合现今高端医疗器械行业发展情况来看,聚焦在填补行业空白、打破进口垄断、突破进口卡脖子或是国产自主创新的医疗器械,具有高技术含量和高应用价值,能够解决企业、临床和患者未被满足的需求。
但我们必须认识到,“高端”这一概念具有时效性,产品的成熟和迭代将推动“高端”产品迭代和突破路径的迁移。因此,即使是最初研发出填补行业空白或打破进口垄断产品的企业,也需要继续保持研发实力,不断推出新的产品,并完成新的突破,以保持领先地位,筑高壁垒。
精微视达就是一个很好的例子。尽管企业已在共聚焦显微内镜领域取得了国内领先的成就,但仍不断完善着企业的产品管线和发展战略。相信以此为方向,精微视达将在未来的全球市场竞争中获得更深入的发展和更快速的推广,最终实现全球领先。
2023深圳CMEF 精微视达邀您共襄盛会

欢迎扫描上方二维码预约参展
参考资料:
1.《2023高端医疗器械行业研究报告》,蛋壳研究院
2.《2023年医用内窥镜行业研究报告》,蛋壳研究院





























