11月26日,四川科伦博泰生物医药股份有限公司(以下简称“科伦博泰”)发布公告称,公司在研的RET小分子激酶抑制剂A400(KL590586,EP0031)获得了美国食品药品监督管理局(FDA)授予的孤儿药资格认定,用于治疗RET融合阳性实体瘤。
这是科伦博泰今年首个获得FDA孤儿药资格认定的在研药物,也是今年国内第23个获FDA批准的孤儿药。
RET基因是每个人都会携带的原癌基因,正常情况下RET基因受人体自身调控限制,不会引起正常细胞或肿瘤细胞的过度增长。但一旦RET基因发生突变,则可能导致癌细胞产生。数据显示,RET基因融合在NSCLC患者中的发生率约为1~2%,在甲状腺乳头状癌(PTC)中的发生率约为10%,在甲状腺髓样癌(MTC)中的发生率约为60%1。
目前传统化疗和免疫治疗是常用的治疗方法,但是对多靶点激酶抑制剂(MKI)和第一代RET选择性抑制剂(SRI)存在耐药性的患者来说,化疗和免疫治疗效果有限,且预后较差,他们可选择的有效治疗方式有限。因此,RET阳性肿瘤患者仍存在未被满足的临床需求。
A400是新一代SRI,对常见的RET基因融合和突变具有广泛活性,有望成为治疗RET+实体瘤的第二代SRI。其临床前研究结果显示,与一代SRI相比,A400在体外和体内对RET激酶表现出良好的抑制活性,对RET的抑制作用远高于VEGFR2、JAK1和JAK2。在动物模型中,它也表现出良好的血脑屏障穿透性。
此前,科伦博泰公布了A400针对RET基因改变的晚期实体瘤患者的I/II期临床研究结果。本次研究分为剂量递增(6个剂量组,10mg—120mg,QD)和剂量拓展(60mg/90mg,QD)两个部分,共纳入109例患者。
数据显示,在安全性方面,在A400 10—120mg组内未观察到剂量限制性毒性(DLTs),其中94.5%的患者出现治疗相关不良事件(TRAEs),但大多数为1-2级。在疗效仿麦呢,截至今年4月20日,在A400 40mg—120mg剂量范围内,90例患者疗效可评估,其客观缓解率(ORR)达60%,疾病控制率(DCR)达94%。在A400 90mg剂量组中,56例患者疗效可评估,其ORR达63%,DCR达95%。
值得注意的是,A400在6例基线有可测量脑部病灶的患者中,其中5例均未接受过放疗的患者脑部病灶缩小超过30%,其中3例脑部病灶完全消失。
2021年3月,科伦博泰与英国生物制药企业Ellipses Pharma LTD达成区域授权合作协议,将A400在欧美等区域权利有偿独家授权给Ellipses,科伦博泰保留大中华区及韩国、新加坡、马来西亚等部分亚太地区的权利,双方将在各自区域内进行开发、商业化等活动,并利用各自区域内数据支持项目全球研发。
2023年5月,科伦博泰完成了CDE临床咨询。目前,正在国内开展A400针对2L+晚期RET+ NSCLC的关键临床研究。
“罕见病”并不罕见,但是罕见病药物“罕见”。
根据《中国罕见病定义研究报告2021》数据,国内目前已知的罕见病数量大约有1400多种,而罕见病患者群体已超过2000万。《第一批罕见病目录》显示,截至目前,共有199种药物在全球上市,涉及87种罕见病;其中103种药物在中国上市,涉及47种罕见病。
尽管近年来国内罕见病药物上市数量呈现明显上市趋势,但相对于国外数量来说仍然较少,患者依然面临治疗药物不足、“境外有药,境内无药”的困境。
但罕见病药物可获得性低的局面正在逐步改善。相较于此前制药企业在罕见病领域望而却步,随着国家医药政策调整、临床需求增长等因素影响,国内药企正在积极布局罕见病药物研发赛道,加速罕见病药物研发。
根据《沙利文:2023中国罕见病行业趋势观察报告》数据,截至2023年2月,国内有81种罕见病药物(除化学仿制药和生物类似药)处于临床试验及上市申请阶段,涉及27种罕见病,其中46种药物由国内药企自主研发或参与引进,涉及16种罕见病。国内药企正积极推动罕见病药物研发,罕见病创新药也在不断涌现。
据不完全统计,截至目前,2023年国内共有23款在研药物获得FDA孤儿药资格认定。
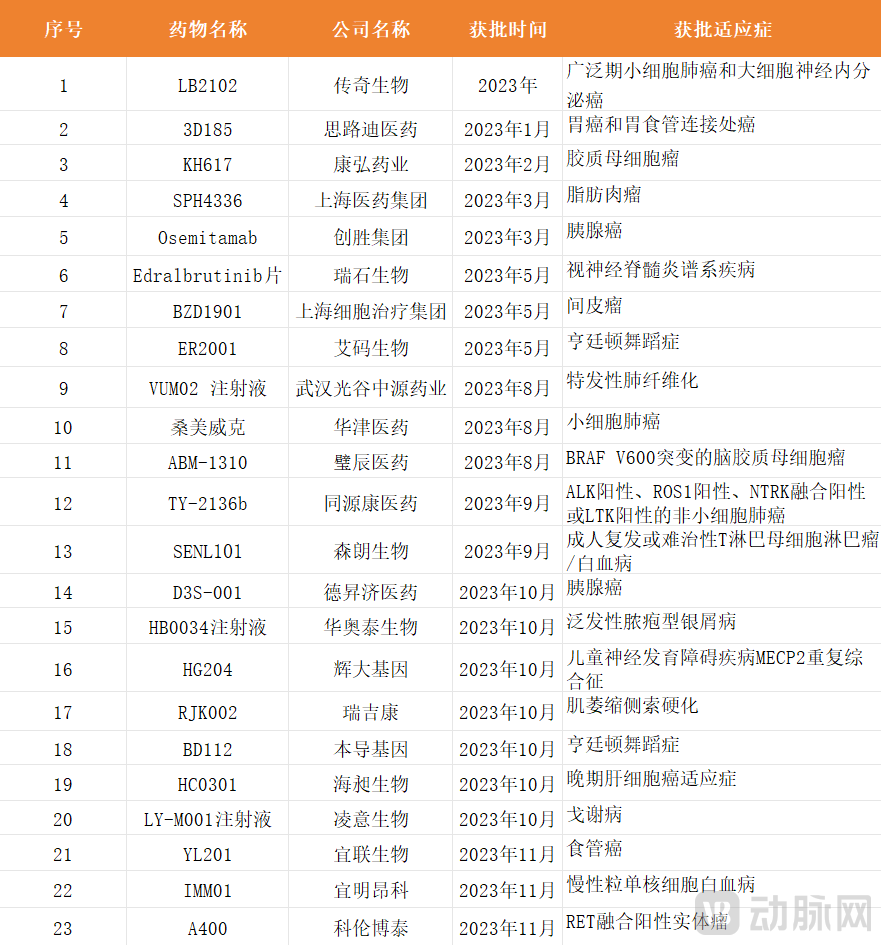 2023年国内FDA批准的孤儿药
2023年国内FDA批准的孤儿药
数据来源:公开数据整理,动脉网制图
随着罕见病药物上市产品不断增多,其市场规模也在不断扩大。根据弗若斯特沙利文公布的数据,2020年中国孤儿药市场规模约为13亿美元,预计到2030年,中国孤儿药市场规模将达到259亿美元,在全球孤儿药市场规模占比约7%。
未来,随着研发的推进和产品的获批上市,国内药企或将成为这一百亿美元市场的主导者,解决“无药可治”的难题。
参考资料:
1.Drilon A, Hu ZI, Lai GGY, Tan DSW. Targeting RET-driven cancers: lessons from evolving preclinical and clinical landscapes. Nat Rev Clin Oncol. 2018 Mar;15(3):151-167. doi: 10.1038/nrclinonc.2017.175. Epub 2017 Nov 14. Erratum in: Nat Rev Clin Oncol. 2017 Nov 28;: PMID: 29134959; PMCID: PMC7938338.





























