11月30日,艾伯维(AbbVie)与抗体偶联药物(ADC)开发商ImmunoGen宣布达成最终协议,艾伯维将以总额达约101亿美元收购ImmunoGen,并获得其经批准用于铂耐药性卵巢癌(PROC)的ADC药物ELAHERE®。
根据协议条款,艾伯维将以每股31.26美元现金收购ImmunoGen的所有流通股,ImmunoGen较周三收盘价溢价95%,在艾伯维的报价公开前,该股已经达到2015年以来的最高水平。此次交易预计将在2024年年中完成。
艾伯维董事长兼CEORichard A. Gonzalez表示:“本次收购加速了艾伯维在实体肿瘤领域的商业和临床业务布局,并且ImmunoGen其余的ADC管线进一步补充了艾伯维的ADC平台和现有肿瘤产品线。”
ImmunoGen成立于1981年,1989年成功IPO,是开发下一代抗肿瘤ADC的先驱,曾与Seagen、罗氏一同并称为ADC领域的“三巨头”。
ImmunoGen构建了专有的喜树碱ADC药物开发平台和集靶点筛选、抗体开发、毒素库、连接子库四位一体的ADC工具库。目前,公司管线包括用于多种不同实体瘤和血液恶性肿瘤治疗的潜在项目。其中,ELAHERE®是其进展最快的一款ADC。
 ImmunoGen的在研管线
ImmunoGen的在研管线
图片来源:ImmunoGen官网
ELAHERE®是一款靶向叶酸受体α(FRα)的ADC,由IgG1亚型抗FRα人源化单抗M9346A、微管抑制剂DM4(一种美登素衍生物)和连接子三部分组成。
当ELAHERE®与FRα结合后,FRα能够将其内化转移到细胞内部,ADC携带的细胞毒性分子从而抑制肿瘤细胞的有丝分裂,最终导致肿瘤细胞周期停滞和死亡。同时,在肿瘤细胞死亡和破裂后,DM4及其衍生物能够扩散到周围肿瘤组织,进一步通过“旁观者效应”对周围肿瘤细胞造成杀伤。
ImmunoGen在2023年美国临床肿瘤学会(ASCO)上公布了ELAHERE®的3期临床试验结果,本次试验评估了Elahere®与化疗在受过一至三线治疗的FRα阳性PROC患者中的安全性和疗效。
数据显示,接受ELAHERE®治疗的患者(n=227)的中位无进展生存期(PFS)为5.62个月,接受化疗的患者(n=226)的PFS为3.98个月。Elahere®治疗组的中位总生存期(OS)为16.46个月,化疗组的为12.75个月。此外,Elahere®治疗组的客观缓解率(ORR)为42%,而化疗组的为16%。
2022年11月,FDA加速批准ELAHERE®上市,用于治疗曾接受过一至三种全身治疗方案,且FRα阳性、铂类耐药的上皮性卵巢癌、输卵管癌或原发性腹膜癌的成人患者。这是目前全球首款且唯一获FDA批准的靶向FRα的ADC药物。
此外,2020年10月,华东医药以4000万美元首付款和高达2.65亿美元的里程碑付款获得了ELAHERE®在大中华区的独家开发和商业化权益。今年10月,ELAHERE®的上市许可申请(MAA)获得国家药品监督管理局药品审评中心(CDE)受理,不仅如此,ELAHERE®在欧盟的MAA也获得欧洲药品管理局(EMA)受理。
凭借良好的疗效,ELAHERE®刚上市便迎来了好的开局。根据ImmunoGen公布的2023年Q3财报,Elahere®第三季度美国净销售额为1.052亿美元,前三季度销售额达2.12亿美元。
这不是艾伯维第一次花重金布局ADC领域。
2016年,艾伯维以58亿美元收购肿瘤药企Stemcentrx,获得了其重点ADC在研药物Rova-T。Rova-T是一款靶向Delta样配体3(DLL3)的ADC,曾被认为是治疗小细胞肺癌(SCLC)的潜力药物。
然而,这58亿美元最终打了“水漂”,Rova-T的失败接踵而至。2018年,艾伯维停止Rova-T用于SCLC患者的3期试验,2019年,艾伯维宣布彻底停止Rova-T的开发。
随着这一次“打击”而来的,是接连被抛弃的ADC管线。截至目前,艾伯维共放弃了7款ADC管线。
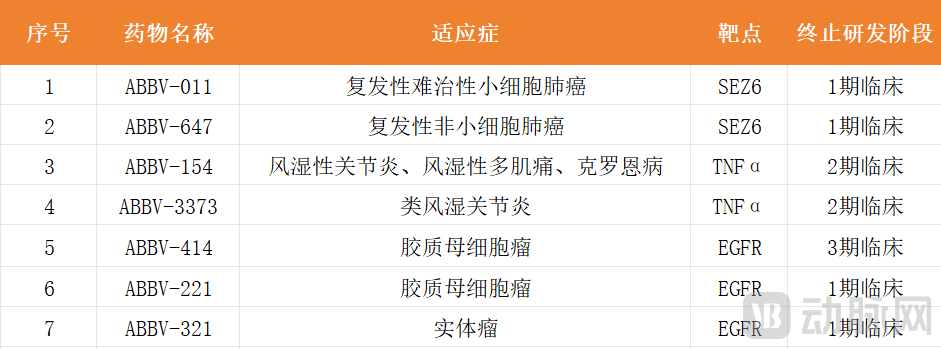 艾伯维放弃的ADC管线
艾伯维放弃的ADC管线
数据来源:公开数据整理,动脉网制图
作为最早入局ADC赛道的制药巨头之一,艾伯维的“ADC之路”最早可追溯到2008年。15年来,艾伯维对ADC的开发大体分为两条主线——自身免疫疾病和抗肿瘤领域。经过调整布局,目前艾伯维将ADC开发重点放在抗肿瘤板块,其中临床阶段的在研ADC项目有4款。
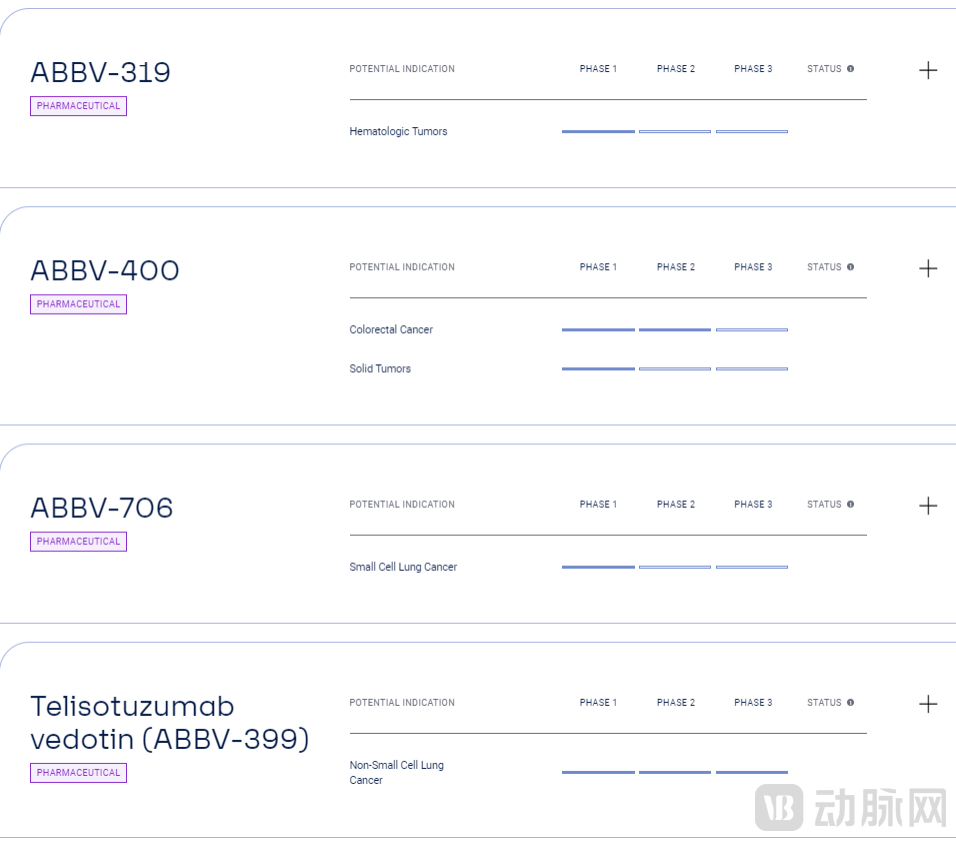 艾伯维在研ADC管线
艾伯维在研ADC管线
图片来源:艾伯维官网
其中最瞩目的,无疑是处于临床3期的ABBV-399。2022年1月,ABBV-399被FDA授予了突破性疗法资格,用于治疗晚期或转移性铂类治疗后进展的c-Met高表达EGFR野生型非鳞状NSCLC患者。
此外,根据Insight数据库数据,截至今年3月,全球已有15款靶向c-MET ADC在研药物,9款已进入临床阶段,但ABBV-399是目前全球唯一一款进入3期临床的c-Met靶向ADC。
目前,艾伯维已启动ABBV-399治疗NSCLC患者的3期M18-868研究,旨在评估ABBV-399联用多西他赛,在既往接受过治疗的c-Met高表达EGFR野生型局部晚期/转移性NSCLC患者中的疗效和安全性,这项研究预计在2025年6月完成。届时,艾伯维可能成为c-Met ADC赛道的破局者。
在布局ADC赛道前,艾伯维早已手握“药王”修美乐,在2012—2022这十一年时间,修美乐为艾伯维贡献了超2000亿美元的销售额,同时也问鼎了药王宝座十一年。但是,随着修美乐专利的到期,摆在艾伯维面前的,将是有史以来最陡峭的专利悬崖。
随着生物仿制药的出现,后续市场将继续被蚕食,修美乐或将走下药王神坛。2023年前三季度,修美乐销售额111亿美元,同比下降29.1%。而默沙东的王牌抗肿瘤药物Keytruda(K药)同期销售额为184亿美元,K药成为2023年前三季度全球最畅销药品,并极有可能取代修美乐成为2023年度药王。
进军ADC赛道成为艾伯维填平专利悬崖的办法之一。尽管Rova-T没有让艾伯维搭上ADC的发展列车,但它依旧希望通过并购来挖掘具有潜力的重磅药物。通过这次交易,艾伯维收获到的是已上市的ELAHERE®,这意味着,类似Rova-T的败局或将不再重演。ELAHERE®目前是艾伯维唯一一款上市ADC,成为艾伯维真正进入ADC市场的“入场券”。
不过,近两年来ADC药物赛道异常火热,全球创新药企纷纷下注入局。今年3月,辉瑞宣布以430亿美元收购ADC先驱Seagen;10月,默沙东与第一三共达成220亿美元ADC研发合作……据医药魔方统计,截至2023年1月,全球共有15款ADC药物获批上市,此外,全球共有400余个ADC在研药物,其中进入临床阶段的超过200个。
在竞争激烈的ADC市场,未能抢占先机的艾伯维要想在众多玩家中脱颖而出,除了花钱买管线外,还需在靶点、抗体、载荷、连接子以及毒性和适应症等方面突破技术壁垒,打造具有差异化优势的创新产品。





























