2003年,今又生(Gendicine)获国家食品药品监督管理局批准上市,成为世界首个获批上市的基因治疗药物。今又生的上市,为当时处于低谷的基因治疗行业带来了新的希望,被称为“基因研究和生物高技术领域新的里程碑”。随着新载体的开发和技术的发展,在今又生获批后的近20年,CGT疗法不断迎来新突破,CGT产业发展势如破竹。据不完全统计,目前全球范围内已有超50款CGT疗法获批上市。
而数款CGT疗法接连获批上市的背后,少不了“卖水人”——CGT CDMO的贡献。与传统药物研发相比,CGT疗法投入的研发成本更高。根据Frost & Sullivan的报告,CGT疗法在发现和临床前阶段的研发费用在9亿—11亿美元,临床阶段的费用在8亿—12亿美元。与此同时,CGT产业发展还面临着质量和批次一致性问题、高成本和高定价的限制等诸多挑战。因此,CDMO成为CGT药企降本增效的重要策略,CGT CDMO市场迎来了快速扩容与发展,吸引着无数精英人才和资本入局。
BioCentriq便是一家提供全方位服务的全球性CGT CDMO企业。公司成立于2019年,总部位于美国新泽西州纽瓦克,目前建立了成熟的质量体系和现代化的基础设施,公司提供的服务与解决方案包括工艺开发、临床制造和分析测试等,涵盖CGT产品的整个生命周期。通过提供专业综合的一站式CGT CDMO服务,BioCentriq希望缩短候选药物研发时间,并降低其成本和临床试验风险,以将有疗效的创新药物更快送达患者手中。
2022年4月,BioCentriq与韩国GC绿十字公司(Green Cross Holdings Corporation)签署最终协议。GC将收购BioCentriq的100%股份,以拓展公司CGT CDMO平台的能力,并加强其在全球CGT市场的影响力。本次交易金额为7300万美元(约合5.3亿元人民币),其中GC母公司将出资5300万美元,子公司GC Cell出资2000万美元。
BioCentriq由美国新泽西创新研究所(NJII)孵化,是美国首个在大学校园内建立的CGT疗法开发和制造中心。成立仅一年后,BioCentriq便与多个行业内领先组织建立了战略合作伙伴关系,包括PALL、KYTOPEN、Terumo Blood and Cell Technologies等。
2020年,BioCentriq在北美建设GMP生产设施,并于次年正式投入使用。截至目前,BioCentriq在北美与韩国总共拥有14个GMP级生产设施,包括中试工厂、AMD、PD和QC实验室以及配套基础设施,具体包括4个用于CGT疗法制造的ISO-7认证洁净室、用于工艺开发与中试的BSL-2全套设备、用于过程及分析测试的质量控制实验室以及仓储与培训实验室等。
发展至今,BioCentriq所有生产基地均配备了标准设备,同时建立成熟的质量体系和程序,并且均可采用开放式和封闭式工艺生产自体和同种异体疗法,从而为全国客户提供覆盖CGT产品研发全周期的CDMO服务与解决方案。
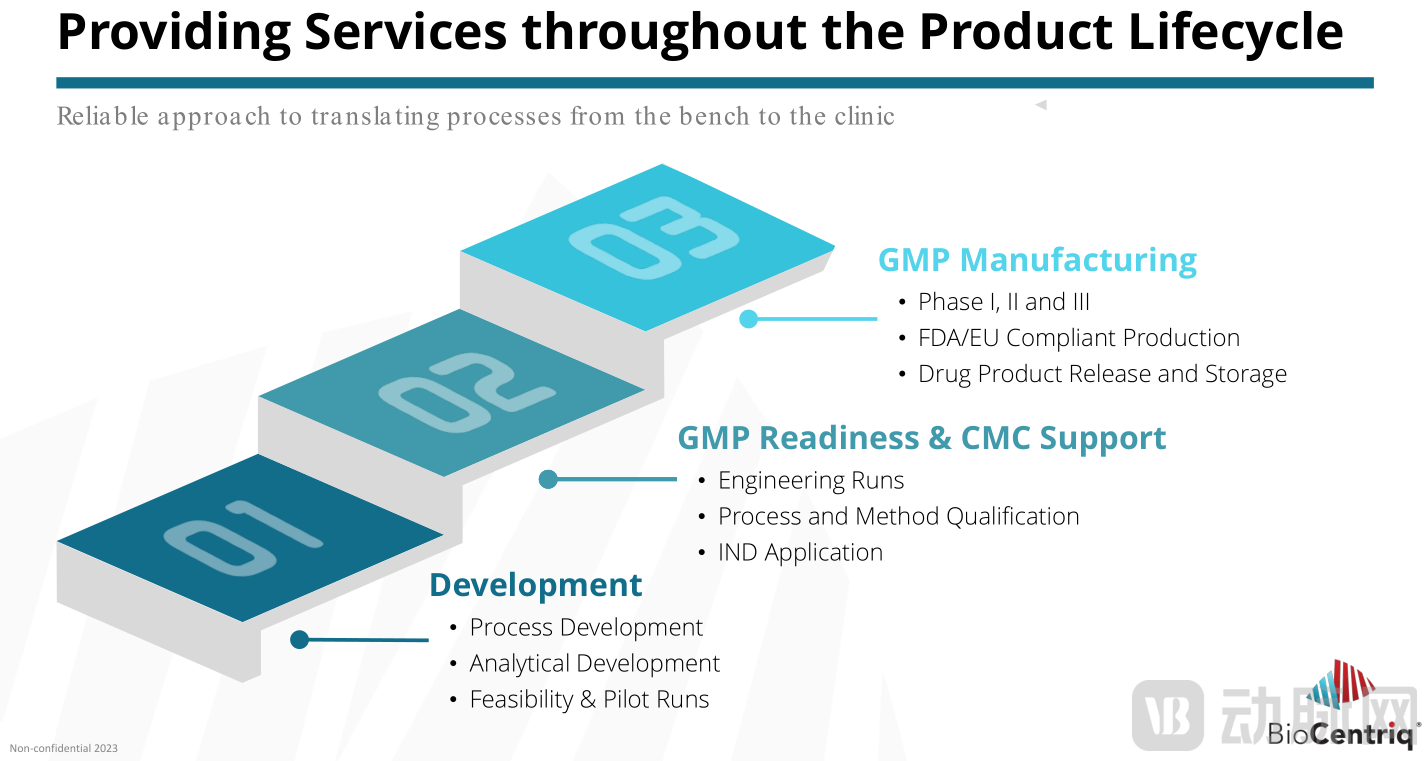 BioCentriq提供的CGT CDMO服务 图源:BioCentriq官网
BioCentriq提供的CGT CDMO服务 图源:BioCentriq官网
除此之外,BioCentriq还打造了一支超80人的具有丰富专业经验的工程师和科学家团队,以确保候选产品从实验室到临床的无缝转化。其中公司团队成员包括,公司CEO James Park,此前他曾在BMS、Merck等跨国生物制药公司担任领导职务,拥有丰富的生物开发、CMC和制造运营以及人员管理经验。公司运营副总裁Mark Broadley在制药和医疗设备制造行业拥有20余年经验,曾担任Charles River Laboratories运营高级总监,领导多个CGT产品的生产运营的日常运营。公司发展副总裁David Smith在再生医学领域拥有15年以上的经验,此前他曾担任Ori Biotech的技术运营副总裁,领导了该公司在细胞治疗制造领域首个创新技术的技术战略实施。
 BioCentriq核心团队成员 图源:BioCentriq官网
BioCentriq核心团队成员 图源:BioCentriq官网
为了加速和优化CGT产品的研发生产流程,为客户提供下一代制造解决方案,BioCentriq通过合作和创新,开发了一个新兴工艺技术平台——LEAP™平台。2023年6月,BioCentriq在第29届国际细胞和基因治疗学会(ISCT)年会上正式推出了LEAP™平台。
LEAP™平台旨在帮助处于早期阶段的生物技术公司加速产品研发速度,并降低IND研究和临床生产的成本与风险。在BioCentriq已有的资产和专业知识的基础上,LEAP™平台可提供多种模式,例如LEAP-NK™、LEAP-CAR™、LEAP-TCELL™、LEAP-TREG™、LEAP-MSC™等。其中,LEAP-NK™平台使用专有的供体细胞系可以将NK细胞的扩增数量提高12000倍以上,此外,该平台还能够将NK细胞扩增过程扩展到搅拌槽生物反应器,从而实现大规模且经济高效的生产。
BioCentriq公布的数据显示,LEAP™平台采用经过验证的生产工艺和分析方法,能够将工艺开发和扩大生产时间缩短高达 75%,在6个月内即可实现从项目启动到患者给药的研发进度,最终能够将临床生产时间缩短50%,同时能够降低临床试验过程中的风险。
凭借专业的技术平台与服务能力,BioCentriq在转让、开发和制造用于临床试验的GMP药物产品方面积累了良好的业绩记录,目前已将4个CGT疗法商业化,并将20多个项目推进至临床研究阶段。
此外,在2024年2月,细胞免疫治疗药物研发商GC Cell宣布与BioCentriq签订工艺转让协议。GC Cell将通过利用 BioCentriq 的细胞疗法工艺开发、分析方法开发和生产制造等服务与解决方案,将自体免疫细胞疗法Immuncell-LC 引入美国市场。
BioCentriq的专业服务能力获得了资本的青睐。2024年1月,BioCentriq宣布完成2920万美元A轮融资。凭借此次融资,BioCentriq 有望进一步加速其创新能力,为CGT疗法开发和制造提供端到端解决方案。融资资金将用于增强BioCentriq的生产设施、技术创新以及扩大其优秀的专家团队,以满足对可扩展细胞疗法解决方案日益增长的需求。
除此之外,在2023年6月,BioCentriq与全球生物技术公司Cytiva宣布获得美国国家生物制药制造创新研究所(NIIMBL)的资助,以进一步加速CGT疗法的开发与创新。
目前,CGT行业已迎来快速阶段。根据ASGCT的统计数据,截至2022年第三季度,全球在研CGT管线达2031个,呈逐季度上升趋势。FDA此前也表示,自2025年起,每年将批准10—20个CGT疗法,这为行业发展注入了巨大的信心与期望。根据Frost&Sullivan预测,2025年全球CGT疗法的市场规模有望达到305.4亿美元。
随着越来越多的CGT疗法获批和进入商业化阶段,创新药企对于CGT CDMO的需求也将随之增加,外包趋势日益凸显。根据Frost&Sullivan分析,全球CGT CDMO市场将从2020年17.2亿美元增长至2025年78.6亿美元,年复合增长率达35.5%。
对于BioCentriq而言,公司早已做好布局并深耕这一赛道的准备。除加强自主创新巩固自身实力外,在新一轮融资的支持下,BioCentriq正在积极推动对外合作,加强自身CDMO服务的专业性与综合性。
2024年1月,BioCentriq与CGT疗法关键制造管理系统开发商Autolomous达成合作。BioCentriq将利用Autolomous的autoloMATE平台等数字化技术加速工艺开发和制造活动。BioCentriq开发副总裁David Smith博士表示,“Autolomous的autoloMATE 平台将改变我们的运营方式,通过简化整个开发和制造过程中的数据处理过程,我们将能够提高运营效率和灵活性并降低风险,最终更快地为患者提供治疗药物”。





























