7月24日,专注于放射性核素偶联药物(RDC)领域的生物制药公司Telix Pharmaceuticals(“Telix”)发布公告,宣布已成功发行了价值6.5亿澳元(约合31亿人民币)的可转债。
根据公告,Telix本次可转债2029年到期,期限为5年,票面利率为2.375%,初始转换价为每股普通股24.78澳元,较参考股价(每股普通股18.70澳元)溢价 32.5%。此次发行预计将于2024年7月30日完成。对于资金用途,Telix表示,这笔资金将为公司提供财务灵活性,以用于进行具有战略意义的并购交易,并继续投资于全球供应链和生产制造。
据动脉橙产业智库统计,这是2024年核药领域的最大额度融资,刷新了此前德国核药公司ITM Isotopen Technologien München完成的1.88亿欧元(约合14.8亿人民币)融资金额。
Telix成立于2015年,总部位于澳大利亚墨尔本。公司主要专注于诊断和治疗放射性药物的开发和商业化,在比利时、瑞士、日本和美国均设有国际业务。Telix 的技术使用靶向辐射成像和治疗相结合,有可能改变临床医生发现和治疗癌症和罕见疾病的方式,更好地为治疗决策提供信息,并为患者提供真正的个性化治疗。
2017年11月,Telix在澳大利亚证券交易所上市。彼时,Telix的市值还不到4000万美元。截至2024年7月25日,Telix市值64亿澳元(约合42亿美元),上涨超100倍。
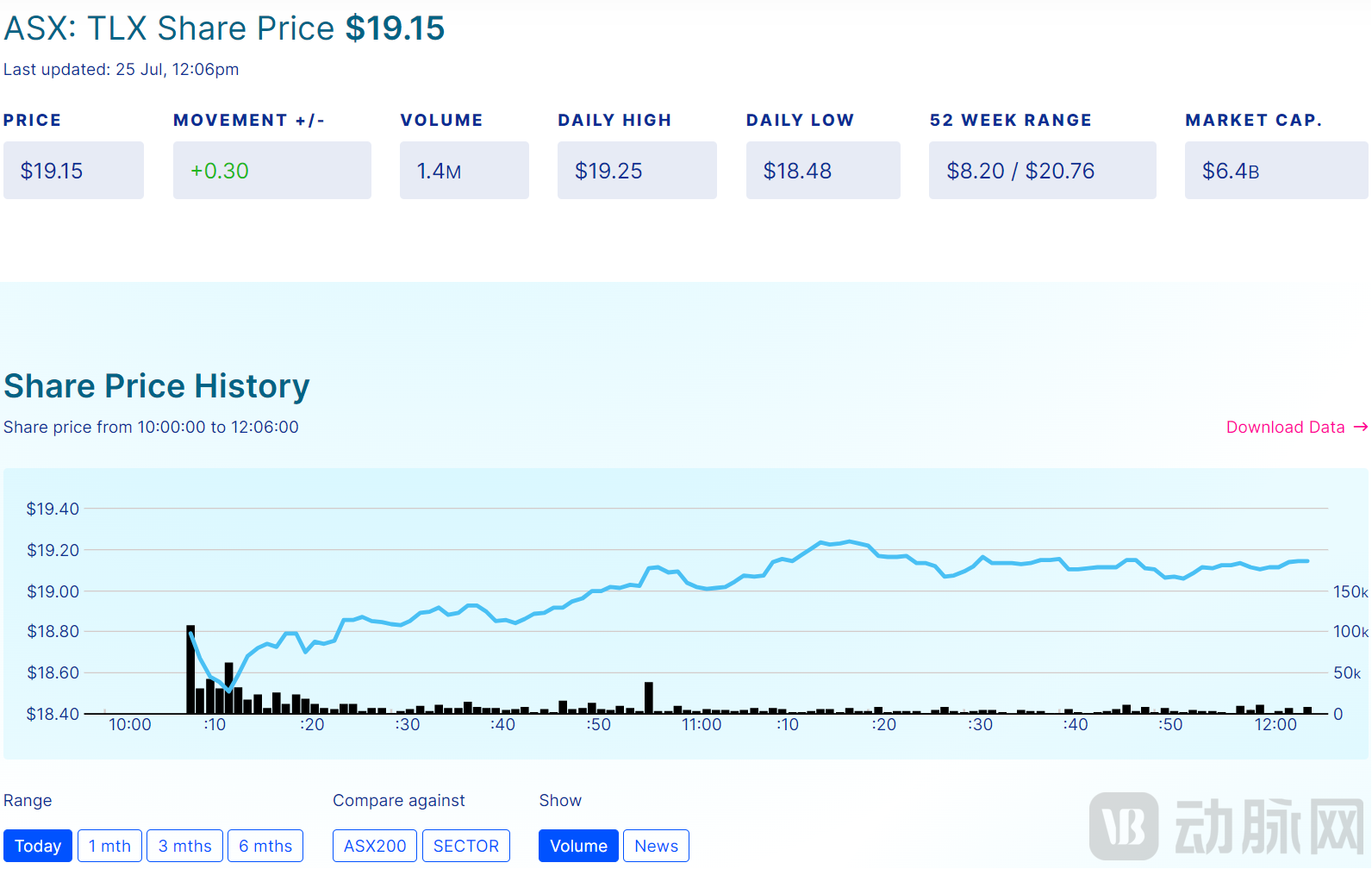 图源:Telix官网
图源:Telix官网
此外,通过接连的并购和合作,Telix在短时间内实现了业务版图的扩展,并扩充了自身的研发管线和生产能力。据不完全统计,Telix目前已收购了8家公司。
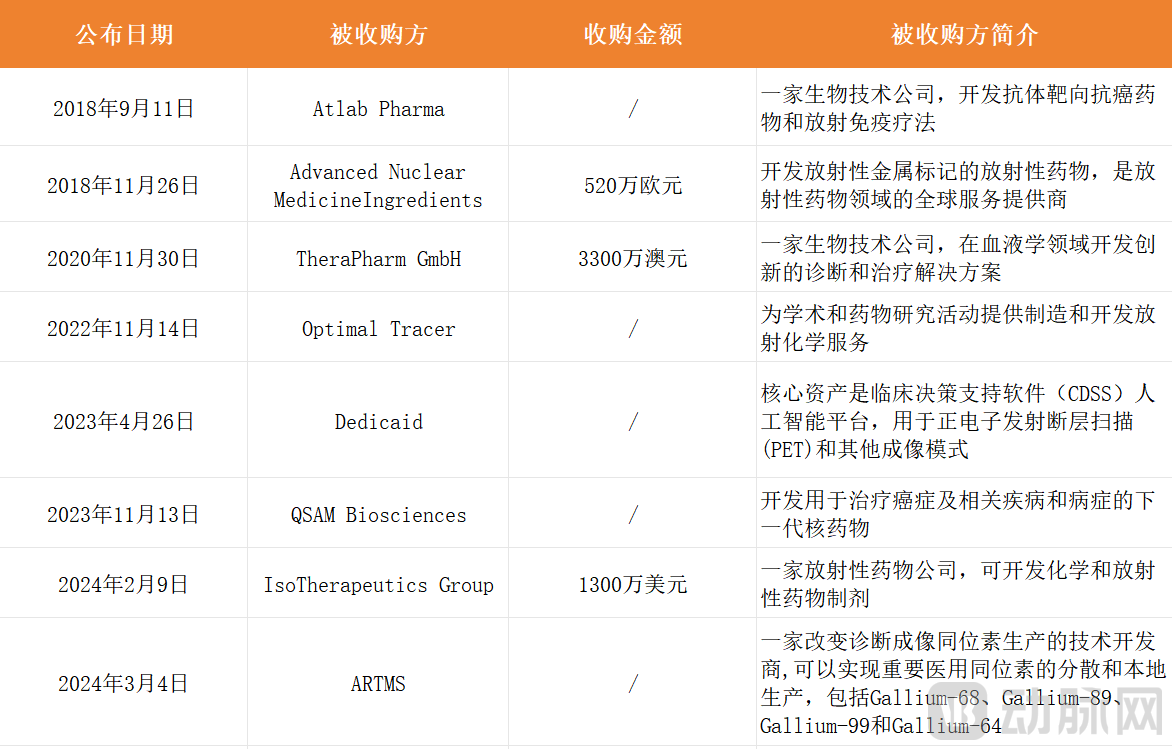 Telix收购情况 图源:数据来源于crunchbase,动脉网制图
Telix收购情况 图源:数据来源于crunchbase,动脉网制图
在对外合作方面,Telix的表现更是十分积极。据不完全统计,上市至今,Telix已有15笔合作。
值得一提的是,远大医药曾与Telix达成了总价不高于2.5亿美元的合作。2020年11月,远大医药宣布与Telix 签订了包括产品授权、独家商业化推广权益以及认购股权等协议。
根据协议,远大医药将获得Telix开发的多款用于肿瘤治疗的创新型放射性核素偶联药物(TLX591-CDx、TLX250-CDx、TLX599-CDx)在中国的独家授权、开发、生产及商业化权益。同时,在未来一定期限内,远大医药将获得Telix其他管线产品在中国的独家开发、生产及商业化权益等的优先谈判权。并且,远大医药将在协议约定的相关条件满足后,以2500万美元认购Telix约7.6%的股本权益,加上授权协议中累计支付的预付款及里程碑款项最多2.25亿美元,交易总价将不高于2.5亿美元。
发展至今,Telix围绕泌尿肿瘤(前列腺和肾脏)、神经胶质瘤、肌肉骨骼肿瘤、骨髓调理4大疾病领域,布局了广泛的治疗诊断放射性药物候选产品管线。目前,Telix已有首款获批商业产品——前列腺癌成像剂Illuccix([68Ga]GaPSMA-11)。
Illuccix是一种用于制备镓-68(68Ga)戈泽肽(PSMA-11)注射液的试剂盒。这是一种放射性诊断剂,能够在室温下进行快速放射性标记,具有高放射化学纯度和生产一致性,适合商业和医院放射性药房环境。其作为靶向前列腺特异性膜抗原(PSMA)的诊断型正电子发射断层扫描(PET)示踪剂,给药后,与PSMA结合,通过PET成像,可显示身体组织中存在PSMA阳性的前列腺癌病变。
2021年11月,Illuccix获得澳大利亚治疗用品管理局(TGA)批准,2021年12月获得美国食品药品管理局(FDA)批准,2022年 10月,获得加拿大卫生部批准。
自2022年4月Illuccix正式上市销售以来,截至2024年3月1日,Telix已从Illuccix 的产品销售中获得了8.243亿澳元(约合5.4亿美元)的收入,其中98%的收入来自美国的销售。根据Telix公布的2024年第二季度财报,该季度营收约为1.24亿美元,同比增长55%,而这主要得益于Illuccix的营销收入。
Telix还在积极扩展Illuccix的适应症标签,以扩大其使用范围。2023年3月,Illuccix的补充新药申请(sNDA)获FDA批准,用于选择适合诺华新药Pluvito(177Lu-PSMA-6017)治疗的晚期前列腺癌患者。标签扩展意味着,Illucix成为首个FDA批准的、用于选择PSMA靶向放射配体疗法(Pluvicto)潜在患者的药物,其为临床医生提供了帮助优化和指导治疗决策的关键信息。
2023年5月,Telix宣布与拜耳达成协议,为3期ARASTP研究提供Illuccix。这项全球研究正在调查拜耳雄激素受体抑制剂(ARi)达罗他胺加雄激素剥夺疗法(ADT)与单独ADT治疗激素敏感型前列腺癌、常规影像学检查无转移证据且基线PSMA-PET/CT阳性的高危生化复发患者的疗效。
与此同时,Telix还在积极开发其他放射性疗法,目前布局了多个临床管线,并已积累了大量临床试验数据。
其中,TLX591(177Lu-DOTA-rosopatamab)是一种放射性抗体靶向的前列腺癌候选药物。目前,Telix正在关键的3期临床试验中评估TLX591在前列腺癌首次复发到晚期转移性疾病所有阶段的疗效。目前,美国多个试验点正在启动并准备为首批患者给药,预计将在2025年上半年报告初步中期数据。
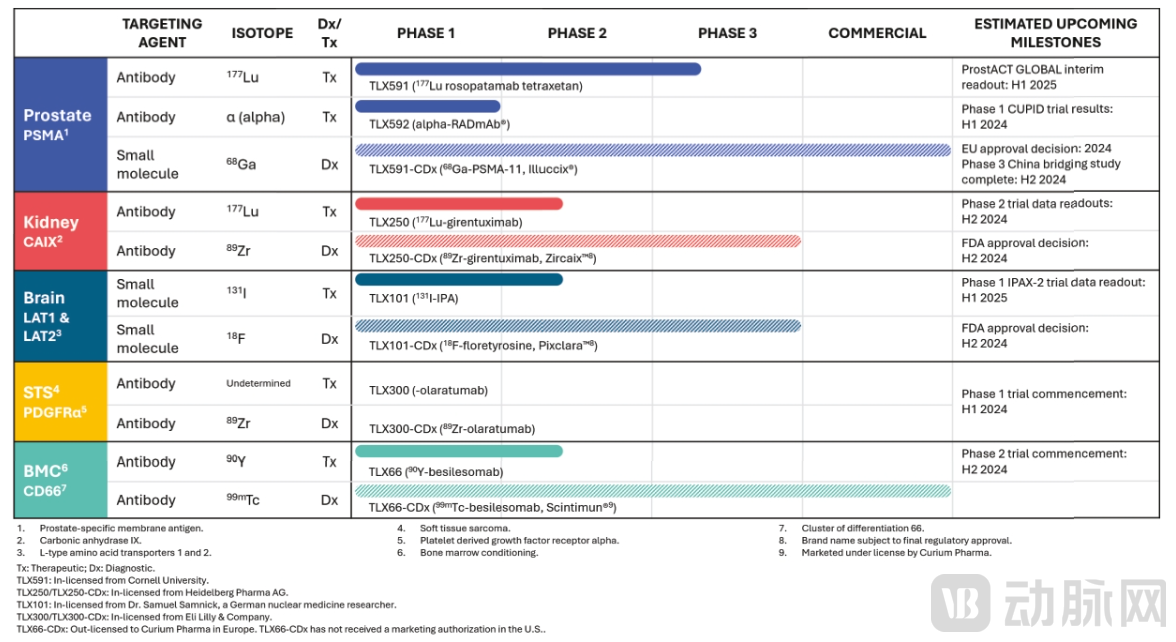
图源:Telix招股书
再次谈到Telix此次通过发行可转债获得的6.5亿澳元。值得关注的是,这6.5亿澳元是在Telix叫停IPO后,获得的最新一轮融资资金。
2024年6月初,Telix官宣了最新的IPO计划,拟募资金额约为2亿美元,预计将于6月14日登陆纳斯达克,并计划募资约2.02亿美元。不过,在原定IPO的当天,Telix宣布,选择撤回其在美国首次公开募股的提议。
对此,Telix表示,鉴于拟议的纳斯达克上市并非基于筹集资金的需要,公司管理层和董事会决定不按照当前市场条件下提供的条款推进交易。公司认为拟议的折扣与其对现有股东的责任不符。
从Telix的发展以及目前美股IPO市场现状来看,Telix在敲钟前一刻叫停IPO并非没有原因。一方面,据不完全统计,2024年上半年共有9家生物技术公司在纳斯达克成功IPO。其中,3家最新股价高于发行价,1家公司持平,其余5家均破发,股价破发率高达55.6%1。由此来看,此时登陆纳斯达克,并非最好选择。在官宣美股IPO计划后,Telix在澳洲交易市场的股价经历了一波下跌。
另一方面,Telix现金流跑道健康。根据Telix招股书披露的数据,截至2024年3月31日,公司拥有现金及现金等价物1.227亿澳元(约合8030万美元)。换言之,在核药爆火的当下,拥有商业化产品以及多款候选资产的Telix不缺钱。
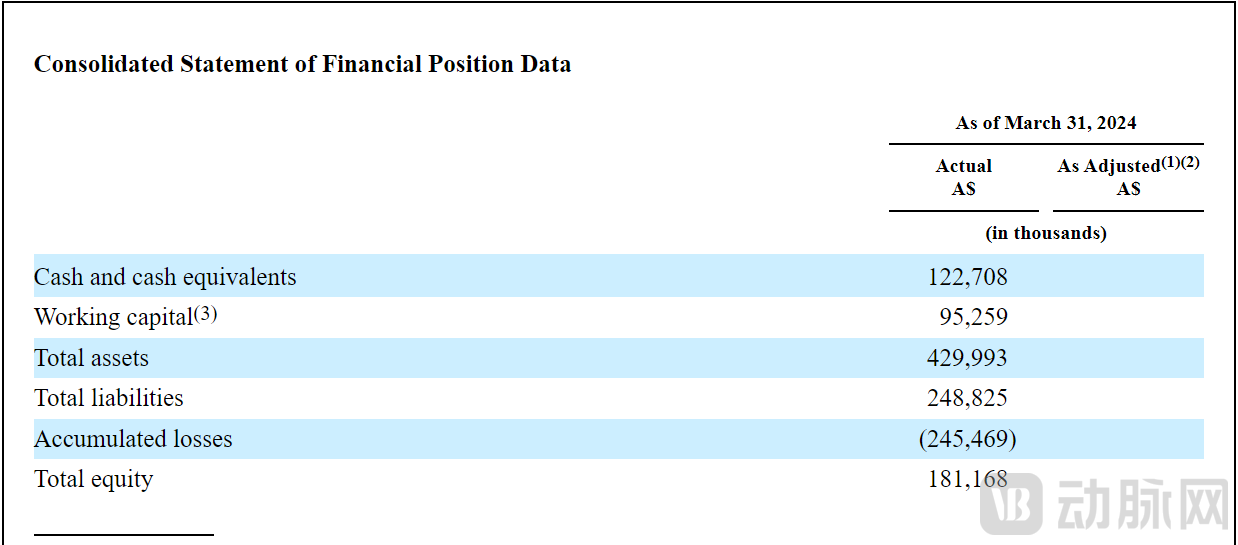 图源:Telix招股书
图源:Telix招股书
因此,相比于IPO,可转债对于Telix来说更是一个好的选择。董事总经理兼集团首席执行官Christian Behrenbruch博士表示:“可转换债券为我们提供了有吸引力的低成本融资,这显然是Telix发展历程中的一个转折点。此次发行的债券为我们提供了财务灵活性,让我们能够执行战略重点,同时减少现有股东的潜在稀释。我们能够利用强大的业务执行力和市场条件来提供有吸引力的融资条件。”
不过,叫停IPO并不意味着Telix真的不缺钱。
尽管目前Telix通过Illuccix实现了营收的增长,但是,目前Illuccix的营收增速正在放缓。根据其2024年第二季度财报,2024年Q2,Illuccix销售额的环比增幅为8%,远低于2023年Q3的14%增幅。而目前,Illuccix的销售额体量仍未突破10亿美元。
需要注意的是,产能和配送是核药领域企业必须解决两大难题。但是,目前放射性同位素原料面临着全球短缺问题,并且仍未形成成熟、完备的供应链体系,这两大因素极大限制了核药市场份额的拓展。
由此来看,Telix的8030万美元现金流不足以支撑其搭建更多的产能与供应链。更何况,Telix手中仍有多个在研项目以及候选产品亟需推进研发与商业化进程。在此情况下,6.5亿澳元无疑成为Telix扩大版图的巨大推动力。
目前,Telix3个项目——TLX007-CDx、TLX250-CDx (Zircaix)、 TLX101-CDx (Pixclara)已经临近商业化。
其中,TLX007-CDx是一种用于准备前列腺癌PSMA-PET成像的新型专有冷冻试剂盒。2024年7月24日,Telix宣布,FDA已接受其TLX007-CDx的新药申请(NDA)。PDUFA 的目标日期为2025年3月24日。如若TLX007-CDx获批,其将扩大PSMA成像产品的销售范围。
TLX250-CDx Zircaix)是一种适用于ccRCC诊断的PET诊断成像剂。2023年12月,Telix向FDA提交了TLX250-CDx的生物制品许可申请(BLA)。在获得监管部门批准后,公司计划在2024年下半年将TLX250-CDx 商业化,届时TLX250-CDx将有望成为美国肾癌领域首个靶向放射性药物成像剂。
TLX101-CDx(Pixclara)是一种PET诊断剂,旨在通过靶向LAT1和LAT2受体对脑癌性病变进行成像。Telix于2024年第二季度通过505(b)(2) NDA监管途径向FDA提交了TLX101-CDx的NDA,用于表征治疗相关变化引起的进行性或复发性胶质瘤。Telix表示,监管机构预计于2024年下半年做出批准决定。此外,Telix还计划对TLX101-CDx进行标签扩展3期试验,用于对非脑癌(包括肺癌和乳腺癌)脑转移患者进行成像。
参考资料:
1.药时代.>50%破发!2024年纳斯达克IPO的biotech公司依然面临挑战





























