近年来,全球生物医药行业竞争的激烈,日趋复杂的研究方案和临床终点,不断增加的研究中心数量和受试者数量,带来了药物研发成本攀升、研发周期延长、临床研究要求不断提高等一系列连锁反应。
传统的临床研究面临着试验设计、患者招募、数据管理及试验监查等多重挑战,如果再考虑将真实世界数据纳入到临床研究之中,更增加了研究设计和数据应用的复杂度。
随着AI技术在临床研究领域的快速发展和不断渗透,一种端到端的数字化智能临床研究模式——E2E(eSource-to-EDC)模式开始兴起。
E2E模式有利于降低临床协调员(CRC)在多源异构多模态的数据源(如HIS/EMR/LIS/PACS,纸质版数据)中去查找临床研究的原始数据,并进行重复性的手动数据录入模式下所必然产生的高额人力成本和时间成本,并且在患者筛选、招募效率、数据质量及研究运营效能等临床研究的关键环节价值显著,能够有效推动研究成本的降低,实现研究效率和研究数据质量(准确性、完整性和一致性)的提升。
本文旨在以E2E模式为核心,对国内外E2E模式的发展情况进行剖析,探索该模式的发展现状、行业价值以及商业化进展等,以期推动中国临床研究的数智化转型,进一步提升研究质量和效率。
AI重塑新药临床试验,E2E成为临研数智化转型的重要手段
近年来,中国已成为全球临床试验总次数最多且增长最快的国家。根据国家药品监督管理局药品审评中心(CDE)发布的数据,2023年中国药物临床试验登记与信息公示平台登记的临床试验总量首次突破4000项,达到4300项,较2022年增长26.1%。其中新药临床试验数量为2323项,与2022年相比增长了14.3%。
尽管中国在新药研发领域取得了显著进展,但诸如受试者招募难、数据收集和监查成本高等挑战仍然存在。研究显示,2020 年中国新药临床试验批准后一年开始招募受试者的比例只有 45.4%。临床试验数据的规范化收集,包括录入和核查,不仅耗时耗力,而且难以保证数据的高精确度。
随着大模型时代到来,AI凭借强大的学习与分析能力,正以前所未有的势头重塑新药临床试验运营模式。
AI技术的价值在于辅助研究人员更快捷、更高效地完成临床研究,不仅能够提高数据处理和分析的效率,还能够通过机器学习和深度学习等技术预测临床试验的结果,优化试验设计,提高临床试验的成功率。
在临床研究方案的设计与执行的各个环节中,AI都能实现强力助力。比如,AI可以提高纳排标准选择的效率与准确性,提升患者招募与筛选的精确度,还能够帮助药企进行风险因素识别与分析。其亦在合成对照臂(SCA)和虚拟临床试验、数据管理与分析等各方面发挥重要作用,有望进一步提升临床试验的自动化与智能化水平。
通过高质量的医疗数据和人工智能技术加持,未来AI将从根本上推动临床研究的范式变革。
近年来,国内外已相继有企业和研究机构采用医疗数字化和AI等技术提升临床研究效率。E2E模式作为其中的典型代表,正逐步发展为推动临床研究数据自动化和智能化管理的重要手段。
E2E模式的重点在于建立了电子源数据(eSource)和电子数据采集系统(EDC)端到端的数据直连,能实现数据的自动化采集和管理,从而提高数据的准确性、完整性和实时性。同时,该模式也使得临床试验参与各方能够在远程情况下,利用人工智能模型和大数据技术,保障临床试验数据采集效率和整体质量,同时兼具流程控制、安全保障、系统合规等诸多方面优势。
与传统模式相比,E2E模式这一将电子源数据智能生成、分析和质控平台、数据自动化采集和转录、数据驱动的远程化、基于风险的监查等系统有效融合的方式,可以达到更小程度的人工干预,系统性提升临床研究效率和数据质量。在保证数据安全与个人信息隐私的前提下,实现数据和操作的有效监管。
E2E模式在国外已有成熟案例,中国正在迅速崛起
目前,E2E模式在欧美等海外市场的应用已经相对成熟。其中,基于美国市场的特点,E2E的应用主要以两种方式展开。第一种是统一对接HIE平台(Health Information Exchange),先统一标准数据格式,然后进行数据采集。这一方式是基于美国的HIE平台网络的多年积累,该平台整合了不同医疗机构和区域的医疗记录、实验室结果、影像资料等数据,能够实现跨机构、跨区域的医疗信息互联互通。
另一种应用方式则是逐一跟医院进行合作,这一模式更易于复制和推广。以IQVIA为例,作为全球CRO领导者,IQVIA在全球范围内积极推动E2E技术的应用,以提高临床试验的效率和患者体验,同时也在数据收集和分析方面发挥了重要作用。
IQVIA通过不同的业务单元和合作伙伴,为不同地区提供定制化的E2E服务,以满足临床研究的特定需求。目前IQVIA的E2E全球布局已覆盖至北美、欧洲和亚太地区,并计划扩展到加拿大、日本和其他欧盟国家。
在美国,IQVIA通过Inteliquet提供E2E解决方案。Inteliquet在美国拥有12个研究中心,专注于肿瘤学研究,利用E2E技术进行临床试验的数据收集和管理。
相比国外,中国在E2E方面的应用较晚,但发展速度较快。璞睿作为IQVIA全球临床试验创新网络的重要贡献者,负责E2E模式在中国的开发和应用推广,璞睿在中国完成50多家研究中心布局,在全球占据领头羊地位。
璞睿是国内首家实现E2E技术在临床研究数据运营自动化应用的公司。据了解,璞睿构建的全国首个基于E2E技术的数字化临床研究一体化平台,将临床诊疗与临床研究工作流程互相融合,实现数据自动化录入,能够全面提升临床科研与研究的质量与效能,实现研究规范与效率跨越式发展。
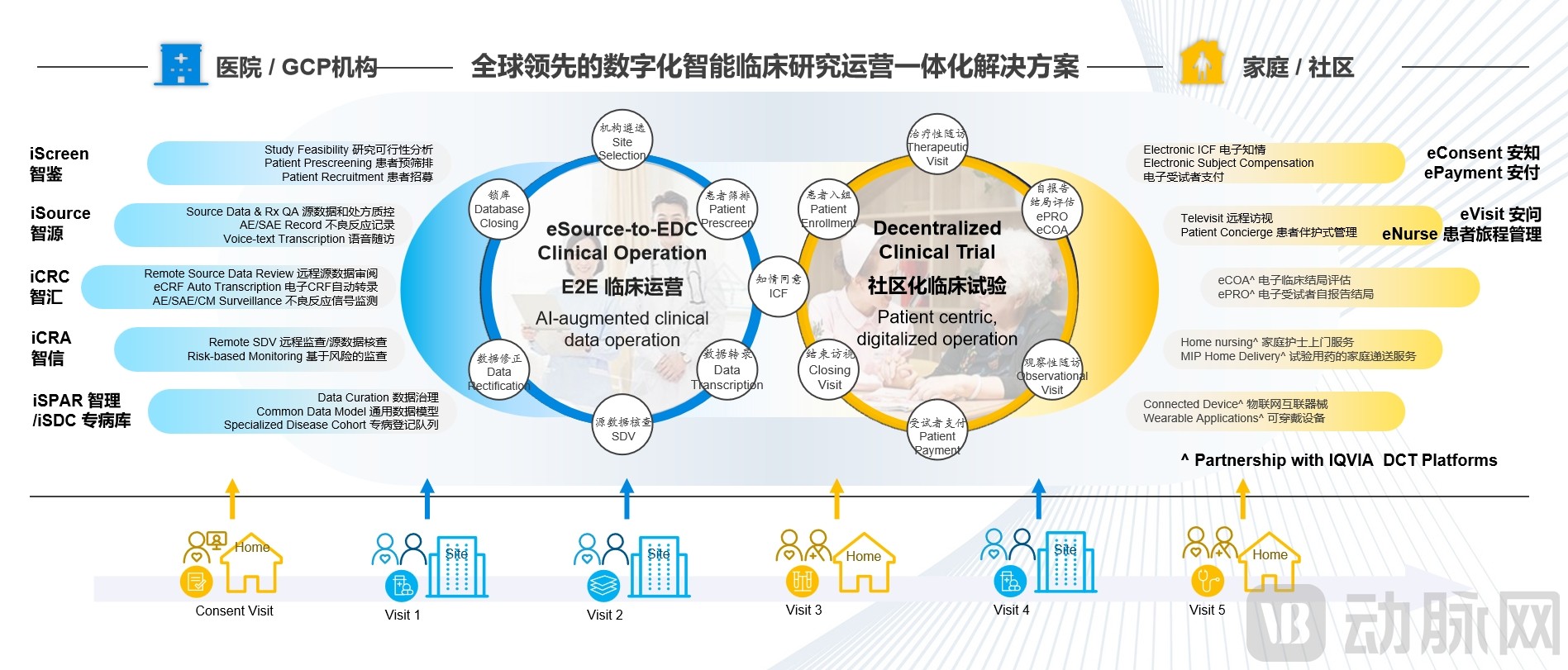
璞睿的数字化智能临床研究一体化解决方案
当前,中国临床CRO市场规模约为1500亿到1800亿,约60%~70%的研发成本耗费在患者招募、临床研究数据录入、数据监查阶段,而其中约2/3的现场数据录入与监查工作可完成基于数字化与智能化技术的自动化替代。
璞睿的解决方案正是瞄准临床研究运营阶段60% ~70%的成本优化市场空间,包括患者招募与筛选匹配、临床研究数据录入、数据监查等阶段,潜在市场潜力将近1000亿。
其中,在患者招募环节,璞睿的iScreen(智鉴)智能受试者招募系统可对受试者相关信息关联规则进行挖掘,即对不同来源的受试者信息与临床试验方案纳入/排除标准进行识别和匹配,既能提高招募效率,还可以优化研究运营成本。
目前,该技术已得到了落地与验证。据悉,在一项由某创新生物医药企业发起的心血管领域疾病临床三期研究中,与璞睿合作的浙江某三甲医院启动后近一年,仍未能实现受试者入组。经与研究团队沟通后,璞睿发现其研究入组条件之一为近期发生过急性发作,而该疾病的急性发作常为一过性,因此无法在院内就诊中及时捕捉。在采用璞睿iScreen智能患者招募模式后,该企业在数据不出院保护患者隐私的前提下,实现了0到1的入组突破;且纳排设置完成后,可根据数据更新自动筛选符合纳排的患者并通知研究团队。
在临床研究数据录入阶段,E2E 模式的端到端直连可消除数据复制和转录中的错误,使研究者更及时地审阅到临床来源的 EMR源数据。不仅如此,通过iCRC(智汇)和iCRA(智信)系统,临床协调员(CRC)/临床监查员 (CRA) 还能够实现远程操作和协助,能有效节约试验成本、提升试验效率。
在数据监查阶段,E2E平台亦改变了传统的监管模式,将传统的高度依赖CRC和CRA的单一的事后监管方式,转变为事前和事中再到事后的监管全流程过程管理。
通过这一解决方案,璞睿希望达到的目标是减少70%的CRC及CRA的人力成本,降低45%的临研总花销,并实现提速30%,真正意义上实现临床研究关键环节的提质增效。
降低50%研发成本,缩短30%试验时长,打造E2E的中国模式
自成立以来,短短3年时间,璞睿推动了数智化临床研究解决方案的建立和不断完善,更实现了多条业务线的商业化,在收入和合同方面都取得了较大进展。截至目前,璞睿已经与超过50多家国内领先的三甲医院GCP机构达成合作,近30家医院完成部署;计划于未来三年覆盖全国顶尖GCP三甲医院300余家。
多家顶级医院和国际药企的认可,不仅显示了璞睿在市场中的领先地位,更突显了其快速的市场拓展能力。据统计,在中国创新药临床研究的E2E细分领域,璞睿的市场占有率已成功跻身全国三甲行列。
不仅如此,公司还在不断强化与国内外临床研究机构和研究型医院的深入合作,持续优化E2E平台对临床研究整体效能的提升。
多项临床研究案例均表明,E2E可显著加速招募、提高数据质量、缩短时间和节省成本。比如,璞睿E2E系统在浙江某三甲医院分别进行了2项试点。其中一项多中心4期单臂非介入研究,旨在研究药物在心衰治疗过程中的安全性和耐受性;另一项多中心3期研究,旨在研究接受机械血栓栓塞切除术后患者安全性研究。
在2个试点项目中,璞睿iScreen(智鉴)筛选设置约5天,现场筛选约2小时,受试者招募时间缩短50%;璞睿iCRC(智汇)将日常工作时间缩短三分之一,成本降低30%~34%;璞睿iCRA(智信)将常规工作时间缩短超过二分之一,成本降低49%~58%;两个项目平均节约成本达到50%。
在企业合作方面,璞睿也全方位开展了各类项目试点,不断推动其商业化进程。目前璞睿在E2E平台的应用与合作方面位于国内领先水平,将不断引领中国临床研究向全新的数字化、自动化、智能化模式升级。
 主要合作客户及业务伙伴图谱
主要合作客户及业务伙伴图谱
中国已成为新药研究领域的重要力量,是全球最具潜力的生物制药市场之一。未来,随着AI技术更快更深地向新药研发的价值链环节渗透,临床试验去中心化将成为未来的重要趋势,E2E技术的应用将越来越广泛,为新药研发带来无限可能。
在中国率先领先推广和应用E2E模式,璞睿有着自己独特的优势。随着越来越多的中国药企向研发创新药转型,加大海外市场布局,提升中国药企的国际竞争力成为核心关键。一方面,璞睿与IQVIA的深度战略合作,为其在中国推广E2E模式奠定了深厚的产业资源和技术优势。更重要的是,璞睿的E2E系统为中国临床研究的数据和规范性提供了很好的背书,不仅能实现更快的临床研究速度和更好的成本效益,更能够更好地对接和融入全球临床研究合作网络和创新体系。
在这一进程中,临床研究的数智化转型同样也需要与政策和技术的发展同步,包括进一步明晰监管政策、制定全流程应用规范、不断优化AI和大语言模型(LLM)算法等,以确保临床试验的数智化转型既符合监管要求,又能充分利用技术优势推动新药研发的创新和效率提升。
未来,期待更多像璞睿这样的企业,不断打破AI等新技术与临床研究融合的边界,引领高效、科学、可靠的E2E中国模式,为新药研发带来无限可能。





























