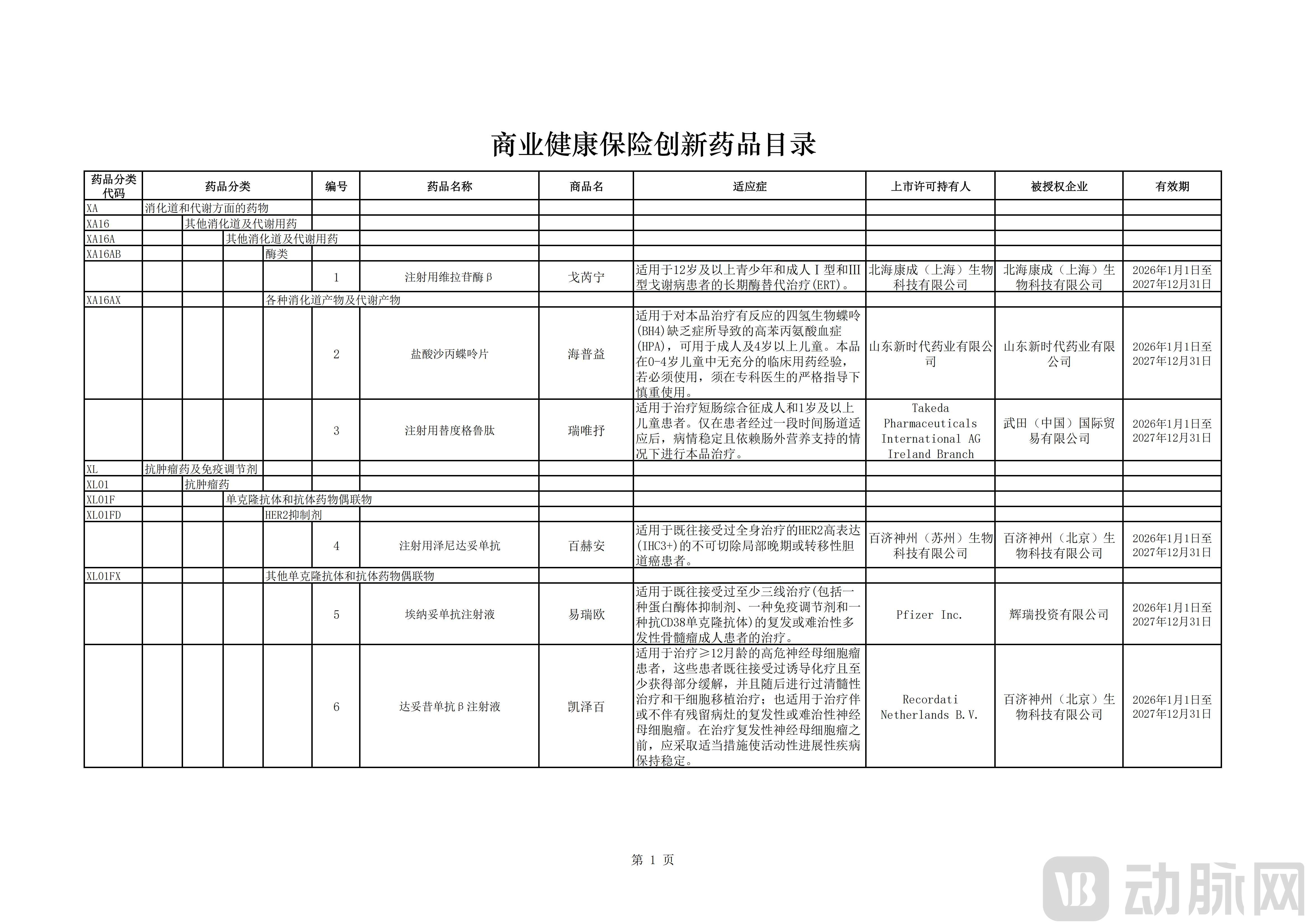
12月7日,2025创新药高质量发展大会在广州召开,2025年《国家基本医疗保险、生育保险和工伤保险药品目录》(以下简称“国家医保药品目录”)和2025年《商业健康保险创新药品目录》(以下简称“商保创新药目录”)在会上发布。 2025年国家医保药品目录成功新增114种药品,有50种是1类创新药,总体成功率88%,较2024年的76%明显提高。调整后,国家医保药品目录内药品总数增至3253种,其中西药1857种、中成药1396种,肿瘤、慢性病、精神疾病、罕见病、儿童用药等重点领域的保障水平得到进一步提升。 商保创新药目录则填补了基本医保保障之外的空白,重点纳入临床价值大、创新程度高、患者受益明显,但超出基本医保保障范围的药品。 此次发布的商保目录堪称一份“前沿疗法清单”,最终有18家创新药企业的19个药品成功纳入,其中包括9个1类新药。CAR-T细胞疗法、单抗类、小分子靶向药等在列,此前通过专家评审的5款百万元级别的CAR-T细胞治疗产品也被纳入商保创新药目录。 然而,目录落地仅是第一步,如何建立可持续的支付机制成为下一道现实考题。业内专家对动脉网指出,创新药支付的核心矛盾在于“一次性支付”与“长期健康获益”的定价悖论。支付方难以在药品上市初期,仅凭有限数据就为患者未来数十年的健康收益“预付”全款。以CAR-T疗法为例,其单针治疗费用超过百万元,即便有保险覆盖,仍对支付体系形成巨大的短期财务冲击。 《商业健康保险创新药品目录》(2025年)
5款百万级CAR-T疗法中选
此次商保创新药目录体现了三大特点:一是导向鲜明,力挺医药科技前沿成果,收录了CAR-T疗法、TCE疗法、双特异性抗体等全球热点药物;二是关注重点群体,既涵盖应对阿尔茨海默病的药物以应对老龄化挑战,也纳入戈谢病、神经母细胞瘤等儿童罕见病用药;三是清晰界定基本医保与商业保险的保障边界。基本医保坚持“保基本”的定位,主要保障安全可靠、疗效确切、靶点机理相对成熟的药品;商业健康保险则更侧重于保障创新前沿、价格相对较高的药物,满足患者对尖端治疗的可及性。
从治疗领域看,这些药品覆盖肿瘤、罕见病、神经退行性疾病及代谢类疾病多个关键领域。
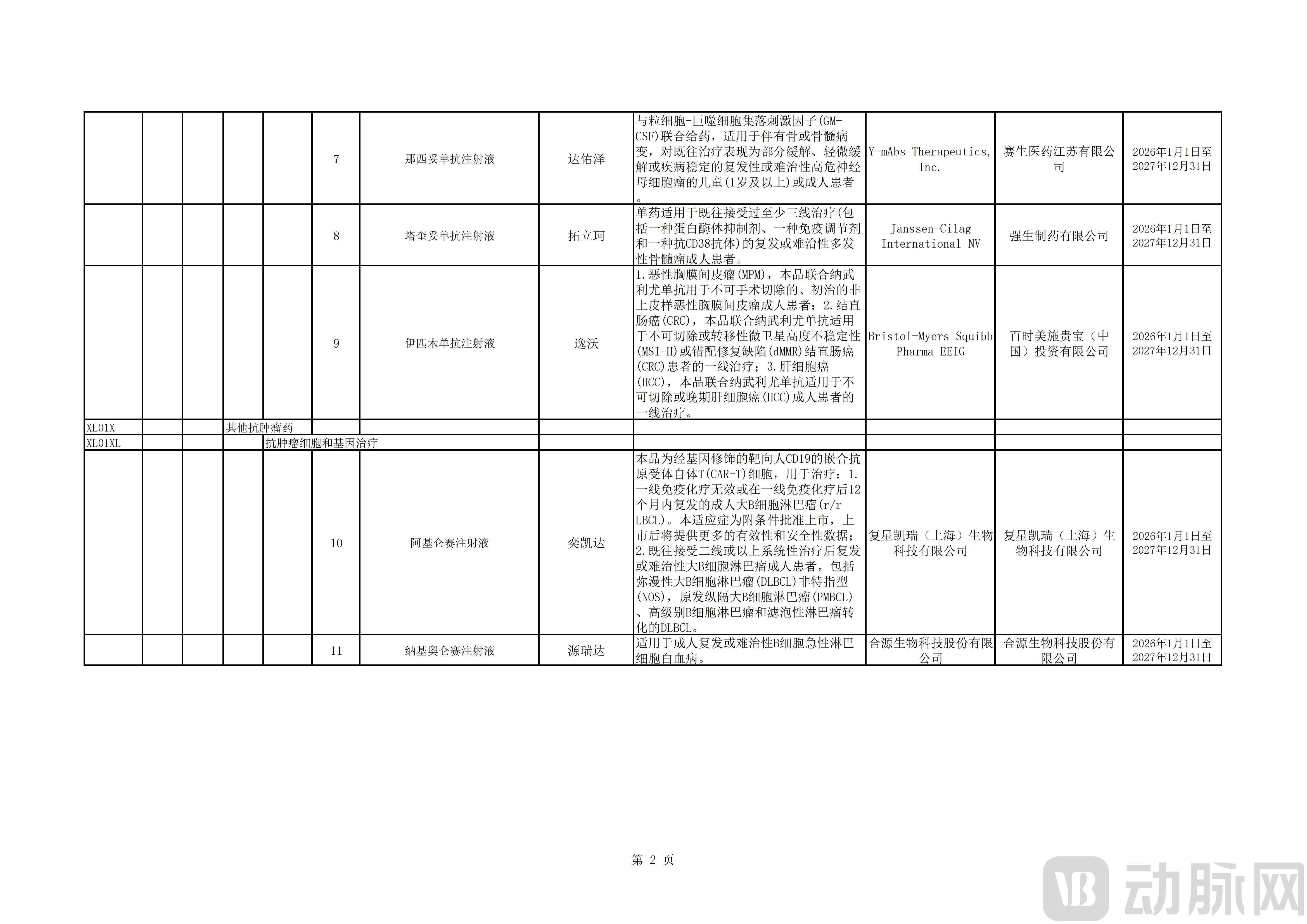
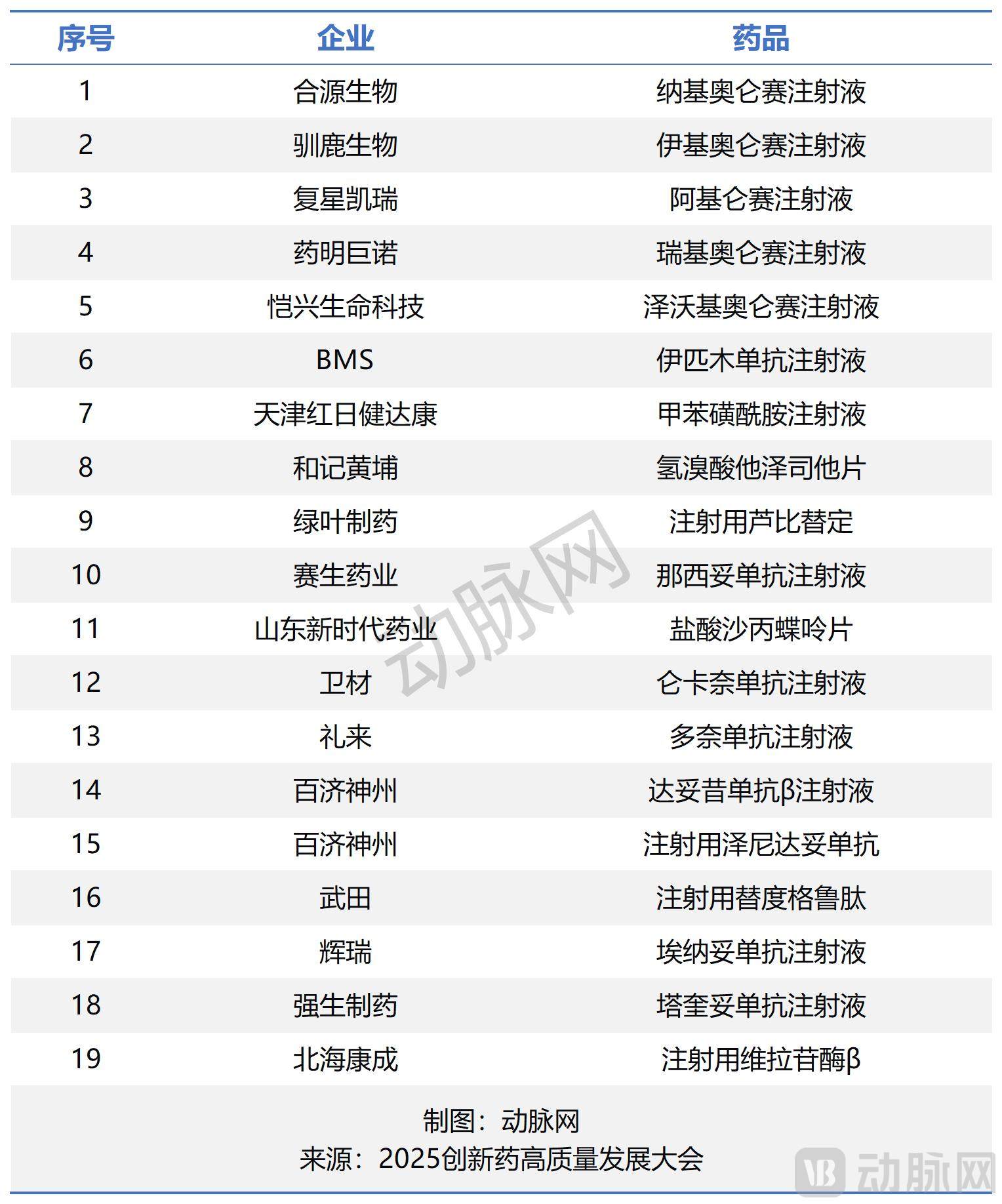
具体入选药品里,此前通过专家评审的5款CAR-T细胞治疗产品集体入围,包括合源生物的纳基奥仑赛注射液、驯鹿生物的伊基奥仑赛注射液、复星凯瑞的阿基仑赛注射液、药明巨诺的瑞基奥仑赛注射液、恺兴生命科技的泽沃基奥仑赛注射液。
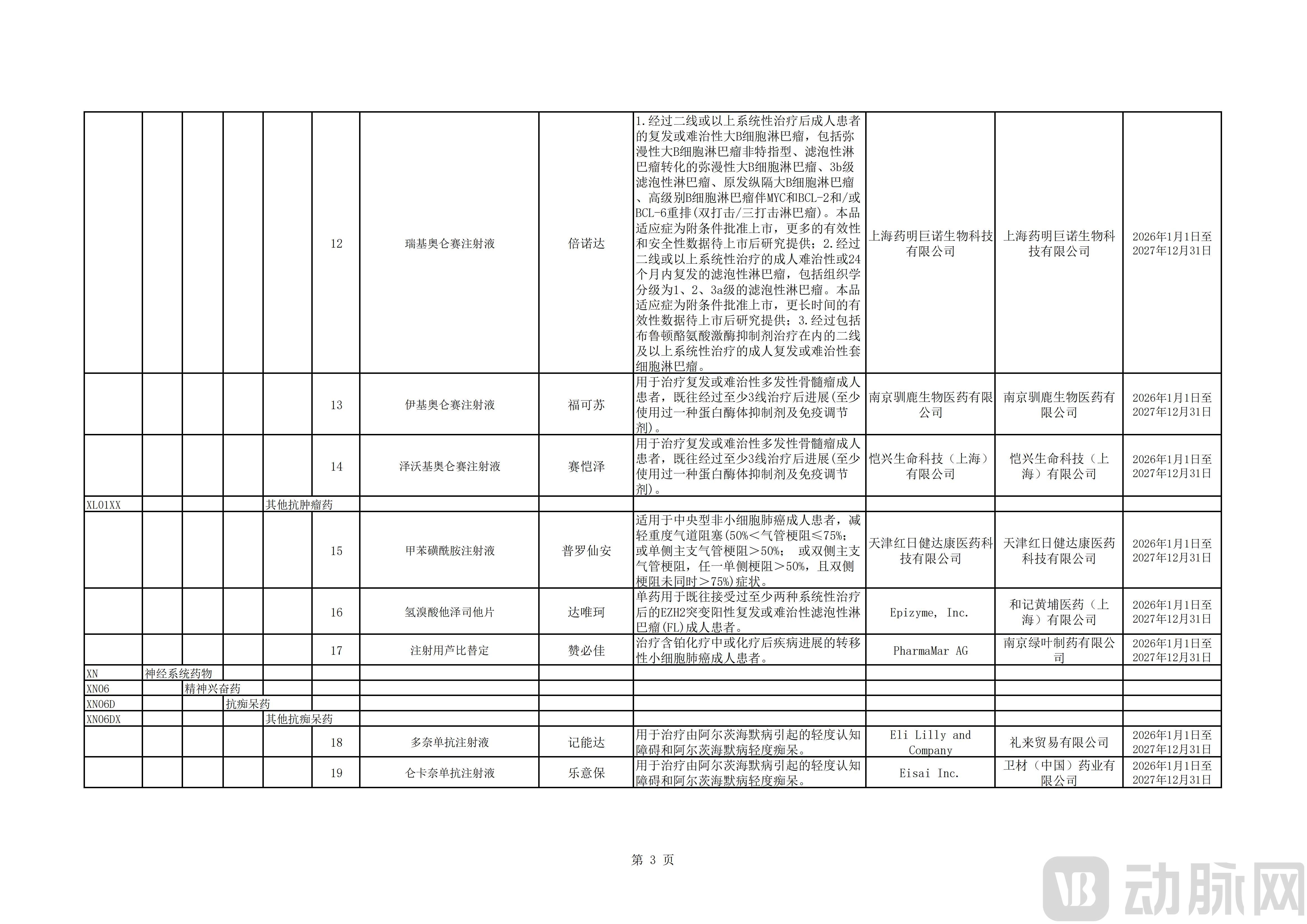
被纳入目录的另外14款创新药分别为:BMS的伊匹木单抗注射液、天津红日健达康的甲苯磺酰胺注射液、和记黄埔的氢溴酸他泽司他片、绿叶制药的注射用芦比替定、赛生药业的那西妥单抗注射液、山东新时代药业的盐酸沙丙蝶呤片、卫材的仑卡奈单抗注射液、礼来的多奈单抗注射液、百济神州的达妥昔单抗β注射液与注射用泽尼达妥单抗、武田的注射用替度格鲁肽、辉瑞的埃纳妥单抗注射液、强生制药的塔奎妥单抗注射液、北海康成的注射用维拉苷酶β。
其中,武田的注射用替度格鲁肽用于治疗短肠综合征,常见于新生儿先天性肠道畸形或术后患者。北海康成的注射用维拉苷酶β用于治疗Ⅰ型戈谢病。新时代药业的盐酸沙丙蝶呤片适用于苯丙酮尿症中对四氢生物蝶呤有反应的患者,这类遗传代谢病若不及时干预可导致智力发育迟缓。
在儿童肿瘤领域,赛生药业的那西妥单抗注射液与百济神州的达妥昔单抗β注射液均用于治疗神经母细胞瘤。
值得注意的是,商保创新药目录纳入了两款阿尔兹海默症治疗药物,分别是礼来的多奈单抗和卫材的仑卡奈单抗。
礼来制药有限公司中国总裁兼总经理德赫兰在发布会上发言时指出,近年来,中国已成为跨国企业的核心战略市场,创新药获批和报销速度持续加快,全球企业也不断拓展在华研发、生产与临床试验布局。2024年中国临床试验数量增长近10%,2025年初外商投资额已达485亿美元,较2020年增长8%。
德赫兰透露:“未来三年,我们计划在中国上市超过20个新产品及新适应症,重点聚焦医疗需求迫切、市场准入壁垒较高的领域。我们的目标是实现全球同步上市,让中国患者‘零时差’受益于创新成果。”
一位药品入选商保创新药目录的企业代表表示:“创新药的质量不仅来自于药品本身,还来自于患者能否真正用得上。如果说2016年建立的药品国家谈判机制是中国创新药可及性道路上的一个极其重要的里程碑,那么商保创新药目录的发布,无疑是另一个值得纪念的里程碑。这标志着我国多层次医疗保障体系建设迈出了关键一步,为更多前沿、高价值的创新疗法提供了新的支付路径。”
创新药支付改革如何迈好下一步?
诚然,商保目录问世是创新药支付改革的又一里程碑,但具体实践的规模与模式还有待各方探索。
一位前CDE资深专家对动脉网指出,创新药支付核心难题最明显的便是高值疗法对支付体系的短期“冲击波”。无论是基本医保还是商业健康保险,其年度支出预算通常基于长期、稳定的历史数据精算得出。当单价达数十万乃至百万元的创新药集中进入临床应用时,会对支付池形成显著的短期“冲击波”,直接考验着整个支付体系的财务稳定性和可持续性。
广东医保局在会上披露了一个数据:2025年3月,广州市率先开展创新药械纳入商业健康保险保障试点,推出6款“穗新保”系列商保产品,覆盖省市创新药械目录产品超过40种。预计至年底累计投保可超2万人次,累计保费超1000万元。
对于这一保费体量,一位资深保险从业者认为,这与业内此前的预期相近。当大量高值创新药械被纳入保障范围,而保险公司的相应控费能力尚在建设时,采取审慎的定价策略是必然选择。
从CAR-T药物与商业保险的合作先例来看,上海“沪惠保”已连续4年将复星凯瑞的阿基仑赛注射液(市场定价约120万元/针)纳入特药保障目录,参保患者在符合适应症条件下可获得最高50万元的药品费用报销。过去3年,已有80多例淋巴瘤患者通过“沪惠保”获得阿基仑赛注射液治疗理赔,累计赔付金额超过4000万元。
另根据业内流传的消息,此次纳入商保目录的药品,经过协商后最终确定的折扣幅度在15%至50%之间。具体折扣比例根据各产品的特性而定,由专家评审确定,不同产品享有差异化的价格优惠。
在讨论支付端创新的同时,药企国际化面临的现实挑战也被摆上台面。
香港科研制药联合高级执行董事陈素娟在发言时直言,内地药企出海存在多重痛点。
例如,处于临床研究阶段的药品是否拥有国际多中心试验数据?药品是否已获得国际监管机构的审批甚至上市?内地药厂普遍采用的GMP标准,与国际及香港认可的PIC/S GMP标准(国际药品检查合作计划药品生产质量管理规范)存在差异。此外,企业也常常不确定其产品能否通过目标市场的卫生技术评估(HTA),而这正是国际市场准入与定价的关键参考。
与此同时,陈素娟透露,规划中的香港药械监管中心有望在2030年前全面运行,届时所有创新药物都有望在香港进行第一层审批。“如果香港的监管中心是国际水平的话,将会进一步协助国内机构出海国际市场。”
有证券从业者从资本市场的角度分析指出,在研发端,存在重复投资、同质化竞争,热门靶点“扎堆”开发;在国际化方面,部分企业面临跨国交易时,对方期待看到更多基于国际多中心临床数据而不仅限于中国的证据;在资本市场,头部企业融资能力强劲,但部分中小公司仍随市场波动面临融资困境。
但行业潜力已可从数据中刊出,目前中国创新药的研发管线正从“快速跟随”(fast follow)迈向“同类最优”(best in class)甚至“同类首创”(first in class)。
前述证券从业者分享最新数据,前三季度中国企业已完成103笔对外授权交易,总金额高达903亿美元,较2023年同比增长77%。多笔交易的首付款已超过10亿美元,步入全球前列。中国已成为美国之后,跨国药企第二大项目交易来源地。
业界坚信中国本土市场有能力孕育出销售额超数十亿乃至百亿的“重磅炸弹”级创新药。这要求企业彻底转向源头创新,同时也需要支付端优化评估体系,对真正具有临床突破价值的产品给予充分的价值认可与价格保护,从而缩短回报周期,吸引“耐心资本”长期投入。
那么,如何鼓励“重磅产品”,甚至托举本土大药诞生?
今年发布的商保目录,堪称破解支付困境的“破题之举”。业界期待,“基本医保保基本、商保促创新”的多层次支付格局尽快成熟,让创新药在上市初期能通过商保探索价值定价,再通过医保谈判实现广泛可及,从而形成良性的价格与价值实现路径。
中国创新药企的研发效率具备国际竞争力,但持续出海竞争需要巨额的研发投入。
一个稳定、可预期的国内利润基本盘,是企业出海闯荡的“压舱石”和“加油站”。这一基本盘并非依靠政策保护获得,而需凭借企业自身实力实现,通过科学的集采与医保谈判规则、保护创新药的合理利润以及建设多元化支付体系,能让优秀企业在国内市场获得滋养。
详细清单: