2026年伊始,Evaluate最新报告指出,今年有望获FDA批准的十款创新疗法,涵盖代谢疾病、肿瘤、自身免疫等多个领域。它们不仅是科学进步的缩影,更预示着未来几年治疗范式的转变。
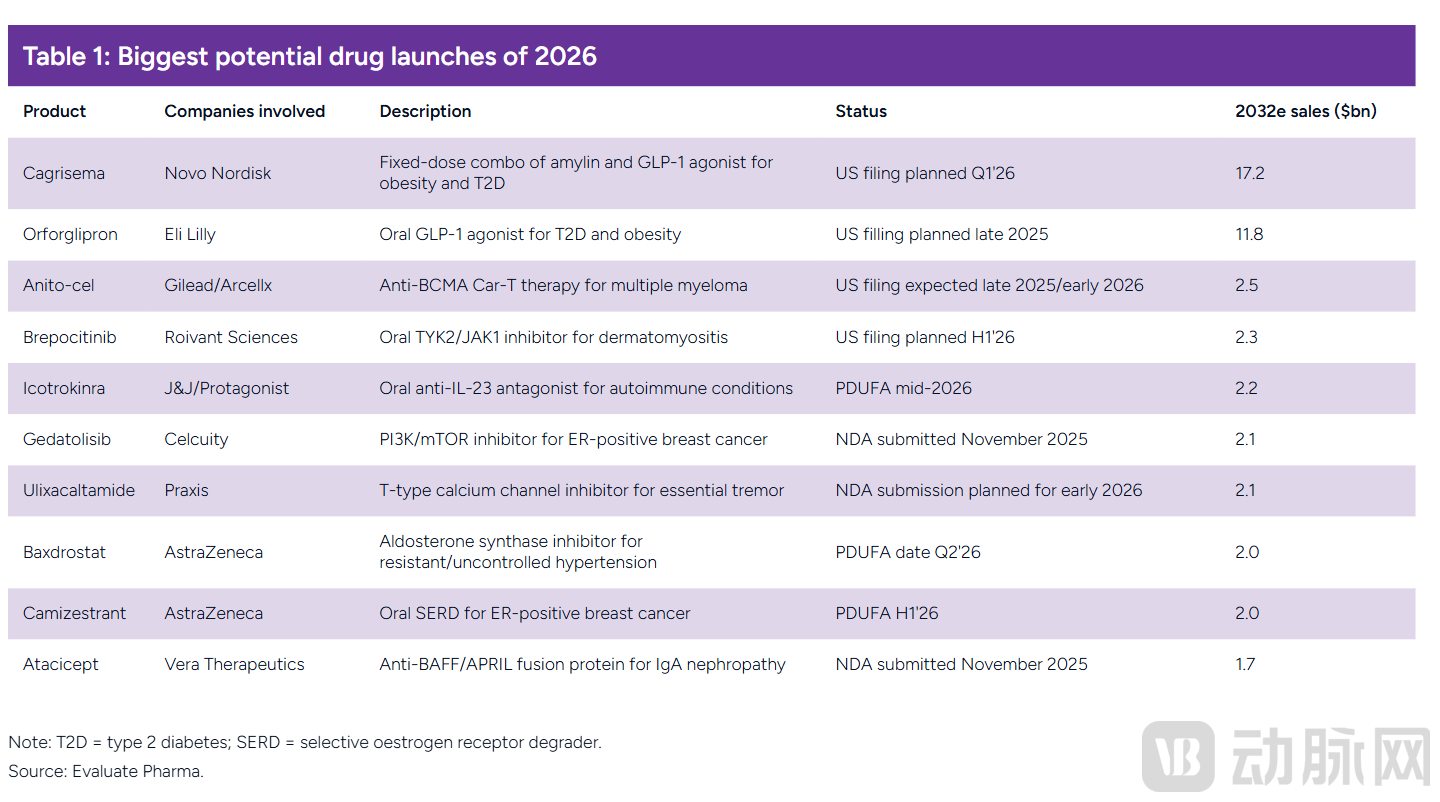
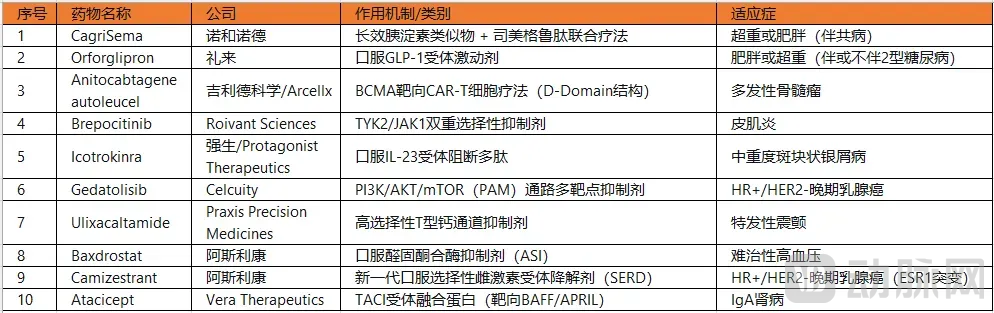
2026年最大潜力待上市药物(图源:Evaluate)
01
代谢疾病赛道“双雄争霸”,GLP-1之外的新故事
在代谢疾病治疗领域,尤其是肥胖症治疗市场,诺和诺德与礼来两大巨头的竞争一直备受瞩目。2026 年,随着诺和诺德的 CagriSema 与礼来的 Orforglipron 新药申请递交,这一领域的竞争态势愈发激烈,有望重塑肥胖治疗格局。
CagriSema 是一款由长效胰淀素类似物 cagrilintide(2.4 mg)和司美格鲁肽(2.4 mg)组成的固定剂量联合疗法,设计为每周一次皮下注射。胰淀素与 GLP-1 均为人体在进食后由肠道分泌的激素,二者具有协同作用机制。胰淀素能够减缓胃排空速度,抑制胰高血糖素分泌,从而降低餐后血糖波动,同时还能作用于中枢神经系统,增加饱腹感;司美格鲁肽作为 GLP-1 受体激动剂,可刺激胰岛素分泌,抑制食欲,减少食物摄入。CagriSema 将二者结合,旨在通过多种途径更有效地调节代谢,实现减重效果。
礼来的 Orforglipron 则是一种在研、每日一次的小分子口服胰高血糖素样肽 - 1(GLP-1)受体激动剂 ,可在一天中的任何时间服用,不受进食和饮水限制。它通过与 GLP-1 受体结合,激活下游信号通路,发挥与天然 GLP-1 类似的生理作用,如促进胰岛素分泌、抑制胰高血糖素释放、延缓胃排空等,进而达到控制血糖和减轻体重的目的。小分子结构使其在口服吸收方面具有天然优势,无需像多肽类药物那样面临诸多递送难题。
给药方式上,CagriSema 的每周一次皮下注射,对于部分患者来说可能存在注射不便、恐惧针头的问题;而 Orforglipron 每日一次的口服给药方式,无疑大大提高了患者的依从性,更符合现代患者对于便捷治疗的需求 。
临床数据方面,CagriSema 的 NDA 主要基于两项 3 期临床试验 REDEFINE 1 与 REDEFINE 2 的结果。其中 REDEFINE 1 试验结果显示,在不论患者是否持续用药的情况下,CagriSema 组在第 68 周实现了 20.4% 的体重下降,而安慰剂组为 3.0%,差异具有统计学显著性。而在假设所有患者均持续用药的情况下,CagriSema 组在第 68 周的体重下降幅度为 22.7%,安慰剂组为 2.3%。此外,CagriSema 组有 91.9% 的受试者体重下降幅度达到或超过 5%,而安慰剂组为 31.5%。
Orforglipron 去年 8 月公布的 3 期临床试验 ATTAIN-2 的结果显示,针对肥胖或超重并伴有 2 型糖尿病的成年人,orforglipron 的三种剂量均达到了主要和所有关键次要终点。在为期 72 周的治疗中,药物带来了显著的体重下降、糖化血红蛋白水平有意义的降低,并改善了心脏代谢风险因素。12 月公布的 3 期临床试验 ATTAIN-MAINTAIN 的积极顶线结果显示,orforglipron 在维持体重减轻方面也达到临床试验的主要和关键次要终点。
从减重幅度来看,CagriSema 在最佳假设下的体重下降幅度略高于Orforglipron公布的结果,但 Orforglipron 在血糖控制和心脏代谢风险因素改善方面也表现出色,且其口服给药的便利性可能会吸引更多患者。
这两款药物代表了肥胖治疗领域的两大趋势:联合疗法与口服 GLP-1 激动剂。联合疗法通过整合多种作用机制,有望提供更全面、更有效的治疗效果;而口服 GLP-1 激动剂则解决了传统注射剂型的依从性问题。随着这两款药物在 2026 年有望获批上市,肥胖治疗市场将迎来新的竞争格局,患者也将有更多、更优质的治疗选择。这不仅会推动肥胖治疗领域的发展,也可能对整个代谢疾病治疗市场产生深远影响,促使更多药企加大在该领域的研发投入,探索更多创新疗法。
02
细胞疗法再进化:BCMA CAR-T如何突破实体瘤困局?
细胞疗法作为癌症治疗领域的新兴力量,近年来取得了显著进展,尤其是嵌合抗原受体 T 细胞(CAR-T)疗法,在血液系统恶性肿瘤的治疗中展现出令人瞩目的疗效。然而,如何将 CAR-T 疗法的成功拓展至实体瘤领域,一直是科研人员和临床医生面临的重大挑战。2026 年,吉利德科学 / Arcellx 联合开发的 Anitocabtagene autoleucel(anito-cel)有望为这一困境带来新的突破方向。
Anitocabtagene autoleucel 是一款靶向 B 细胞成熟抗原(BCMA)的 CAR-T 细胞疗法 ,其独特之处在于采用了 Arcellx 开发的创新紧凑结合结构域 ——D-Domain。传统的 CAR-T 细胞疗法在治疗过程中,常面临严重免疫毒性和 CAR 表达不稳定等问题。
D-Domain 的设计则有效改善了这些状况,它体积小且稳定,能够在不产生持续信号传导的情况下实现较高的 CAR 表达。这一特性使得 CAR-T 细胞在识别和清除肿瘤细胞时,既能够保持高效的活性,又能避免过度激活免疫系统导致的严重毒性反应 。同时,D-Domain 被设计为可快速从 BCMA 靶点解离,进一步降低了免疫相关不良反应的发生风险,在保障安全性的同时,实现对多发性骨髓瘤细胞的有效清除。
在多发性骨髓瘤治疗中,Anitocabtagene autoleucel 已展现出优异的疗效。去年 12 月美国血液学会年会上公布的关键性 2 期临床试验 iMMagine-1 数据显示,中位随访时间为 15.9 个月时,接受 anito-cel 治疗的复发 / 难治性 MM 患者的总缓解率为 96%,完全缓解 / 严格完全缓解率为 74%。患者 24 个月无进展生存率为 61.7%,24 个月总生存率为 83.0% 。这些数据表明,Anitocabtagene autoleucel 为多发性骨髓瘤患者提供了一种高效且持久的治疗选择,显著改善了患者的生存预后。
从 CAR-T 在多发性骨髓瘤治疗的进阶路径来看,从最初的探索性应用到如今不断优化升级,每一次技术革新都带来了更好的治疗效果和安全性。以第一代 CAR-T 为基础,逐步发展出引入共刺激结构域的第二代 CAR-T,增强了 T 细胞的活性和持久性 ;而后第三代 CAR-T 进一步增加共刺激结构域,以期望实现更强大的免疫激活 。而 Anitocabtagene autoleucel 的出现,则代表了从结构设计层面进行创新,通过 D-Domain 解决了传统 CAR-T 面临的关键问题,推动 CAR-T 疗法在多发性骨髓瘤治疗中迈向新的高度。
对于未来向实体瘤拓展的可能性,Anitocabtagene autoleucel 的成功为其他实体瘤 CAR-T 疗法的研发提供了宝贵经验。实体瘤由于其复杂的肿瘤微环境、异质性以及缺乏特异性肿瘤抗原等问题,一直是 CAR-T 治疗的难点。但 D-Domain 所展现出的优势,如高表达、低免疫毒性、快速解离等特性,或许可以通过合理的靶点选择和结构优化,应用于实体瘤的治疗中 。
例如,针对某些实体瘤特异性抗原,设计基于 D-Domain 的 CAR-T 细胞,有望突破肿瘤微环境的抑制,实现对实体瘤细胞的有效杀伤 。尽管 CAR-T 疗法向实体瘤领域拓展仍面临诸多科学挑战,包括 CAR-T 细胞的实体瘤组织浸润效率提升、肿瘤微环境中免疫抑制信号的解除等关键问题,但 Anitocabtagene autoleucel 的研发与临床应用,为该领域的突破提供了新的研究思路与技术借鉴。
03
自身免疫疾病:从“抑制炎症”到“精准阻断”
自身免疫性疾病系免疫系统识别异常致自身组织损伤的慢性进展性难治性疾病,传统治疗以糖皮质激素等非特异性免疫抑制剂为主,虽能缓解炎症,但因缺乏靶向性,易削弱正常免疫功能并引发多种不良反应。
自身免疫性疾病发病机制研究证实,特异性细胞因子异常及信号通路紊乱为核心驱动因素,这一认知推动治疗研发从广谱抑制转向精准靶向。2026年有望获批的Brepocitinib与Icotrokinra,为该领域精准治疗策略优化提供关键支撑,代表前沿发展方向。
Brepocitinib为选择性TYK2/JAK1双重抑制剂。TYK2与JAK1是细胞因子信号转导关键节点,介导I型干扰素、IL-6、IL-12/23等促炎细胞因子传导,后者为自身免疫病核心驱动因素,可诱发免疫异常激活及自身组织损伤。Brepocitinib通过特异性抑制TYK2/JAK1活性,精准阻断致病性信号通路,避免广泛抑制正常免疫功能,实现增效减毒。
2024年9月公布的VALOR关键性Ⅲ期临床试验数据显示,Brepocitinib治疗皮肌炎(DM)患者达到预设主要终点及关键次要终点。主要终点分析结果表明,治疗第52周时,Brepocitinib组患者平均总改善评分(Total Improvement Score,TIS)为46.5,显著高于安慰剂组的31.2(p=0.0006),提示该药物可显著改善皮肌炎患者的临床症状,进而提升患者生存质量。亚组分析显示,Brepocitinib组停用背景激素治疗的患者比例接近安慰剂组的2倍,表明其可降低患者对糖皮质激素等传统药物的依赖程度,进一步减少长期激素治疗相关的不良反应风险,为皮肌炎患者提供了更优的治疗选择。
Icotrokinra是一款潜在first-in-class口服靶向多肽,其核心作用机制为特异性阻断白细胞介素-23受体(IL-23R)。IL-23作为自身免疫性疾病病理微环境中的关键促炎因子,在中度至重度斑块状银屑病等疾病的致病性T细胞活化过程中发挥不可或缺的调控作用,是介导此类疾病慢性炎症反应的核心分子。
Icotrokinra通过与IL-23R特异性结合,竞争性阻断IL-23与受体的相互作用,从而抑制下游炎症信号通路的激活,从源头遏制病理性炎症反应的启动与进展。该精准靶向IL-23R的作用模式,可实现对银屑病等相关自身免疫性疾病的特异性治疗,避免对机体正常免疫功能的非特异性干扰。
强生(Johnson&Johnson)与Protagonist Therapeutics联合开展的临床研究证实了Icotrokinra的治疗效能,该药物在4项针对银屑病的Ⅲ期临床试验中均达到主要终点及共同主要终点。2025年4月公布的ICONIC-LEAD关键性Ⅲ期临床试验顶线数据显示,每日一次口服Icotrokinra可显著改善中度至重度斑块状银屑病患者的皮肤病变,且安全性良好。
治疗第16周时,Icotrokinra组65%的患者达到研究者总体评估(IGA)0/1分(皮肤症状清除或几乎清除),50%的患者实现银屑病面积与严重程度指数(PASI)90改善(即症状改善≥90%),而安慰剂组上述指标达标率分别仅为8%和4%;治疗第24周时,患者缓解率进一步提升,74%的患者达到IGA 0/1分,其中46%达到IGA 0分(皮肤症状完全清除),65%的患者达到PASI 90改善,40%实现PASI 100改善(症状完全缓解)。上述临床数据充分验证了Icotrokinra治疗银屑病的有效性与安全性,为中度至重度斑块状银屑病患者提供了新的治疗选择。
除治疗效能外,Brepocitinib与Icotrokinra的给药方式对提升患者治疗依从性具有重要临床意义。自身免疫性疾病多呈慢性进展性病程,需长期维持治疗,患者的治疗依从性直接影响临床结局。传统治疗药物中,注射剂型及高频给药方案易增加患者治疗负担,导致依从性下降,进而影响治疗效果。
Brepocitinib与Icotrokinra均采用口服给药方式,其中Icotrokinra为每日一次给药,简化了治疗方案,降低了患者用药难度。口服给药模式可避免注射相关的创伤与不适感,便于患者居家自行用药,在提升治疗便利性的同时,可显著改善长期治疗患者的依从性,保障治疗方案的规范实施,进而优化患者生存质量,促进患者回归正常社会生活。
Brepocitinib与Icotrokinra的研发与临床应用,标志着自身免疫性疾病治疗领域从广谱炎症抑制向精准机制阻断的重要突破。二者通过精准靶向疾病关键信号通路,在临床疗效上展现出显著优势,同时口服给药模式进一步提升了患者治疗依从性,具有重要的临床应用价值。若2026年顺利获批上市,将为自身免疫性疾病患者提供更高效、安全且便捷的治疗选择,推动自身免疫性疾病治疗领域的诊疗范式革新与学科发展。
04
乳腺癌治疗进入“联合时代”,PAM通路能否成为破局关键?
HR+/HER2-晚期乳腺癌占乳腺癌患者70%,依赖内分泌治疗但耐药问题突出,严重限制患者预后。传统治疗以他莫昔芬等内分泌单药为主,30%-40%患者原发耐药,初始有效者5-12个月易继发耐药;耐药后治疗选择有限,化疗毒副作用大,严重影响生活质量。
PAM通路在HR+/HER2-晚期乳腺癌发生、发展及耐药中起关键作用。正常细胞中该通路调控生长、增殖等生理过程,而超半数患者存在通路相关基因变异(如AKT1激活突变、PTEN缺失/突变),导致通路失控,既促进肿瘤进展,又诱发内分泌治疗耐药。
Gedatolisib为在研多靶点PAM抑制剂,可强效靶向全部I类PI3K亚型及mTORC1/2,实现通路全面阻断。与单靶点抑制剂易引发交叉激活、抑制效果有限不同,其全面抑制可减少适应性交叉激活,充分阻断通路,恢复肿瘤细胞对治疗的敏感性。
Celcuity 公司在相关研究中展示了 Gedatolisib 的卓越疗效。去年 11 月,该公司宣布已完成向美国 FDA 递交 gedatolisib 的 NDA,拟用于治疗 HR 阳性、HER2 阴性的晚期乳腺癌患者。NDA 的递交主要基于 3 期 VIKTORIA-1 临床试验中 PIK3CA 野生型患者队列的研究结果。该试验旨在评估 gedatolisib 组合在接受过 CDK4/6 抑制剂及芳香化酶抑制剂治疗后疾病进展的 HR 阳性、HER2 阴性晚期乳腺癌患者中的疗效与安全性 。
针对 PIK3CA 野生型亚群分析的结果显示,与活性对照药物相比,gedatolisib、palbociclib、fulvestrant 三联方案使疾病进展或死亡风险降低 76%,中位无进展生存期(PFS)达到 9.3 个月,而对照组仅为 2.0 个月,延长了 7.3 个月(HR=0.24,95% CI:0.17-0.35,p<0.0001);客观缓解率为 31.5%,中位缓解持续时间(DOR)为 17.5 个月。这些数据充分表明,Gedatolisib 与其他药物的联合使用,能够显著改善 HR+/HER2 - 晚期乳腺癌耐药患者的治疗效果,延长患者的无进展生存期。
除了 Gedatolisib,新一代口服选择性雌激素受体降解剂(SERD)Camizestrant 也为 HR+/HER2 - 晚期乳腺癌的治疗带来了新的希望。Camizestrant 是阿斯利康公司研发的一款新型药物,它不仅能够阻断雌激素受体(ER)的信号传导,还能进一步诱导 ER 降解,从根本上切断乳腺癌细胞的生长信号。与传统的内分泌治疗药物相比,Camizestrant 在分子结构上进行了优化,显著增强了对突变 ER 的降解能力 ,尤其对于存在 ESR1 突变的患者具有更好的疗效 。在 HR+/HER2 - 晚期乳腺癌患者中,ESR1 突变是导致内分泌治疗耐药的重要原因之一,约 30% 的晚期患者存在 ESR1 突变。
阿斯利康公司开展的多项临床试验证实了 Camizestrant 的疗效 。在 2 期 SERENA-2 研究中,Camizestrant 组患者的 PFS 较氟维司群组显著延长(7.2 vs 3.7 个月,HR=0.59) 。更为关键的是,在 ESR1 突变亚组中,Camizestrant 组患者实现了更加显著的 PFS 获益(6.3 vs 2.2 个月,HR=0.33) 。去年 6 月公布的 3 期临床试验 SERENA-6 的分析显示,camizestrant 与 CDK4/6 抑制剂(palbociclib、ribociclib 或 abemaciclib)联用,在无进展生存期方面实现了高度具有统计学意义且临床意义显著的改善 。
SERENA-6 试验评估了在一线治疗中,对于携带 ESR1 突变的 HR 阳性、HER2 阴性晚期乳腺癌患者,从标准治疗方案芳香化酶抑制剂联合 CDK4/6 抑制剂,转换至 camizestrant 联合方案的疗效与安全性 。研究结果显示,相较于标准治疗方案,camizestrant 联合方案将疾病进展或死亡风险降低了 56%(HR=0.44;95% CI:0.31–0.60;p<0.00001) 。转换至 camizestrant 联合治疗患者的无进展生存期为 16.0 个月,而对照组为 9.2 个月。值得一提的是,无论所用 CDK4/6 抑制剂类型如何,在临床相关的各个亚组中,均观察到一致的 PFS 获益。
Gedatolisib 和 Camizestrant 的出现,标志着 HR+/HER2 - 晚期乳腺癌治疗从单靶点向多通路联合治疗的重要转变 。这种联合治疗模式不再局限于单一的作用机制,而是通过同时作用于多个关键靶点和信号通路,协同发挥抗肿瘤作用 。一方面,Gedatolisib 对 PAM 通路的全面抑制,能够有效克服因通路异常激活导致的耐药问题,恢复肿瘤细胞对治疗的敏感性;另一方面,Camizestrant 对雌激素受体的阻断和降解,从根源上抑制肿瘤细胞的生长 。二者联合,从不同角度对肿瘤细胞进行攻击,为 HR+/HER2 - 晚期乳腺癌患者提供了更全面、更有效的治疗策略。
对于耐药患者而言,这种多通路联合治疗模式具有重大的突破价值。在过去,耐药后的 HR+/HER2 - 晚期乳腺癌患者治疗选择极为有限,预后往往较差。而现在,Gedatolisib 和 Camizestrant 的联合应用,为这些患者开辟了新的治疗途径 。通过基因检测等手段,筛选出存在 PAM 通路异常和 ESR1 突变的患者,针对性地给予联合治疗方案,能够显著延长患者的无进展生存期,提高患者的生活质量。同时,这种联合治疗模式也为未来乳腺癌治疗的发展提供了新的思路和方向,促使更多药企加大在多通路联合治疗领域的研发投入,推动乳腺癌治疗技术的不断进步。
05
高血压、震颤、IgA 肾病…… 那些被忽视的 “小众战场”
生物医药领域中,部分发病率较低或症状不显著的小众疾病,虽易被忽视,但给患者带来严重痛苦,治疗需求长期未满足。2026年多款针对此类疾病的创新疗法有望获批,既为患者带来希望,也体现了药企在高未满足需求领域的布局与探索。高血压为全球常见疾病,WHO 2025年数据显示全球患者达14亿。其中难控制高血压(经两种及以上降压药治疗后血压仍升高)是临床难题,长期患病显著增加心梗、中风、肾衰风险;传统降压药虽种类多,但仍有大量患者血压控制不佳。
阿斯利康的 Baxdrostat 为这部分患者带来了新的治疗选择 。它是一款每日一次的高选择性、口服醛固酮合酶抑制剂(ASI),有望成为 “first-in-class” 疗法 。其作用机制是通过特异性抑制醛固酮合成酶,该酶负责肾上腺中醛固酮的合成 。醛固酮是一种通过促进钠和水的保留来增加血压的激素 ,约 25% 的高血压源于 “醛固酮” 水平失调 。Baxdrostat 通过阻断醛固酮的生成,减少钠和水的潴留,从而降低血压。
在 3 期临床试验 BaxHTN 中,纳入了 796 名患有不受控制的高血压(2 种不同类别的最大耐受抗高血压药物,其中至少 1 种为利尿剂)或难治性高血压(≥3 种不同类别的最大耐受抗高血压药物,其中至少 1 种为利尿剂)的成年人 。研究受试者按 1:1:1 的比例随机分配,在现有标准治疗的基础上,每日一次服用 baxdrostat 2mg、baxdrostat 1mg 或安慰剂 。主要终点是第 12 周时坐位收缩压相对于起始的平均变化差异 。
结果显示,与安慰剂组相比,两种剂量的 baxdrostat 在第 12 周均显示出统计学上显著且具有临床意义的平均收缩压降低 。与安慰剂组相比,baxdrostat 组还观察到次要疗效终点的改善,包括难治性高血压亚群的坐位收缩压、坐位舒张压以及坐位收缩压低于 130mmHg 。试验中,baxdrostat 的总体耐受性良好。
此外,11 月 11 日公布的 Bax24 3 期试验的阳性完整结果显示,与安慰剂相比,baxdrostat 在 12 周时使 24 小时平均收缩压(SBP)实现具有统计学和临床意义的显著降低 。难治性高血压(rHTN)患者在标准治疗的基础上接受 baxdrostat 2mg 或安慰剂治疗,疗效在 24 小时的周期内均有体现,包括高血压患者心血管事件风险较高的清晨时段 。
Baxdrostat 在多个关键次要终点上也显示出具有统计学和临床意义的显著降低,包括夜间动态平均收缩压(安慰剂校正后降低 13.9 mmHg)和坐位收缩压(安慰剂校正后降低 10.3 mmHg) 。接受 Baxdrostat 治疗的患者(71%)24 小时平均收缩压<130mmHg 的比例显著高于接受安慰剂治疗的患者(17%) 。这些数据充分证明了 Baxdrostat 凭借其长效半衰期和对醛固酮合成酶的高度选择性抑制,可显著改善难治性高血压患者 24 小时血压和夜间血压。
特发性震颤是最常见的运动障碍,其特征是上肢不自主的节律性运动,伴或不伴头部、声带或腿部等其他身体部位的震颤 。这些震颤严重扰乱日常生活,且呈进展性,通常在病程中震颤严重程度和幅度不断增加 。在美国,β 受体阻滞剂普萘洛尔是唯一获批用于治疗特发性震颤的药物,但疗效有限,耐受性差,并且禁用于影响相当一部分特发性震颤患者的合并症 。其他 β 受体阻滞剂和抗惊厥药也属于非适应症用药,但同样疗效和耐受性有限。
Ulixacaltamide为高选择性T型钙通道小分子抑制剂,通过阻断小脑-丘脑-皮层(CTC)环路异常神经元放电缓解震颤。其疗效与安全性获Essential3三期项目验证,该项目含两项同步试验:研究1(1:1随机双盲安慰剂对照,12周疗程)显示,Ulixacaltamide组第8周mADL11评分改善(-4.3 vs 安慰剂-1.7,P<0.0001)及各关键次要终点均具统计学意义;研究2(随机停药试验)显示,Ulixacaltamide组疗效维持率(55%)显著高于安慰剂组(33%,P=0.037)。药物耐受性良好,常见不良事件为便秘、头晕等,无死亡或药物相关严重不良事件。
IgA肾病是以肾小球系膜区IgA沉积为特征的原发性肾小球肾炎(又称IgA肾炎、Berger病),发病机制复杂,临床表现为反复血尿、蛋白尿,可进展为慢性肾衰。其为全球最常见原发性肾小球疾病,中国占比30%-40%,高发于20-40岁青壮年;亚洲人群患病率及进展速度均高于欧美,国内现有约500万患者、年新增超10万。该病早期无症状、进展隐匿,20%-40%患者确诊后20年内进展至终末期肾病,需透析或肾移植维持生命。
目前,IgA 肾病的治疗主要以控制血压、减少蛋白尿、延缓肾功能进展为主,常用的药物包括血管紧张素转换酶抑制剂(ACEI)、血管紧张素 Ⅱ 受体拮抗剂(ARB)、糖皮质激素 、免疫抑制剂等 。然而,这些传统治疗方法在实际应用中存在一些不足之处 。例如,糖皮质激素虽然在一定程度上可以减轻炎症反应,但长期使用可能会带来诸多副作用,如骨质疏松、血糖升高、感染风险增加等 。此外,对于一些病情较重或对传统治疗反应不佳的患者,缺乏更有效的治疗手段 。传统治疗方法往往只能缓解症状,难以从根本上阻止疾病的进展。
Atacicept 为 IgA 肾病患者带来了新的希望 。它是一种重组融合蛋白,含有可溶性跨膜激活剂和钙调亲环素配体相互作用因子(TACI)受体,可以与 B 细胞活化因子(BAFF)和增殖诱导配体(APRIL)结合 。这些细胞因子是肿瘤坏死因子家族的成员,可促进与某些自身免疫性疾病(包括 IgA 肾病和狼疮性肾炎)相关的 B 细胞存活和自身抗体产生。Vera 公司认为 atacicept 通过靶向 B 细胞和浆细胞以减少自身抗体,可能成为潜在 “best-in-class” 药物 。
今年 1 月,Vera 公司宣布美国 FDA 已受理其为 atacicept 递交用于治疗成人 IgA 肾病的生物制品许可申请,并授予优先审评资格 。这一申请主要基于 ORIGIN 3 研究预设的期中分析数据 。结果显示,atacicept 在第 36 周显著降低患者蛋白尿水平,治疗组 24 小时尿蛋白 / 肌酐比值(UPCR)较基线下降 46%,并较安慰剂组实现具有统计学意义和临床意义的 42% 下降(p<0.0001)。与此同时,atacicept 在整个 ORIGIN 项目中的安全性表现良好,总体上与安慰剂组相当。
Baxdrostat、Ulixacaltamide 和 Atacicept 分别针对高血压、特发性震颤和 IgA 肾病这几种高未满足需求的疾病,展现出了良好的临床疗效和安全性。这些药物的研发成功,不仅为患者提供了新的治疗选择,改善了他们的生活质量,也体现了制药企业对小众疾病领域的关注和投入 。从社会价值角度来看,这些创新疗法的出现有助于减轻患者家庭和社会的医疗负担,提高患者的生活自理能力和社会参与度。同时,它们也为生物医药领域的发展注入了新的活力,激励更多企业在小众疾病治疗领域开展创新研究,推动整个行业不断进步。
06
结尾
综观上述十款疗法,其共同特征体现为靶点机制深化、给药策略优化及临床应答率提升,标志着生物医药研发正从“泛化抑制”迈向“精准调控”新阶段。这些潜在获批疗法不仅拓展了关键适应症的治疗边界,更折射出创新药研发范式向患者为中心、数据驱动决策的系统性转变。未来,其长期安全性、可及性与真实世界效力的验证,将成为评估临床价值与产业影响的关键维度。2026年或将成为检验这一转型成果的重要观察窗口。
参考来源:Evaluate;公开资料整理




























