2025年,T细胞衔接器(TCE)赛道持续升温,作为下一代免疫治疗的核心方向,其凭借“现货可及、机制独特”的优势,逐步重构肿瘤与自免疾病治疗格局。据弗若斯特沙利文数据,全球TCE市场规模已从2024年的30亿美元稳步攀升,预计2034年将突破1101亿美元。本年度,血液瘤管线商业化持续深化,实体瘤管线实现关键突破,三特异性TCE崭露头角,国内Biotech出海成果显著。
在这一轮快速演进中,不同管线之间的分化也愈发清晰——有的已完成临床与商业化验证,有的持续获得资本与跨国药企押注,还有的则在尝试打开实体瘤与自免等新边界。
基于这一分化趋势,本文不再简单罗列项目进展,而是从“临床确定性—产业押注方向—技术与适应症边界”三个维度出发,梳理2026年值得期待的10条TCE管线,以更结构化的方式呈现赛道的真实演进路径。
2025年商业化提速,边界持续突破
在具体展开之前,我们先从年度层面看一看:2025年,正在发生哪些变化?
2025年,TCE赛道整体呈现出“商业化加速、技术迭代、靶点多元、边界外延”的核心特征,清晰勾勒出行业发展全貌,也成为本次管线盘点的核心背景。
首先,实体瘤正式成为研发主战场,临床可行性得到实质性验证。随着Tarlatamab在小细胞肺癌的商业化落地,CLDN18.2、EGFR、CDH6等实体瘤靶点快速升温,多款管线进入Ⅱ期确证性临床;“2+1”结构、遮蔽肽等创新设计落地应用,有效缓解脱靶毒性、肿瘤穿透不足等关键瓶颈,推动TCE从血液瘤向实体瘤加速渗透。
其次,技术路径迭代成熟,用药体验与成药性双提升。TriTAC、DART等工程化平台应用愈发广泛,三特异性TCE开始进入临床验证阶段,如维立志博LBL-051等产品已体现出多靶点协同的潜力。同时,围绕半衰期延长与给药方式优化,白蛋白结合域、Fc融合及皮下给药逐渐成为标配,TCE从“可用”走向“更好用”。
第三,国内企业全球话语权提升,出海成价值释放核心路径。2025年,多款国产TCE管线通过海外授权进入全球视野,GR1803、LBL-051等代表性项目持续达成大额交易,推动行业逐步形成“国内研发+全球商业化”的新分工模式,国际药企对中国创新的认可度明显提升。
第四,赛道竞争分化加剧,临床数据成为核心评判标准。血液瘤领域BCMA、CD19等成熟靶点竞争拥挤,GPRC5D等新靶点成为差异化突破口;实体瘤研发聚焦未满足临床需求,CRS发生率、脱靶毒性等安全性指标成为核心门槛,临床数据质量逐步取代概念叙事,成为估值与合作的关键依据。
第五,TCE的适应症边界正在向自身免疫疾病延伸。2025年,以CC312(CD19/CD28/CD3)为代表的三特异性TCE,已进入系统性红斑狼疮(SLE)等适应症的早期临床探索;同时,CM336(CLDN18.2/CD3)在实体瘤之外,也开始尝试自身免疫性溶血性贫血(AIHA)等非肿瘤场景。TCE通过“深度清除致病B细胞”的机制,开始展现出区别于传统免疫抑制剂的潜力,自免领域正成为新的增长方向。
十大管线分层盘点
如果说2025年是TCE从“技术可行性”走向“临床验证”的关键一年,那么站在2026年的门槛回看,行业关注的焦点已经发生变化:不再只是“有没有效果”,而是哪些路径已经被验证成立,哪些方向正在积累新的确定性。
基于开篇提到的三个维度,当前TCE管线大致可以归入三类:一类是已完成临床验证并形成清晰路径的成熟项目;一类是持续获得资本与MNC押注、预期正在形成的方向;另一类则处于技术或适应症边界的探索阶段。
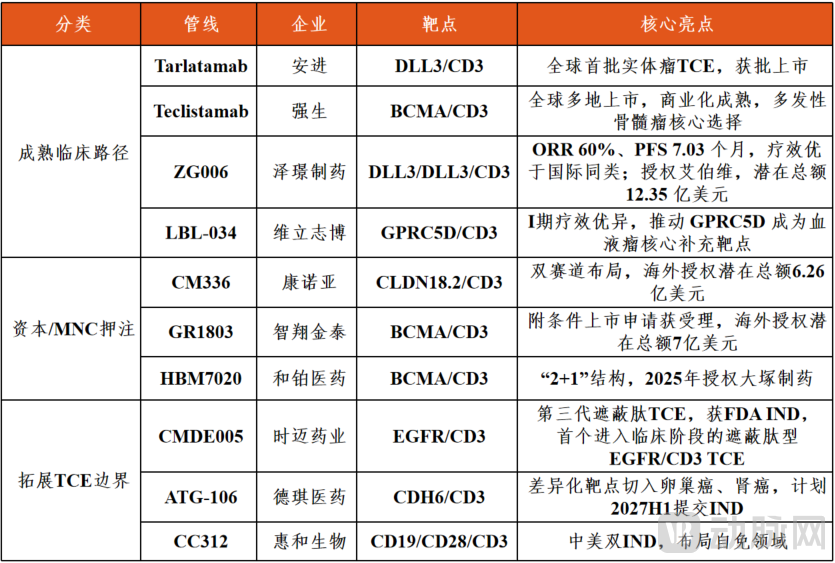
TCE赛道10条代表性管线盘点
1成熟临床路径的TCE管线:赛道基本盘正在成型
在TCE赛道中,真正稀缺的并不是概念,而是能够被反复验证的临床路径。这类管线或已获批上市,或具备明确、扎实的临床数据,形成了临床价值与商业化路径清晰的赛道“基本盘”。
需要指出的是,部分已获批上市的TCE药物同样处在商业化与适应症拓展的关键阶段,在2026年依然具备高度期待价值。其市场放量速度、治疗线数前移以及更多肿瘤类型的探索,仍具有重要观察价值,是判断TCE技术成熟度与产业化潜力的重要坐标。
Tarlatamab(安进,DLL3/CD3)是这一类别中最具标志性的存在。作为全球首批获批上市的实体瘤TCE之一,其意义并不仅在于单一适应症的成功,而在于证明了实体瘤场景下TCE可以在安全性可控的前提下实现真实疗效。其基于BiTE(双特异性T细胞衔接器)设计,通过桥接DLL3与CD3,将T细胞重定向至肿瘤细胞并触发杀伤反应,为难治性小细胞肺癌提供了新的治疗路径。随着更多治疗线数与适应症的探索推进,其商业化潜力仍在持续释放。商业化层面,Tarlatamab表现亮眼,2025年实现全年销售额6.27亿美元,季度销售额保持环比高增长;伴随适应症前移与市场渗透率提升,产品有望在2026年进一步放量,成为实体瘤TCE领域的商业化标杆。
血液瘤领域,Teclistamab(强生,BCMA/CD3)是TCE治疗模式的成熟标杆,2026年其临床与商业化价值将持续释放。作为全球首款获批的BCMA/CD3双抗,该药已在全球多国上市,2024年6月获NMPA批准用于多发性骨髓瘤后线治疗,凭借皮下给药、疗效确切、安全性可控的优势,成为复发/难治患者的重要治疗选择。
2026年3月,该药迎来关键突破,FDA批准其联合Darzalex Faspro 用于多发性骨髓瘤二线治疗,成为该领域二线潜在新标准,治疗线数前移大幅打开临床与商业化空间。依托强生成熟的商业化体系,叠加前线治疗的广阔市场空间,Teclistamab 2026年的市场放量表现值得重点期待。
值得注意的是,ZG006(泽璟制药,DLL3/DLL3/CD3)与LBL-034(维立志博,GPRC5D/CD3)代表了国产TCE管线中临床推进较快、且持续有数据读出的典型项目。
其中,ZG006的创新三抗结构进一步提升肿瘤靶向特异性、降低脱靶毒性,核心布局广泛期小细胞肺癌这一高未满足临床需求领域,目前处于Ⅱ期临床阶段。其在三线小细胞肺癌临床中展现出同类最佳潜力,客观缓解率(ORR)达60%,无进展生存期(PFS)7.03个月,优于安进已上市Tarlatamab。2025年12月,泽璟制药将ZG006海外独家开发与商业化权益授权给艾伯维,潜在交易总金额达12.35亿美元。
LBL-034在复发/难治性多发性骨髓瘤(R/R MM)Ⅰ期临床中,50余例患者全剂量段均表现出良好的安全性与有效性,高剂量疗效媲美CAR-T,伴髓外瘤患者疗效显著且MRD阴性率高于标准治疗,目前已完成Ⅱ期临床首例给药,其在BCMA耐药人群中的表现,让GPRC5D逐步成为BCMA之后血液瘤的重要补充靶点。
2正在被资本与MNC押注的TCE管线:预期正在形成
与“成熟临床路径”的管线不同,这一类热门TCE管线的关注度,更多来自交易、合作与平台层面的信号。
CM336(康诺亚,BCMA/CD3)是这一类别中最具代表性的管线之一。其一方面切入骨髓瘤这一血液瘤大适应症;另一方面探索自身免疫性溶血性贫血(AIHA)等非肿瘤领域,体现出TCE在不同免疫场景下的可塑性:2025年6月,其治疗难治性自身免疫性溶血性贫血(AIHA)的突破性案例荣登《新英格兰医学杂志》(NEJM)。商业化层面,康诺亚已于2024年11月将该管线大中华区以外权益授权给Platina Medicines,潜在总金额达6.26亿美元。
GR1803(智翔金泰,BCMA/CD3)GR1803治疗R/R MM的Ⅰ期临床中,57例可评估患者ORR达89.5%,RP2D(Ⅱ期推荐剂量组)队列患者ORR87.5%、≥VGPR占70.8%,凭借优异的疗效与安全性已提交附条件上市申请并获NMPA受理。2025年5月该管线授权Cullinan获超7亿美元潜在总额,大额出海印证了其临床价值与分子设计的科学性。
HBM7020(和铂医药,BCMA/CD3)更体现出资本对平台型技术的集中下注逻辑。HBM7020基于全人源HBICE®双抗技术与Harbour Mice®平台开发,核心布局多发性骨髓瘤,依托结构创新具备自免领域拓展潜力。通过非对称“2+1”结构(双BCMA结合位点+单价CD3)优化传统TCE的安全性痛点,目前处于临床前阶段。2025年,该管线与大塚制药达成全球战略合作,授权大中华区以外开发及商业化权益,成为平台技术获国际MNC认可的典型案例。
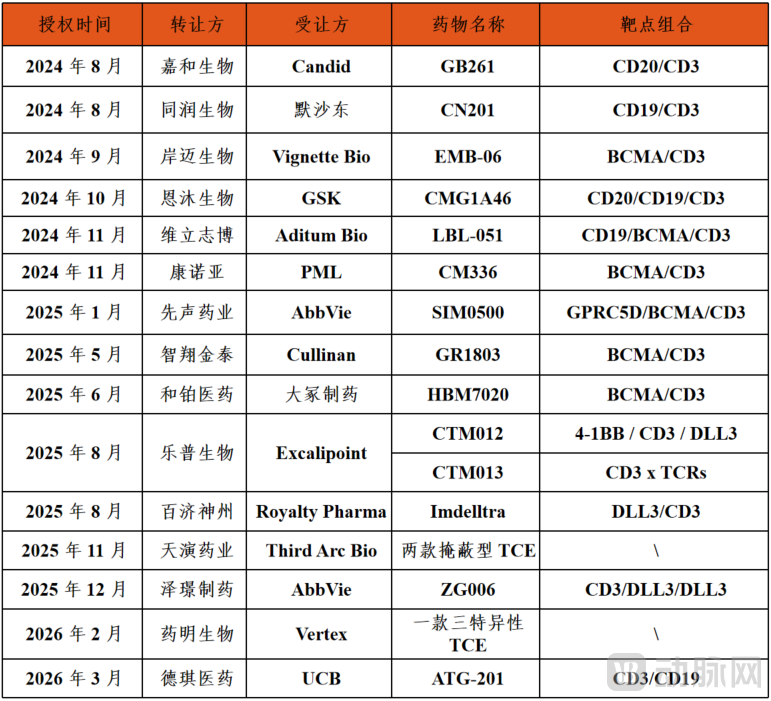
主要TCE管线出海交易一览
3正在拓展TCE边界的探索型管线:方向尚未收敛
第三类值得关注的TCE管线,未必拥有最靠前的临床进度,但其价值在于尝试解决TCE现阶段的难题及拓展适应症边界。
CMDE005(时迈药业,EGFR/CD3)基于Pro-BiTE遮蔽肽酶控激活平台开发,属于第三代EGFR/CD3 TCE,通过肿瘤微环境特异性激活机制降低脱靶毒性,直击实体瘤TCE安全性核心痛点。2025年4月,CMDE005获FDA IND批准,成为全球前二、中国首个进入临床阶段的遮蔽肽型EGFR/CD3 TCE。其I期临床显示良好耐受性与剂量依赖性免疫激活特征,其平台价值与国际化潜力已成为资本与MNC对实体瘤TCE下一代技术押注的重要标的。
ATG-106(德琪医药,CDH6/CD3)是全球首款进入临床前研究阶段的CDH6×CD3 TCE,选择差异化靶点切入卵巢癌、肾癌等领域,避开了BCMA、CD19等成熟靶点的红海竞争,其临床前数据已验证了TCE在CDH6靶点实体瘤中的适用性,公司计划于2027年上半年提交IND申请。
而CC312(惠和生物,CD19/CD28/CD3)将TCE明确引入系统性红斑狼疮等自身免疫疾病领域,标志着TCE不再仅仅是肿瘤工具,而可能成为免疫系统重塑的技术选项之一。CC312已实现中美自免适应症双IND获批,其中国内自免适应症已进入临床I期阶段。
赛道成熟度提升,价值判断趋于一致
如果说三类划分展示的是TCE赛道的“结构分层”,那么进一步剖析这10条管线,可以看到当前行业正在形成一套相对清晰的共性逻辑,同时在关键路径上也呈现出明显的分化趋势。
从共性来看,这批管线几乎都围绕“未满足临床需求”展开,靶点选择既体现出集中度(如BCMA、CD3、CLDN18.2),也在不断外延扩展;在技术层面,产品均围绕安全性与给药便利性进行工程化优化,无论是降低CD3亲和力、采用“2+1”结构,还是引入长半衰设计与皮下给药,本质上都在解决TCE从“有效”走向“可长期使用”的问题。与此同时,这些管线大多已获得资本与产业的双重验证。
而在差异层面,分化同样清晰。一方面,技术路线呈现“海外成熟平台主导+国内自主创新突围”的格局,TriTAC、DART等路径已被验证,而国内企业则通过LeadsBody、FIT-Ig及三特异性设计寻找弯道机会。此外,从发展阶段来看,海外管线部分已进入商业化或后期临床,而国内项目多处于Ⅱ期阶段,整体仍处于“追赶+差异化突破”的窗口期。
从血液瘤单点突破,TCE走向多适应症与多机制协同
上述10条管线构成了当前TCE赛道的样本切片,从中可以清晰地看到一个正在成型的方向:TCE正在从单一药物形态,演进为具备工程化能力的治疗平台。
首先,在结构层面,TCE的竞争已从“是否连接成功”转向“如何更精细地调控免疫反应”。多特异性设计正在成为重要方向,三抗甚至多抗不再只是简单叠加靶点,而是通过模块化组合,在疗效与安全性之间寻找更优解;与此同时,条件激活、低亲和力CD3以及“屏蔽”设计等策略的引入,使TCE逐步具备“按需激活”的能力,本质上是从广谱、非选择性的免疫激活工具,升级为可精准调控、按需起效的靶向免疫系统。
其次,在适应症层面,TCE正从血液瘤的成功经验出发,向更复杂的疾病场景延伸。一方面,实体瘤仍是决定行业上限的关键战场,围绕肿瘤微环境、抗原异质性等问题,脑靶向、HLA肽靶向等新策略不断涌现;另一方面,自身免疫疾病的探索正在打开第二增长曲线,通过深度清除致病B细胞,TCE有望在部分疾病中实现类似“功能性治愈”的效果,这一点在当前Top10管线中已初现端倪。
再次,在产业层面,TCE正加速向“平台级资产”演变。跨国药企通过收购与合作快速补齐布局,艾伯维、阿斯利康、默沙东、GSK等持续加码相关资产。与此同时,国内 Biotech 依托自主研发的技术平台,通过对外授权实现价值快速放大,例如和铂医药Harbour Mice®、岸迈生物FIT-Ig®、时迈药业Pro-BiTE等平台均已达成多项海外合作。这种“平台+管线”的组合,使TCE不再只是单个产品竞争,而是进入体系化能力比拼阶段。
2026年正成为TCE赛道进一步演化的重要节点——血液瘤商业化持续深化,实体瘤临床可行性不断得到验证,自免领域的探索也开始逐步展开。技术迭代、临床数据与产业资本在这一过程中逐渐形成更稳定的互动关系,推动赛道进入新的发展阶段。
从这一意义上看,本次盘点的10条管线既是当前赛道阶段性进展的缩影,也构成了2026年值得持续观察的一组关键项目。哪些路径将率先兑现临床与商业价值,值得我们共同期待。




























