12000亿成绩单藏着三个变化
动脉网:从商会监测的数据看,2025年我国医药贸易突破2000亿美元。在这份成绩单背后,您观察到了哪些结构性变化?创新药、高端器械这些品类的出口表现具体怎么样?
张小会:这个2000亿确实很有标志性,中国医药产业告别了过去以原料药和低端耗材为主的“规模扩张”时代,开始进入以创新和高质量为核心的“价值跃升”新阶段。
数据很直观。一是出口市场持续优化。2025年对美进出口额同比均下降约为10%,同时对欧盟、俄罗斯、非洲、拉美等地区和国家出口额均超过10%,逐步摆脱对单一市场的依赖,多元化发展已经有成效。二是产品科技含量不断提升。西药制剂出口同比增长近30%,手术机器人出口同比增长368.1%,核磁共振增长了14.4%等。三是创新药国际化迎来新突破。2025年创新药对外授权交易金额超1300亿美元,在ADC、双抗、GLP-1这些前沿领域,我们跟全球先进水平并跑,甚至有些产品已经开始领跑。
2优势突出、短板明显,这四类企业更适合出海
动脉网:成绩背后,我们也在思考——国际市场上,我国药械出海的核心优势和主要短板是什么?
张小会:综合来看,依托成本控制、质量合规、产业效率、规模配套、创新迭代以及对外开放水平形成的综合竞争优势,我们能够高效整合上下游全产业链资源,强化各环节协同联动,其他单一国家或区域市场很难复制。
具体来说:全产业链配套与规模化制造优势突出,制造成本与研发效率显著优于欧美;创新能力快速提升,近年来我国创新药与创新医疗器械获批数量稳步增长,在研产品规模稳居全球前列;供应链韧性强,出口覆盖欧美及“一带一路”新兴市场,能够有效对冲单一区域波动带来的风险;政策环境持续优化,监管与国际规则逐步接轨为企业出海提供了制度保障。
但短板也很明显:国际化能力相对薄弱,很多企业缺乏成熟的海外注册团队,国际注册与合规运营能力仍显不足;海外商业化与品牌建设能力偏弱,多数企业出海仍以产品贸易或授权合作为主,产品出去了,但卖不动量、卖不上价、站不住品牌。原始创新能力仍需提升,首创新药(FIC)、高端核心技术、关键底层专利等方面容易在国际竞争中面临侵权争议与市场壁垒。地缘政治风险上升,非关税壁垒增多。
动脉网:在这样的竞争格局下,什么样的药械公司更适合走向国际?什么样的企业起步更容易些?
张小会:我们认为更适合走向国际的企业,不在于规模和过往成绩,而在于能否抓住政策机遇,打造供应链韧性,产品持续创新迭代,灵活合规地适应多变市场。
一类是具备全产业链整合能力的龙头,如原料药制剂一体化,能稳定切入欧美市场;二是手握核心技术平台的创新型企业,在前沿靶点、ADC、双抗等领域具有差异化优势,具备全球临床价值与竞争力;三是高性价比的医疗器械龙头,在影像、监护、IVD、外科器械等领域产品兼具性能与成本竞争力,既能打新兴市场也能进欧美中高端;四是细分领域的“隐形冠军”,如在骨科、电生理、微创耗材等垂直赛道形成技术壁垒,出海路径清晰、风险可控。
3体系合规薄弱,本地化门槛重重——如何破局?
动脉网:结合商会和您的实际经验,企业出海在注册认证、合规核查这些环节,目前最突出的卡点是什么?
张小会:根据我们的观察,我总结下来就是“资料不齐、数据不合、体系不严、管理混乱”。
资料完整性与数据合规性。欧美这种规范市场,对注册资料的数据完整性、可溯源性要求严苛。国内企业原始记录缺失、电子数据管理不规范等问题导致申报周期延长。
GMP质量体系合规以及资质管理。国内企业不同程度存在因生产环境监控、无菌保障、追溯体系不合规等问题,导致出海受阻等;部分企业资质证明材料过期、注册证与生产地址不符导致注册被拒或清关受阻等。
互认机制如果进一步推动,将有望加快新兴市场的本土化进程,现在很多新兴市场要求本地化生产,这就面临“四重门”——本地临床、本地伙伴、本地语言、本地生产,每个国家全部做一遍,拉长了准入周期,推高了本地化成本。
动脉网:不同市场表现也有差异。2025年我国对欧盟出口增长10.98%,欧盟的增长动力来自哪里?另外,欧盟MDR升级后,对以CE为参考的其他国家准入有何影响?
张小会:对欧盟出口增长,有几个原因。一是中国高性价比的产品成为欧盟采购的优先项,特别是美国高关税和供应链波动,凸显了我们的优势。二是中国企业合规能力提升,拿到的MDR、CE证书越来越多。三是产品结构升级,PET/CT、手术机器人、监护仪、高值耗材等增幅明显,契合了欧盟需求。
至于MDR升级的影响,得分区域看。
对认可CE(MDR/IVDR)的国家在准入方面是利好的,一次认证管好几个市场,像挪威、冰岛等,直接采纳MDR,无额外壁垒;土耳其医疗器械法规与欧盟高度对齐强制要求MDR;英国正在推进“无限期认可CE标志”的政策,外界普遍认为未来基本可以确定将实现“一次认证,英欧双通”。
将CE(MDR)作为核心参考或简化路径的国家,总体看门槛是提升的。中东、东南亚、拉美部分国家将CE认证作为注册的核心技术文件,对旧版MDD证书的接受度正在下降。
将CE仅作参考、仍需本地注册的国家,总体影响有限。印度、俄罗斯、非洲多数国家,CE认证是一个重要的“加分项”。
不过,CE-IVDD证书不是全面失效,而是有条件延期。D类设备可以延到2027年底,C类延到2028年底,B类及以下延到2029年底;所以企业需要抓紧梳理产品,切勿因延期而松懈。
动脉网:您觉得未来一两年,药械出海最大机遇和最大风险分别是什么?哪些赛道、技术或产品最具备全球竞争力?
张小会:未来两年的最大机遇在于“中国药械创新发展”与“全球医药市场对中国供应链依赖”形成的双重红利。一方面,创新药“技术出海”进入爆发期,License-out升级到2.0阶段,Co-co共同开发、风险共担、收益共享,中国企业开始分享全球商业化利润;另一方面是原料药与高端器械的“结构性替代”;2026-2030年全球将有约3000亿美元品牌药专利到期,利好中国药企承接转移;同时部分高端器械领域凭借高性价比和产业链优势,正在快速填补欧美市场空白。
最大风险则主要是“合规壁垒升级”与“地缘政治博弈外溢影响”的相互叠加。风险不再局限于商业竞争,显性壁垒和隐性壁垒逐渐增多。同时,交易达成由原来的“价格和效率”优先逐渐让位于“安全和可控”,地缘政治与供应链“去风险”影响日渐扩散等。
综合近期出口数据和BD交易情况看,生物药领域的ADC和双抗产品,高端医疗器械领域的内窥镜与影像设备,以及特色原料药与GLP-1等具备较强的竞争力。总之,未来两年手握硬核技术且具备全球合规能力的企业将在竞争中占据有利地位。
动脉网:您受邀作为2026未来医疗医药百强大会·药械国际市场拓展论坛【全球第一课】嘉宾,计划分享什么内容?
张小会:内容还在准备,核心会围绕中国药械出海全景洞察及行动建议的方向。
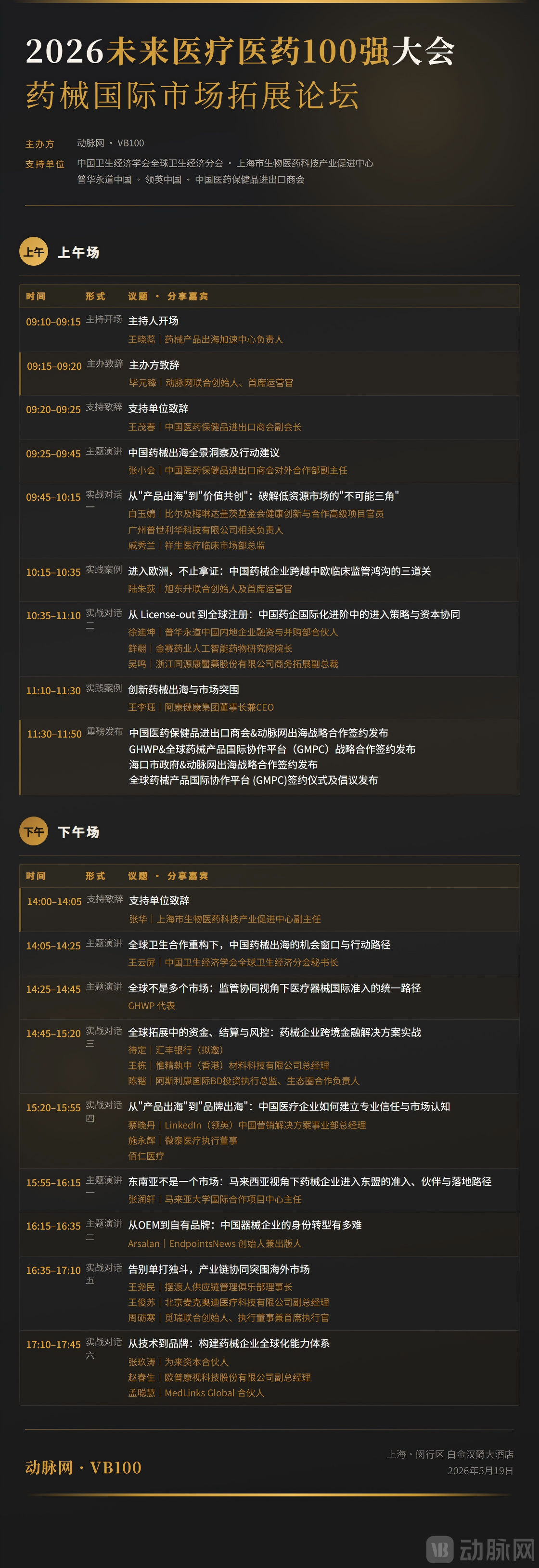
2026未来医疗医药百强大会·药械国际市场拓展论坛将于5月19日在上海重磅开幕,将邀请祥生医疗、欧普康视、微泰医疗、普世利华等具有丰富海外经验的企业分享实战经验,以及渠道流通、准入合规、跨境金融等机构带来赋能思考。
您最关心哪个市场?最想链接什么资源?最想听到什么分享?
论坛正在发起【药械出海需求与论坛话题征集】,诚邀您参与。
参与回报:
● 话题贡献者将获得2026未来医疗医药百强大会·药械国际市场拓展论坛免费门票1张
● 优质话题贡献者将获得动脉网平台供需发布机会1次(出海相关)
会议咨询、商务合作:王女士 17774983530