2022年2月,浙江大学医学院及附属第一医院章京教授课题组和焕一生物战略合作副总裁Robin Chan博士在《Journal of Neuroinflammation》(影响因子:8.322)共同发布了题为"α-Synuclein-containing erythrocytic extracellular vesicles: essential contributors to hyperactivation of monocytes in Parkinson's disease"的文章。该研究针对帕金森病(PD)发病机制的一个重要特性——外周免疫系统相关单核细胞激活水平较高进行了研究,明确了含α-突触核蛋白(α-syn)的红细胞胞外囊泡(RBC-EVs)对帕金森病(PD)患者单核细胞过度激活过程的核心作用。
尽管在200年前人类就发现了帕金森病的特征,但学术界和产业界目前还不完全清楚帕金森病的发病机制,也尚无可治疗的药物。单核细胞过度激活过程的揭示对帕金森发病机制的研究有何意义,针对帕金森病(PD)的治疗药物研发又有哪些推动?
我们邀请到了本次研究的合著作者Robin Chan博士,并结合他此前在神经学权威杂志《GLIA》(影响因子:7.452)发表的关于α-syn蛋白与血脑屏障(BBB)损坏的文章“Astrocytic VEGFA: An essential mediator in blood-brain-barrier disruption in Parkinson's disease”,就帕金森病(PD)的机制研究与临床诊疗方案的研发展开对话,希望能为从事帕金森病乃至神经退行性疾病机制研究和诊疗方案的业界同仁带来启示。

Robin Chan,新加坡国立大学生物化学博士,师承Markus R. Wenk教授,并在哥伦比亚大学脂质代谢和神经疾病从事博士后研究,拥有哥伦比亚大学商学院MBA学位。
Dr. Chan 专注于神经退行性疾病研究、病理学和细胞生物学等领域,在脂质代谢和神经疾病领域有十余年建树,曾任哥伦比亚大学脂质组学核心实验室创始主任,于国际顶尖期刊(Nature、Nat Neurosci.等)上发表论文逾 38 篇,并多次获得美国国立卫生研究所(NIH)和非盈利研究基金会科研资助。以学术研究科学家身份转战商业领域后,Dr. Chan 积累了丰富的产业经验,加入焕一生物担任战略合作副总裁(VP of Strategic Partnerships),主导公司战略合作,推进公司与国际MNC与Biotech的深度合作,加速公司在联合研发及商业策略上的发展,并多维赋能焕一生物在产业生态中开展深层合作。
橙果局:您迄今连着在顶级期刊上发布了两篇文章,可以为我们介绍下这两篇文章分别的研究进展吗?
Dr Robin Chan :这两篇文章分别聚焦帕金森病(PD)两个致病特征的机制,包括星形胶质细胞激活引起的血脑屏障(BBB)损伤和含有α-syn的红细胞外囊泡诱导的外周单核细胞过度激活。
早前的一篇文章主要阐述了帕金森病(PD)发病机制中,有害的寡聚α-syn蛋白在血脑屏障(BBB)损坏过程中的重要作用。我们发现外周血红细胞外囊泡(RBC-EVs)的寡聚α-syn蛋白能够穿过血脑屏障(BBB)进入星型胶质细胞,并导致其活化。活化后,星型胶质细胞会产生两种蛋白,即VEGFA 生长因子(星形胶质细胞中血管内皮生长因子)和NOS氧化氮合酶蛋白。研究成果表明,VEGFA 和 NO的产生和释放,最终引起血脑屏障(BBB)完整性受损。
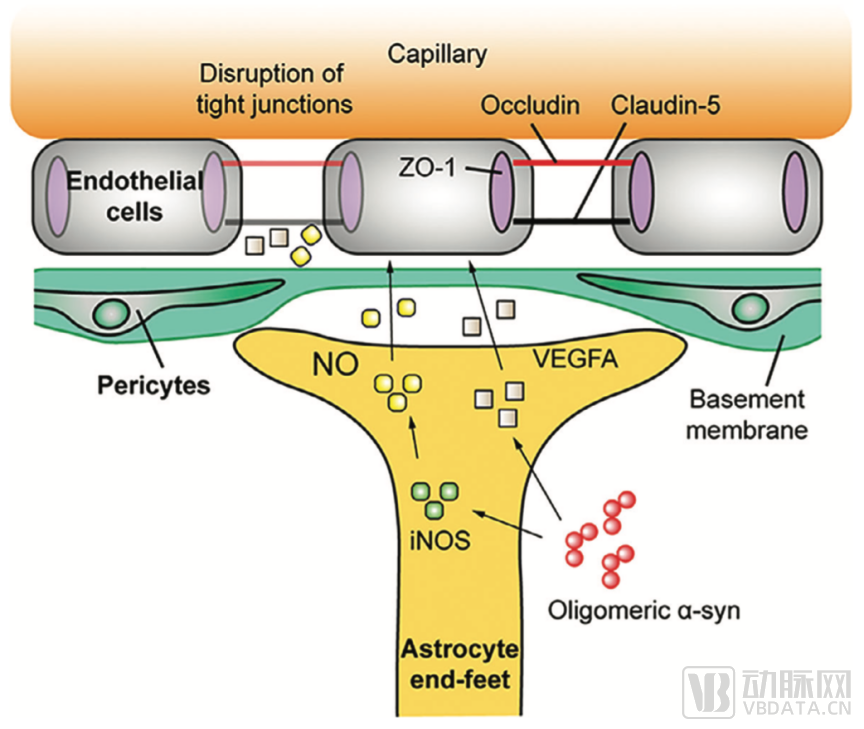
星形胶质细胞寡聚a-Syn激活引起血脑屏障(BBB)功能障碍机制的说明
(来源:Lan et al. Glia. 2022. 70(2):337-353.)
这是一个比较重要的研究结果,因为血脑屏障(BBB)损坏不仅仅存在于帕金森病(PD),在其他神经退行性疾病中也存在。这一机制的揭示,也为VEGFA和NO信号通路可以作为帕金森病(PD)中血脑屏障(BBB)保护的潜在治疗性靶点提供了证据。
另一篇文章聚焦帕金森病(PD)发病机制中外周单核细胞过度激活的反应机制,并描述了含有α-syn蛋白的红细胞外囊泡(RBC-EVs)、内吞作用、LRRK2之间的相互作用。
目前已经有研究表明,外周血中免疫细胞的激活程度能够影响帕金森病的严重程度。我们这一项研究的结果证实,外周血中的α-syn蛋白能够激活血液中的免疫细胞。
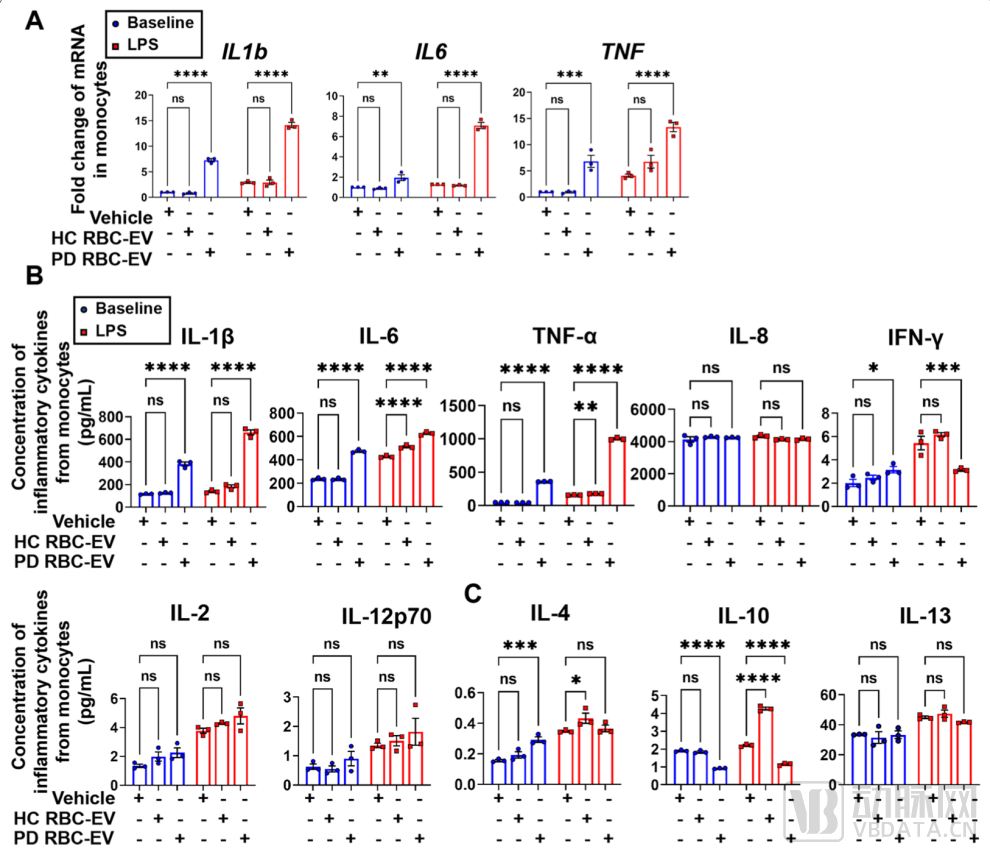
PD患者中RBC-EVs诱导的单核细胞的炎症敏感性
(A) 使用qPCR定量分析IL1b、IL6和TNF mRNA水平
使用MSD定量分析(B) 促炎细胞因子和(C)抗炎细胞因子
(来源:Liu et al. J Neuroinflammation, 2022, 19(1):53.)
橙果局:这些进展对帕金森病潜在治疗药物、诊断技术的研/开发有哪些价值?
Dr Robin Chan :我先讲下血脑屏障(BBB)的研究吧。这个研究其实解释了血脑屏障(BBB)受损是如何发生,由哪一个细胞和因子引起的。我们的研究中还包含了针对VEGFA和NO信号通路抑制剂的体外和体内研究,证明这些抑制剂对血脑屏障(BBB)有保护作用。如果能够在疾病的初期阶段阻止这个信号通路,哪或许就可以阻止这种损害的发生。那么在疾病解决方案的转化上就有了一个比较明确的方向,可以基于这个研究去找到相关的靶点,研发合适的药物。
而针对外周血中免疫细胞激动的研究在治疗方向的转化还需要进一步探索。免疫系统的激动程度跟病人的炎症程度有一定的相关性。我们目前的想法是去探索外周血中的免疫细胞是否会存在某一种生物标志物,基于这个生物标志物去开发更加精准的早筛方案。
橙果局:为什么针对α-syn/外周免疫系统失调和PD发病关联的研究会成为学术界的研究热点,哪些研究值得关注?这些研究对临床解决方案的研/开发有哪些意义?
Dr Robin Chan :这个问题需要回述一些历史。帕金森病(PD)患者的大脑内部会存在蛋白的异常聚集,称为路易小体,在100年前首次被观察到。
这种蛋白的异常聚集其实是许多神经退行性疾病的共性,不同的神经退行性疾病对应的是不同种类的蛋白聚集。帕金森病(PD)路易小体对应的就是α-syn蛋白异常聚集, 据假设这是该疾病的一个关键原因。因此,在帕金森病研究领域,针对寡聚α-syn蛋白的研究就成了学术界的研究热点。经过多年研究,寡聚α-syn对帕金森病(PD)发病的有害影响(从妨碍突触信号,到激活小神经胶质细胞,再到引发神经炎症)得到了更全面的理解。我们本次的两项研究了寡聚α-syn的两个新维度:寡聚α-syn是如何破坏BBB和寡聚α-syn对外周免疫系统的影响。
这两项研究强调了帕金森病与免疫系统功能障碍之间的联系,这已成为帕金森病研究界的一个重要研究课题。
美国学者团队Sulzer和Sette发现,外周血中的T细胞识别α-syn衍生肽,并且由此激发T细胞的免疫反应,渗透在患者大脑中,导致了帕金森病(PD)患者脑部神经元死亡。该成果于2017年在《Nature》上发布。
2020年,团队后续研究发现,帕金森病(PD)发病早期与含有α-syn蛋白的T细胞的免疫反应存在关联。这也说明了对T细胞免疫反应的监测可以帮助进行帕金森病(PD)的早筛以及患者治疗。
除此之外,全基因组关联分析研究还发现了许多编码调节免疫细胞功能的蛋白质的风险基因,如LRRK2、PRKN等。另一方面,TNF和IL1B等免疫相关基因的多态性也会影响PD风险和发病年龄。
但需要强调的是,存在这些风险基因也并不意味着一定会患病。因此,我们需要在遗传学(基因组)之外更多维地来理解这些已识别的遗传风险因素的重要性,从功能上理解编码的蛋白质和代谢物如何相互作用导致免疫系统功能障碍。
综上,所有这些研究成果表明帕金森病(PD)与自身免疫疾病相似,因为外周免疫系统被慢性激活,并产生炎症介质,可能刺激神经炎症,从而促进PD的发病机制。这些研究对于促进旨在延缓帕金森病(PD)患者病情恶化和帕金森病前期(发病前)发生的新疗法的发展具有重要意义。
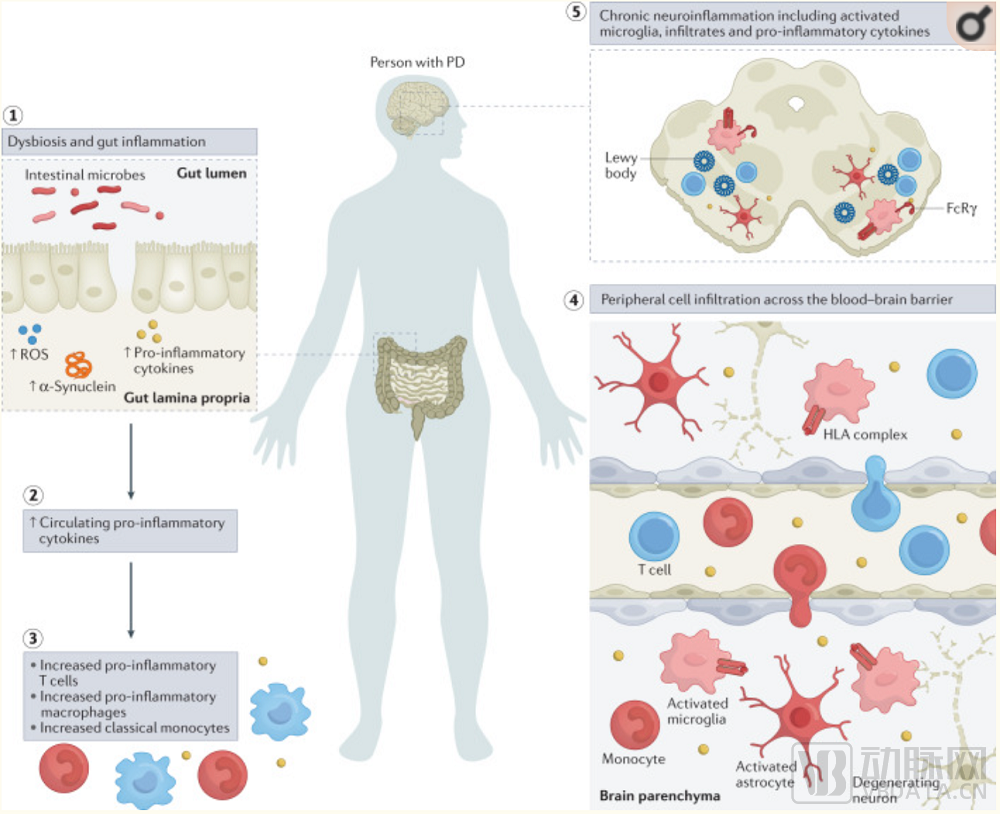
帕金森病的炎症临床表现 (来源:Tansey et al. Nat Rev Immunol. 2022, 1-17.)
另外,学术界还有大量围绕早筛和疾病监测生物标志物展开的研究。早前,帕金森病(PD)生物标志物研究多数聚焦单一蛋白标志物,如脑脊髓液(CSF)中的α-syn 和 tau蛋白。但随着科学家们对疾病的认知有了巨大突破,以及多组学技术的发展,学术界的研究方向也转向聚焦多维标志物,比如外泌体、免疫细胞、遗传学标识、非α-syn/tau蛋白、脂质以及其他类的分子。新的研究也从脑脊髓液(CSF)转而关注外周血、唾液等更易获得的液体来源。
除了基于液体的生物标志物,先进AI技术的发展也提升了大脑和视网膜成像、电子移动性分析等技术的研究辅助价值。新型的生物标志物的出现为帕金森病(PD)的早筛和治疗提供了重要工具。
橙果局:基于现目前的研究证据,我们可以认为免疫反应是帕金森病的致病原因吗?
Dr Robin Chan :这是一个很难回答的问题,帕金森病(PD)是一种高度复杂的疾病。帕金森病(PD)的发病由多种并发的致病机制同时作用所导致,包括α-syn蛋白异常聚集、内溶酶体运输失调、内在的获得性免疫变化、以及环境因素如接触病毒、饮食引起的肠道微生物群落变化等。我只能说帕金森病(PD)与免疫失调的确存在强有力的关联。
最初我们认为,当神经细胞不能消耗多余的蛋白时,就会产生帕金森病(PD)。但现在随着我们掌握的证据越来越多,对疾病对认知也渐渐提高,蛋白消耗只是其中可能的一种发病机制。免疫系统的过度反应、微生物组代谢物对肠脑轴的影响,这些都可能与帕金森病的发病机制有关。
但是,这些多种致病机制中究竟哪种是帕金森病(PD)的发病根源仍未有定论。所以我也会提出一个假设,帕金森病的发病会有不同的通路导致的疾病,患者发病的原因或者通路可能会各不相同,但是最后的结果都是帕金森病。这也表示,要成功治疗帕金森病(PD)患者,有必要确定哪条通路与特定患者最相关, 这就需要更精准的生物标志物,以此帮助到对病人的精准用药。
橙果局:您之前提到了神经退行性疾病之间存在共性,具体有哪些呢?这些共性是否有利于其他神经退行性疾病治疗药物的研/开发?
Dr Robin Chan :神经退行性疾病之间确实存在一些共性。其中一点就是有害蛋白在神经元细胞中的异常聚集。具体而言,这是指由于内溶酶体和自噬途径的功能失调,导致不同致病蛋白和其他疾病相关致病蛋白的聚集。
另一种共同性则是神经退行性疾病和免疫激活的关联,慢性神经炎症和免疫系统失调导致了疾病发生和发展。比如,在阿尔兹海默病(AD)患者中发现T细胞能够识别Aβ蛋白,就像在帕金森病(PD)患者中发现T细胞能够识别α-syn蛋白。
基于这些共性,我认为帕金森病(PD)相关的研究在很大程度上能够帮助到其他神经类疾病的研究,对后续对疾病研究和药物研发都会有帮助,反之亦然。
当然,神经退行性疾病间的其他相似之处仍待继续探索。比如肠-脑轴互作机制以及环境因素和免疫的互相作用对神经退行发生发展的影响。肠道的一些代谢产物也会影响外周血对免疫系统,免疫系统在直接对脑部产生影响。这个方向是值得我们去观察和探索的。
橙果局:下一步有什么研究计划?
Dr Robin Chan :焕一生物在神经退行性疾病的主要研究方向是帕金森病(PD)和阿尔兹海默病(AD)的药物靶点和诊断生物标志物。焕一生物正在利用多组学技术和AI驱动的机制建模方法,联合免疫知识图谱和自主搭建的端到端生物计算平台,多维度深度理解神经免疫机制,以此提升药物研发的效率和成功率,最终赋能到神经类疾病精准诊疗的发展。





























