
商务合作

动脉网APP
2026年4月24日至2026年5月7日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及12个器械获FDA批准,4个器械获欧盟及其它批准,3个器械获NMPA创新产品批准,另有477个器械获NMPA批准注册文件。
海外获批
一 、FDA
1. 雅培AI心脏成像平台获批,冠心病介入治疗迎来“精准导航”
冠心病介入治疗迎精准导航,雅培新一代冠脉成像平台Ultreon 3.0获美国FDA批准和欧盟CE认证,即将登陆美欧市场。该平台在原有Ultreon 2.0基础上新增AI算法,优化OCT成像技术。OCT是诊断治疗冠心病“核心武器”,Ultreon 3.0将AI与OCT完美结合,能自动捕捉分析图像,实时指导手术,提供堵塞情况、评估堵塞程度、推荐支架型号和放置位置。其核心优势包括成像更清晰,有效避免漏诊;实时分析图像,节省手术时间,降低患者术中风险;智能推荐支架方案,提升手术疗效。临床医生高度评价,认为其不止是升级,更是“跨越式突破”。
2. RIVANNA的Accuro XV肌肉骨骼超声成像系统获得FDA 510(k)许可
RIVANNA®是一家开发人工智能临床决策支持解决方案的公司,宣布其Accuro® XV诊断超声系统已获得FDA的510(k)许可。该许可允许合格的医疗专业人员在医院和诊所使用Accuro XV进行肌肉骨骼成像,标志着该公司取得了重要的监管成就。RIVANNA还在推进Accuro XV平台的人工智能功能,包括用于改善骨骼可视化的图像分割模块BoneEnhance®,以及利用容积超声成像进行自动骨折识别的计算机辅助检测算法CADe/x。这些功能正在通过覆盖八个学术医学中心的多中心临床研究进行验证。RIVANNA的联合创始人兼首席执行官Will Mauldin博士强调,FDA的许可突显了其核心平台在各种临床应用中的可扩展性,并使公司能够为四肢损伤分诊设定新标准。Accuro XV包含一个可适形的3D容积超声探头,可自动获取大视场图像。
3. 诊断设备研发商Bright Uro旗下Glean®腹部传感器获FDA批准
诊断设备研发商Bright Uro宣布,美国食品药品监督管理局(FDA)已批准Glean®腹部传感器的510(k)许可。这款新型传感器扩展了Glean®尿动力学系统的功能,使其能够进行多通道尿动力学检查。该综合系统支持无线、无导管的动态尿动力学监测,旨在为下尿路功能障碍及其他泌尿系统疾病患者的临床决策提供支持。Glean系统突破了当前基于导管的尿道压力检测的局限——这种检测不仅让患者感到不适,而且往往产生不精确的数据。Glean提供更准确的数据,有助于制定更明智的治疗方案,因此更受青睐。
4. 无需眼镜的3D成像软件获得FDA手术规划许可
临床医生常常依赖二维扫描来进行三维决策,这可能会妨碍深度感知,并在规划和会诊期间使对复杂解剖结构的共同理解变得复杂。头戴式系统也对自然的医患互动提出了挑战。为了解决这些问题,医疗团队正在寻找能够在普通手术室屏幕上显示多维数据且不干扰工作流程的工具。一款新软件系统最近获批使用,可以在普通屏幕、自动立体屏幕和虚拟现实显示器上提供无需眼镜的3D可视化CT(计算机断层扫描)和MR(磁共振)图像。由法国巴黎的Avatar Medical公司开发的Avatar Medical Vision允许使用CT和MR数据进行即时的3D处理、审查和手术规划。该系统支持与医学影像存档与通信系统(PACS)集成,并有助于术前规划和术中参考的分析、注释和操作。该系统已获得FDA 510(k)许可,这是首个针对无需眼镜的3D医学影像显示设计的软件批准,并且兼容Barco Eonis 3D无眼镜显示器。
5. FX Shoulder Solutions获得美国食品药品监督管理局对 FX V135® Easytech 肩关节系统的510(k) 上市许可
FX Shoulder Solutions已获得美国食品药品监督管理局(FDA)对其FX V135® Easytech肩关节系统的510(k)批准,这是一种新一代的无柄肩关节置换植入物。该系统为外科医生提供了灵活性,可以无柄方式开始手术,并在需要时切换到短柄解决方案,而无需额外的器械系统。该设计由单一肱骨托盘支持,体现了FX自2011年以来对减少器械使用的承诺,同时并未牺牲植入物的选择或尺寸。FX V135® Easytech在美国市场独具特色,其模块化设计将无柄锚定基座与可拆卸的短柄适配器结合在一个肱骨平台上。该系统提供解剖型和反向型两种配置,角度选项分别为135°,反向型还提供145°。锚定基座的尺寸范围从32毫米到44毫米,肱骨短柄适配器的直径为8毫米,确保与先前获批的肱骨组件兼容。
6. 膝关节置换的增强现实系统获得FDA批准
Pixee Medical已获得FDA 510(k)批准,其Knee+ NexSight是一款为高通量膝关节置换设计的新一代AR平台。该系统采用紧凑型设计,提升了外科医生的舒适度和手术室适应性,并确保与手术罩兼容。Knee+ NexSight将虚拟显示直接投射到外科医生的视野中,并支持语音控制以实现免提操作。它在不使用复杂或昂贵的机器人系统的情况下,提供与机器人相当的精度,同时使用微创器械且不含一次性组件。该平台无缝集成到现有的手术工作流程中,相比传统技术不会增加额外的手术时间,因此非常适合不断增长的美国市场,包括门诊手术中心。
7. FDA正式获批,美敦力新一代二尖瓣瓣膜问世,心脏手术迎来新突破
近日,FDA正式批准美敦力新一代二尖瓣生物瓣Mosaic Neo问世。二尖瓣病变会危及生命,传统二尖瓣置换手术存在切口大、视野模糊、植入难度高等痛点。Mosaic Neo作为“全场景适配”的二尖瓣生物瓣,可通过三种方式植入,适配更多患者需求。它有三大核心升级:低剖面瓣膜支架搭配小型切口测量器,能缩小切口、减少创伤;荧光透视下可视性升级,提升手术精准度和安全性;设计更贴合临床需求,可解决更多复杂心脏解剖问题。Mosaic Neo基于原有Mosaic瓣膜平台,结合数十年经验历经多阶段精心打磨而成,研发始终围绕“解决临床痛点、提升患者预后”展开。
8. 飞利浦获得FDA 510(k)批准,用于1.5T磁共振成像的Smart Fit TorsoCardiac线圈,支持患者舒适度和简化工作流程
飞利浦宣布其Smart Fit TorsoCardiac 1.5T线圈已获得FDA 510(k)许可,并带有CE标志。这款轻便、灵活的磁共振线圈旨在提高患者的舒适度,并优化放射科的工作流程,而当前放射科正面临需求增长、人力不足和复杂检查等日益严峻的挑战。该线圈的设计能够紧密贴合患者的身体结构,确保一致的定位和可靠的信号采集,从而为不同患者群体提供高质量的成像。其轻量化和易于操作的特点旨在提升工作流程效率,使放射团队能够在不牺牲诊断准确性的情况下应对更多的扫描量。Smart Fit TorsoCardiac线圈代表了磁共振技术的一项创新,专注于减少差异、简化流程并提供一致的成像结果。
9. Chest Wall Innovations获得FDA 510(k)许可的PC Fix肋骨固定系统
医疗设备公司Chest Wall Innovations宣布,其PC Fix肋骨固定系统于2026年4月24日获得FDA的510(k)许可,从而可以在美国进行商业化推广。该系统独特之处在于同时提供PEEK和钛合金植入物,支持胸腔内和胸腔外手术方法,为外科医生在治疗创伤性肋骨骨折时提供了无与伦比的灵活性。肋骨骨折在钝性胸部创伤中很常见,而手术固定正逐渐成为部分患者的标准治疗方法。Chest Wall Innovations开发了PC Fix系统,以满足这一不断增长的创伤手术领域的需求。首席执行官Ken Kremer强调,此次获批得益于专注的开发、与领先外科医生的合作以及团队的奉献精神,公司现在将重点转向这一服务不足领域的商业化和创新。该公司计划在2026年第二季度开展首次人体病例试验,并随后进行更广泛的商业推广。
10. 3Shape获得FDA 510(k)许可的3Shape Dx软件
3Shape宣布其Dx软件已获得FDA批准,此前审查于2026年4月10日完成。510(k)上市前通知允许Dx(R1)软件在美国市场商用,使合格的牙科专业人员能够在诊所使用该软件诊断关键的口腔健康状况,并评估成年患者牙齿和牙龈的变化。3Shape首席执行官Jacob Paulsen表示,对于将这一变革性解决方案引入美国感到兴奋,并强调了公司对负责任创新以及高标准临床和监管要求的承诺。此次批准涵盖了Dx Plus和Dx Standard两个版本。Dx Plus仅兼容3Shape TRIOS 6扫描仪,利用人工智能协助检测龋齿、牙菌斑、牙齿磨损和牙龈退缩等口腔健康问题。Dx Standard兼容除TRIOS Core以外的所有3Shape TRIOS型号,帮助牙医手动跟踪和量化患者牙齿的变化,支持常规检查并节省治疗准备时间。
11. TytoCare获得FDA De Novo批准,推出首款AI驱动的鼓膜分析工具
虚拟护理公司TytoCare宣布其Tyto Insights™耳鼻喉套件的首个模型获得了FDA的De Novo分类,开创了一个人工智能驱动的耳鼻喉图像分析的新监管类别。该分类针对“耳鼻喉图像分析仪”。该解决方案利用人工智能分析鼓膜的耳镜视频,通过检测鼓膜隆起(急性中耳炎及其他疾病的常见症状)来帮助医疗服务提供者和患者。该工具专为六个月及以上年龄的患者设计,向医疗保健提供者提供结果作为临床支持工具,并告知患者其病情。Tyto Insights™耳鼻喉套件的开发得益于TytoCare专有的160万张耳朵图像和记录数据库。耳部相关疾病,包括中耳炎等感染,是儿科就诊的常见原因。
12. CGBIO获得FDA 510(k)批准的患者专用钛植入物“EASYMADE TI”
韩国公司CGBIO取得了重要里程碑,其患者定制的钛植入物EASYMADE TI获得了美国食品药品监督管理局(FDA)的510(k)许可。这标志着韩国公司首次为美国市场定制的钛植入物获得此类许可,彰显了CGBIO在全球范围内的技术与监管专业能力,特别是在颅骨和颅面重建领域。EASYMADE TI基于个体CT数据设计,用于重建颅骨和非承重颅面缺陷,采用医疗级钛合金通过激光粉末床熔融(LPBF)这一先进的金属3D打印技术制造。产品的交付流程也值得一提,它从美国临床医生提供患者的CT影像开始,确保针对每个病例的个性化处理。
二、欧盟及其它
1. 雅培AI心脏成像平台获批,冠心病介入治疗迎来“精准导航”
冠心病介入治疗迎精准导航,雅培新一代冠脉成像平台Ultreon 3.0获美国FDA批准和欧盟CE认证,即将登陆美欧市场。该平台在原有Ultreon 2.0基础上新增AI算法,优化OCT成像技术。OCT是诊断治疗冠心病“核心武器”,Ultreon 3.0将AI与OCT完美结合,能自动捕捉分析图像,实时指导手术,提供堵塞情况、评估堵塞程度、推荐支架型号和放置位置。其核心优势包括成像更清晰,有效避免漏诊;实时分析图像,节省手术时间,降低患者术中风险;智能推荐支架方案,提升手术疗效。临床医生高度评价,认为其不止是升级,更是“跨越式突破”。
2. 金属药物支架系统正式获得俄罗斯医疗器械注册证
威高介入集团旗下深圳市金瑞凯利生物科技有限公司自主研发的金属药物支架系统,近日成功通过俄罗斯相关监管部门审核,正式获得俄罗斯医疗器械注册证。这一里程碑标志着该产品品质与安全性获国际认可,为开拓俄罗斯及欧亚市场奠定坚实基础。威高介入坚持创新驱动,严格遵循国际质量标准,此次注册证的取得,不仅彰显了公司在体系与合规方面的实力,更体现了服务全球医疗需求的决心。未来,威高介入将继续推动产品国际化,为更多医疗机构和患者提供优质服务。
3. 金属药物支架系统正式获得乌克兰医疗器械注册证
威高介入集团旗下深圳市金瑞凯利生物科技有限公司自主研发的金属药物支架系统,近日通过乌克兰监管部门审核,正式获得乌克兰医疗器械注册证,取得东欧市场准入资质。这一成果体现了威高介入在研发、生产与合规管理方面的综合能力,印证了其服务全球患者的承诺。威高介入一直秉持创新驱动发展理念,严格遵循国际质量标准。未来,威高介入将继续深耕国际市场,加大研发投入,提升产品品质,以更优质安全的产品服务全球患者,为国产医疗器械走向世界、扎根全球市场筑牢根基。
4. 美敦力宣布Stealth AXiS™手术系统获得CE认证
医疗技术领域的领导者美敦力公司已获得其Stealth AXiS™手术系统的CE标志批准,继近期获得FDA许可后进一步扩大了在欧洲的使用范围。这一下一代平台将手术规划、导航和机器人技术集成到一个智能系统中,专为脊柱和颅脑手术设计,展现了其在不同外科专业中的适应性。美敦力副总裁奥利·普罗斯佩里强调了这一里程碑的重要性,特别是在欧盟医疗器械法规(MDR)下,凸显了公司致力于在多样化医疗环境中引入有意义的创新。Stealth AXiS™系统支持各种临床工作流程和手术环境,使医院能够根据当前需求采用功能,同时保持对未来改进的灵活性。一项显著的创新是LiveAlign™节段追踪技术,可让外科医生实时观察解剖运动和患者对齐情况,从而提高手术过程中的精确性。
国内获批
一、创新器械获批
1. 心腔内超声诊断设备和一次性使用心腔内超声导管获批上市
2026年4月30日,国家药品监督管理局批准了西安华峰医疗科技有限公司的心腔内超声诊断设备、一次性使用心腔内超声导管注册申请。心腔内超声诊断设备由主机、显示器、导管连接单元组成,一次性使用心腔内超声导管由导管主体、操作手柄和连接器组成。二者配合使用,用于成人心脏及心脏大血管、心内解剖结构的超声成像。该产品可显示心腔内组织结构,有利于引导房间隔穿刺及其他心腔内操作。该产品的上市为患者提供了更多的治疗选择。
2. 一次性使用血栓切除装置获批上市
2026年4月30日,国家药品监督管理局批准了上海蓝脉医疗科技有限公司的一次性使用血栓切除装置注册申请。该产品由一次性使用取栓导管和手柄(含电池)组成,与导管鞘、导丝配合使用,适用于急性髂、股深静脉血栓经皮腔内去除。该产品采用同轴双通道技术、一体化设计。该产品的上市为患者提供了更多的治疗选择。
3. 人类白细胞抗原(HLA)基因分型检测试剂盒(荧光PCR法)获批上市
2026年4月30日,国家药品监督管理局批准了江苏伟禾生物科技有限公司的人类白细胞抗原(HLA)基因分型检测试剂盒(荧光PCR法)注册申请。该产品采用实时荧光PCR结合Taqman探针技术,用于体外定性检测人类全血样本中人类白细胞抗原HLA-A、B、C、DRB1、DQB1位点的基因分型。通过移植之前双方的HLA分型鉴定,为肝肾等实体器官移植供受者的选择提供参考。
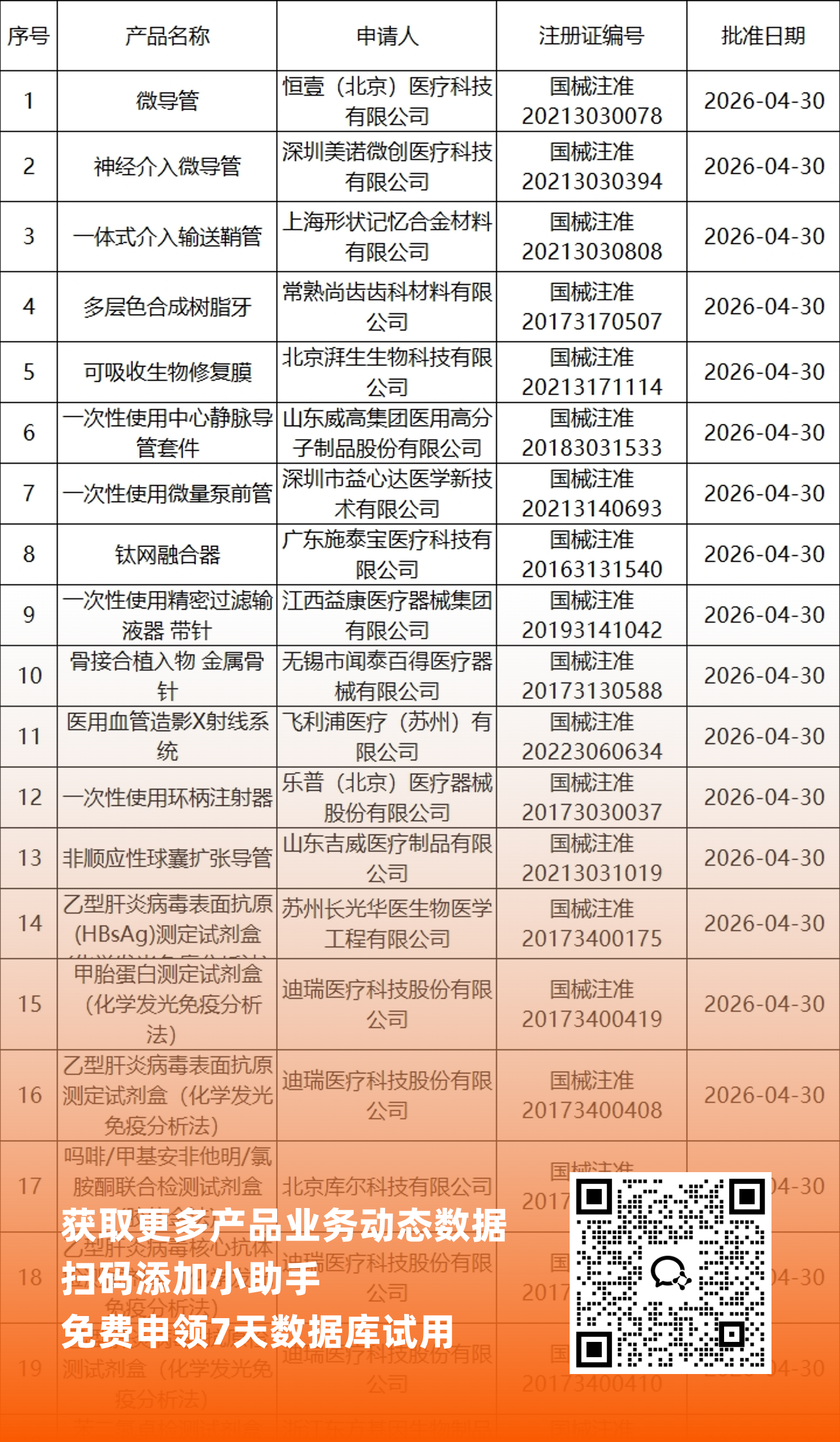
二、NMPA最新获批器械产品明细
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。