商务合作

动脉网APP
2024年8月16日至8月22日,动脉橙产业智库重点整理了医疗器械产品国内外获批资讯及数据,涉及13个器械获FDA批准,1个器械获欧盟及其他批准,2个器械获NMPA创新产品批准,另有382个器械获NMPA批准注册文件。
海外获批
一、FDA
1. 获批FDA,下一代水刀手术机器人
水刀机器人公司的新一代Hydros手术机器人系统获FDA批准,该系统结合AI和图像引导技术,实现精准、微创的前列腺手术,提高手术效率和患者生活质量。
2. 医疗技术公司AISAP首创CARDIO AI床旁超声诊断评估软件获FDA批准
医疗技术公司AISAP宣布,美国食品和药物管理局(FDA)已批准其人工智能心脏护理超声波软件平台510(k)许可。基于云的平台将四个CADx模块和八个关键测量值组合到一个心脏超声软件包中,该软件包自动生成分析,解释和报告。CARDIO允许具有基本扫描技能的临床医生在几分钟内在床边诊断出高达90%的常见心脏参数,这可能会导致更早的检测,更好的患者预后,并为卫生系统节省成本。
3. 获批FDA,美敦力神经刺激系统可兼容MRI
美敦力神经刺激系统获FDA批准,扩展MRI标签,患者植入DBS后可安全接受MRI扫描,有助于疾病诊断、手术效果确认及治疗效果监测。
4. 泌尿外科手术机器人开发商PROCEPT BioRobotics下一代平台HYDROS机器人系统获FDA 510(k)批准
在FDA 510(k)批准其下一代HYDROS机器人系统后,PROCEPT BioRobotics Corp.(PRCT)股价周三飙升逾13%。该系统具有FirstAssist AI治疗计划,高级图像指导,旨在增强外科医生的经验,并提供准确的治疗计划以获得更好的结果。首席执行官Reza Zadno表示,这标志着该公司在美国安装了400多个机器人系统,这是一个关键时刻。伊坎医学院的史蒂文·卡普兰(Steven Kaplan)博士称赞该系统能够利用人工智能获得最佳手术效果,保持患者的生活质量。
5. AlgoDx的软件获得FDA 510(k)批准用于败血症预测
美国食品和药物管理局(FDA)已授予AlgoDx脓毒症检测软件NAVOY CDS 510(k)许可,为医疗AI公司向美国医疗保健市场的扩张扫清了道路。NAVOY CDS是一种作为医疗设备的软件(SaMD),通过分析ICU的患者数据(包括重要参数和血液检查),帮助临床医生早期识别败血症,以提供及时的警告和干预机会。AlgoDx首席产品官安德烈亚斯·马库拉(AndreasMacura)认为,这一许可证明了他们团队在开发先进医疗设备软件方面的专业知识和奉献精神,并且NAVOY CDS可以通过促进早期败血症检测和治疗来显着改善患者预后。
6. 外科设备研发商Si-Bone骨盆固定植入系统获FDA批准和突破性设备认定
Si Bone宣布其iFuse Torq TNT植入系统已获得FDA 510(k)许可和FDA突破性设备指定。TNT植入物设计用于骨盆脆性骨折固定和骶髂关节融合,满足骶骨和髂骨的特定解剖和骨矿物质密度需求。首席执行官Laura Francis表示,该公司很荣幸通过为骨盆脆性骨折提供第一个特定解剖结构的系统,帮助外科医生更快地恢复体弱和老年患者的活动能力。TNT是一种多孔螺纹植入物,可以跨越骨盆后部,并因其提供比当前护理标准更有效治疗的潜力而获得突破性指定。
7. 细菌减少系统开发商SoClean最新CPAP面罩和软管抑菌装置获FDA批准
SoClean是CPAP设备细菌减少系统的领导者,其SoClean 3+设备已获得FDA批准。该产品是FDA批准的唯一一种在清洁后用于减少兼容家用CPAP口罩和软管上细菌的辅助剂,可实现99.9%的细菌减少。它可以在OTC和在线获得,目前与特定的ResMed产品兼容。SoClean正在努力扩展兼容性,并将提供升级程序。该公司拥有150多项专利,专注于细菌减少技术。首席执行官Robert Wilkins强调了CPAP用户日常使用和维护中易于减少细菌的重要性。
8. 医疗美容设备公司Candela多用射频美肤平台Matrix™系统扩大适应症获批FDA
赛诺龙公司的Matrix™射频美肤平台获得FDA批准,用于治疗I-IV型皮肤患者的面部皱纹。研究显示,该平台能显著改善面部皱纹,且94%的受试者评价治疗结果有大幅或非常显著改善。该平台采用最细微针阵列,可精准输送射频能量,提高求美者舒适度和缩短恢复时间。
9. 西门子人工智能心血管超声系统Acuson Origin获FDA批准
西门子Healthineers的人工智能心血管超声系统Acuson Origin已获得FDA批准。人工智能功能是在包含20多亿个注释图像的海量图像数据库上训练的。
10. 成像和数据平台开发商Spryte Medical神经光学相干断层扫描技术获FDA突破性设备称号
美国食品和药物管理局(FDA)已经授予Spryte Medical的神经光学相干断层扫描(nOCT)技术突破性的设备名称,认识到其在诊断或治疗危及生命的疾病方面潜在的革命性影响。这种指定将加快技术的开发、审查和患者访问。此外,Spryte Medical已被纳入FDA的总产品生命周期咨询计划(TAP),旨在加速创新医疗设备的开发。Spryte Medical首席执行官David Kolstad强调了他们的神经OCT成像平台对脑血管疾病患者的潜力,并对与FDA合作表示兴奋。与主要为心脏病学设计的传统血管内成像系统不同,nOCT技术标志着神经介入技术的重大进步,专门为脑血管应用而设计。
11. 全球首款,医疗监测仪器研发商Masimo远程监控连接医用手表Masimo W1获FDA批准
FDA批准全球首款远程监控医用手表Masimo W1,配备SafetyNet功能,可连续监测血氧饱和度和脉搏率,提高护理质量。
12. 万孚生物两款芬太尼尿液检测试剂产品获得美国FDA 510(k)批准
万孚生物两款芬太尼尿液检测试剂获美国FDA批准,可满足家庭自测及专业机构检测的需求,将有力支撑应对美国乃至全球的药物滥用危机。万孚生物本次获得美国 FDA 510(k)上市许可的芬太尼尿液检测试剂,可定性检测人类尿液中是否含有芬太尼。产品检测阈值为1 ng/ml,具有极高的灵敏度,且操作简便、快速出结果,该试剂可用于家庭自测和专业机构检测等场景。获得美国 FDA 510(k) 批准后,用户无需处方即可通过电商、药店、商超等渠道购买万孚生物芬太尼检测产品。同时,该产品设计了几种产品形式,用户可根据自身检测需求灵活选择,方便快捷。
13. 全球首款,深智透医AI磁共振生成加速软件获FDA批准
深智透医研发的SubtleSYNTH软件获FDA批准,成为全球首款AI驱动磁共振生成加速软件,可大幅提高检查效率,多中心研究显示其诊断价值与传统方法相当甚至更优。
二、欧盟及其它
奥精医疗“BonGold™人工骨修复材料”在马来西亚获得注册证
奥精医疗的BonGold™人工骨修复材料在马来西亚获注册证,用于骨缺损修复,具有广阔的临床应用潜力和市场空间。
国内获批
一、创新器械获批
1. 静脉支架系统获批上市
2024年8月22日,国家药品监督管理局批准了上海蓝脉医疗科技有限公司“静脉支架系统”创新产品注册申请。
该产品由静脉支架及输送系统组成,预期在髂股静脉内使用,用于治疗非血栓性髂静脉压迫综合征、深静脉血栓形成及深静脉血栓形成后综合征。其中,支架采用一体化编织方法,具有不同网孔密度,疏密网孔相结合的设计可有效满足临床上对支架的支撑力和柔顺性需求。
2. 经导管主动脉瓣系统获批上市
2024年8月22日,国家药品监督管理局批准了北京佰仁医疗科技股份有限公司“经导管主动脉瓣系统”创新产品注册申请。
该产品由生物瓣膜、输送器、球囊扩张导管、导管鞘套件、压握器、充压泵组成。采用球囊扩张式瓣架结构,适用于经心脏团队结合评分系统评估后认为患有有症状的、钙化的、重度退行性自体主动脉瓣狭窄,不适合接受常规外科手术置换瓣膜、年龄大于等于70岁的患者。在医学影像设备监护下,可选择性通过长、短两款输送系统经由不同入路将生物瓣膜植入到人体主动脉瓣环处,代替原有的病变主动脉瓣膜,改善病变部位狭窄,改善心功能,满足不同入路患者临床需求。
二、NMPA最新获批器械产品明细
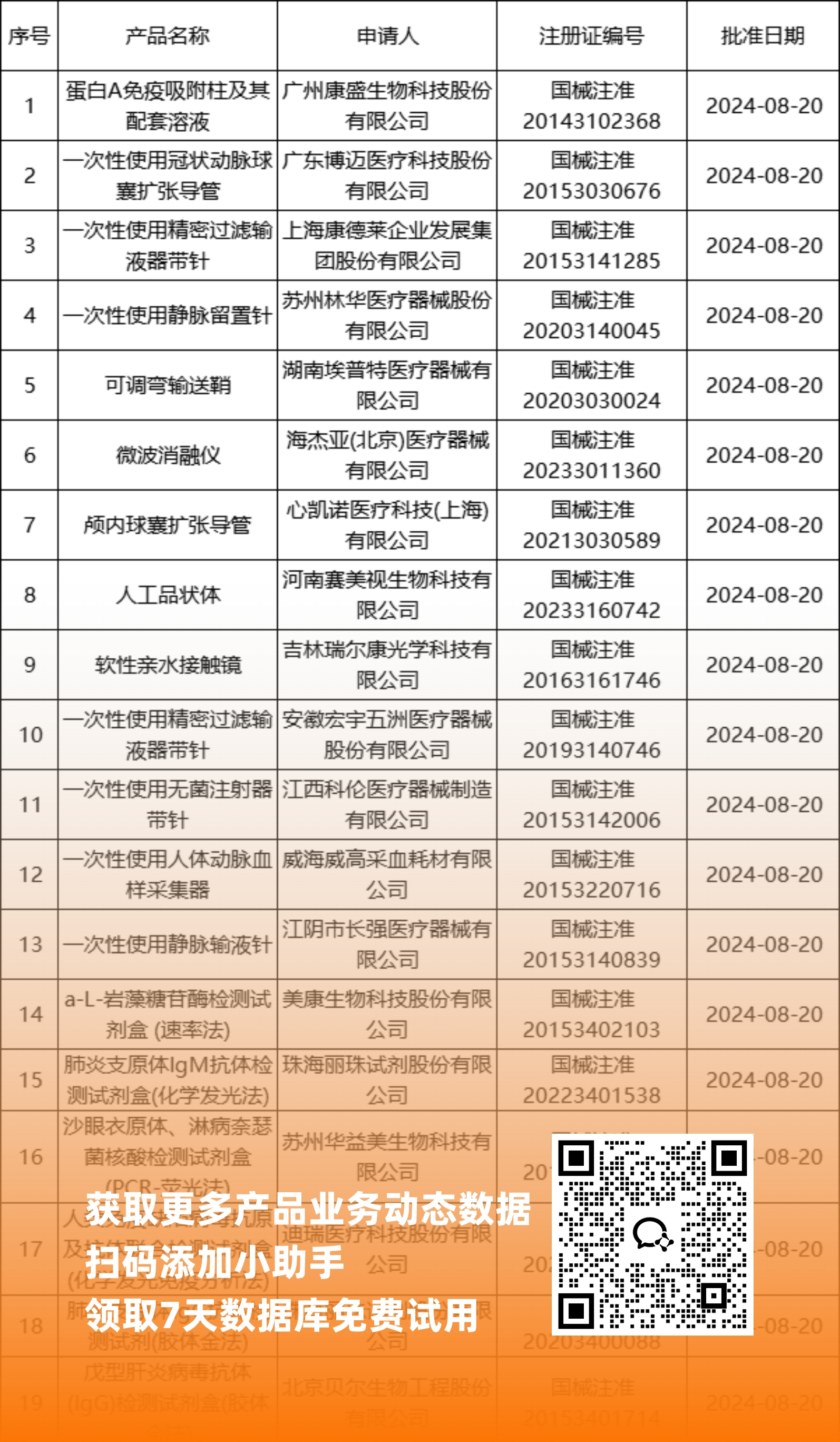
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉橙仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。
扫码添加小助手,立刻领取7天数据库免费试用
动脉橙产业智库,助力追踪数字健康、医疗器械、生物医药领域行业动态,覆盖公司名单、招投标、投融资信息、头部企业动态等各类数据,九大维度实时更新,欢迎扫码添加小助手,免费申请7天试用福利👇