
商务合作

动脉网APP
2024年9月6日至9月12日,动脉橙产业智库重点整理了医疗器械产品国内外获批资讯及数据,涉及10个器械获FDA批准,4个器械获欧盟及其他批准,两个器械获NMPA创新产品批准,另有341个器械获NMPA批准注册文件。
海外获批
一、FDA
1. 美国食品药品监督管理局批准首款与苹果AirPods Pro兼容的OTC助听器软件
FDA已批准第一款非处方助听器软件Hearing Aid Feature(HAF)与兼容的Apple AirPods Pro配合使用。该软件专为18岁及以上的轻度至中度听力障碍患者设计,通过根据用户需求定制,将AirPods Pro转换为助听器。美国食品和药物管理局预计,这将改善人们获得负担得起的听力解决方案的机会。HAF使用自适配策略,可通过iOS设备进行调整,并与iOS HealthKit集成,提供量身定制的听力体验。
2. 友康生物旗下间充质干细胞无血清培养基获FDA批准
2024年9月7日获悉,友康生物的间充质干细胞无血清培养套装成功获得了美国FDA的510(K)二类医疗器械注册证,510(K)号K232543。友康生物2018年在中国市场上推出该产品,并同步启动该产品在美国市场的注册工作。申请期间,友康生物递交了包括可沥滤物研究、急性全身毒性研究、白兔皮内反应性试验、皮肤致敏研究、白兔热原试验、体外细胞毒性试验、无菌试验等几十项干细胞培养基相关检测报告,其间充质干细胞无血清培养基均通过了以上技术检测。
3. 医学影像分析公司Nanox.AI升级版心脏评估解决方案获FDA批准
Nanox.AI是NANO-X imaging Ltd.的深度学习医学成像分析子公司,其升级的心脏评估解决方案HealthCCSng V2.0已获得FDA 510(k)许可。该技术可识别冠心病高危患者,并与现有医疗系统集成。它使用常规CT扫描来测量冠状动脉钙,这是未来心血管事件的关键预测指标。设备输出可供放射科医生和其他医学专业人员进行进一步的临床评估。
4. Illumina旗下IVD生物标志物测试成为首个FDA批准的泛癌症伴随诊断试剂盒
2024年9月11日获悉,基因测序领域的领导者Illumina旗下TruSight Oncology (TSO) Comprehensive体外诊断生物标志物检测试剂盒于8月下旬获得FDA批准。TSO Comprehensive是FDA批准的第一个可分发的具有泛癌症伴随诊断声明的全面基因组分析IVD试剂盒,可以检测近30种实体肿瘤类型的517个基因的变异,从而能够识别癌症患者的生物标志物,并帮助医师为患者匹配合适类型的靶向药物。
5. 泌尿外科手术机器人开发商PROCEPT BioRobotics宣布HYDROS机器人系统获FDA批准上市
PROCEPT BioRobotics的HYDROS机器人系统已获得FDA批准,这标志着该公司的一个重要里程碑。HYDROS利用了来自50000多个程序的见解,引入了技术进步,例如FirstAssist AI治疗计划,高级图像引导,机器人切除和简化的工作流程。它旨在提高效率,增强外科医生和工作人员的经验,并提供更准确和一致的治疗计划,以获得更好的临床结果。
6. 临床超声公司Sonic Incytes宣布Velacur®脂肪测定分数获FDA 510(k)许可
Sonic Incytes Medical Corp宣布,FDA已批准其Velacur®Determined Fat Fraction(VDFF)510(k)许可,这是一种集成到Velacur®设备软件中的创新测量工具。这种新工具在护理方面提供了与MRI-PDFF类似的临床实用性,可能会改变肝脏脂肪变性的管理。随着最近FDA批准了第一种MASH治疗剂,以及AASLD建议将肝脏超声作为二次筛查,VDFF迎来了解决MASLD和MASH现有非侵入性诊断方法局限性的关键时刻。
7. Think Surgical旗下TMINI系统和Zimmer Biomet旗下Persona系统配合使用,获FDA 510(k)认证
骨科机器人开发商Think Surgical宣布,其微型手术机器人TMINI系统与骨科巨头Zimmer Biomet(NYSE:ZBH)的个性化膝关节系统Persona的配合使用获得了FDA 510(k)认证。Think Surgical的膝关节置换系统专门版本旨在与 Zimmer Biomet 的植入物配对。FDA批准了上述两种系统一起使用,标志着Think Surgical成为唯一一家提供既能与Persona膝关节系统独家配合使用,又能以开放平台使用多家制造商的植入物进行全膝关节置换的机器人系统的公司。
8. 医疗设备研发商Femasys创新诊断解决方案FemChec获FDA 510(k)批准,用于输卵管诊断
生物医学公司Femasys, Inc.已获得FDA 510(k)对FemChec的许可,FemChec是一种创新的诊断工具,用于控制对比剂的输送以确认输卵管状态。FemChec也是FemBloc非手术永久性节育管理后确认测试的一部分,该管理处于后期试验阶段。
9. 互联健康技术公司Withings宣布Sleep Rx睡眠呼吸暂停设备获FDA批准
Withings是互联健康领域的领导者,它宣布其用于睡眠呼吸暂停的睡眠接收设备已获得FDA的批准。Sleep Rx为传统的实验室测试提供了一种方便而准确的替代方案,解决了睡眠呼吸暂停的普遍诊断不足问题。该设备是非侵入性的,适合任何床垫下,并提供睡眠、呼吸和心血管活动的综合分析。它经过临床验证可用于诊断睡眠呼吸暂停,易于使用,并可以改善诊断。通过睡眠Rx进行早期诊断和治疗可以带来更好的健康结果。
10. 介入心脏病学医疗器械公司Restore Medical颠覆性心血管介入新品获批FDA
Restore Medical公司的ContraBand™设备获FDA突破性设备认定,用于治疗射血分数降低的心衰患者,可改善生活质量和血流动力学功能。该设备是首个专为这类患者设计的经导管肺动脉束带系统,已通过初步临床试验验证其安全性与有效性,并有望改变充血性心衰的治疗方式。
二、欧盟及其它
1. 数字医疗保健公司iRhythm宣布Zio心电图监护系统获日本PMDA批准
iRhythm Technologies, Inc.宣布其使用人工智能进行心律失常监测的Zio ECG监测系统已获得日本药品和医疗器械管理局的批准。该系统包括佩戴长达14天的贴片心电图设备和报告软件。
2. 手术机器人公司Medicaroid旗下hinotori手术机器人系统在马来西亚获批
日本Medicaroid公司的hinotori手术机器人系统获马来西亚批准,此前已在日本、新加坡获批并完成远程手术演示,适用于泌尿、胃肠、妇科及胸外科手术,具有开放操作空间、减少干扰等特点。
3. 拜耳宣布阿柏西普8mg预充式注射器获欧盟批准上市
2024年9月9日,拜耳宣布欧洲药品管理局(EMA)在欧盟批准预充式注射器用于Eylea™ 8mg(114.3mg/ml注射液)的给药。新的预充式注射器OcuClick™将为眼科医生提供一种高效便携的方法,精准给药70微升剂量的Eylea 8mg,用于治疗新生血管(湿性)年龄相关性黄斑变性(nAMD)和糖尿病性黄斑水肿(DME)。
4. 中日欧三地获批,艾德生物创新产品助力肺癌精准诊疗
艾德生物PCR-11基因伴随诊断试剂盒获中日欧批准,成为肺癌靶向治疗的重要检测选择。其卓越性能在多项临床研究中得到验证,具有高检测成功率、阳性率和快速出报告等优势,满足初诊初治肺癌患者需求。
国内获批
一、创新器械获批
心脏脉冲电场消融仪和一次性使用心脏脉冲电场消融导管获批上市
2024年9月10日,国家药品监督管理局批准了美敦力公司“心脏脉冲电场消融仪”和“一次性使用心脏脉冲电场消融导管”两个创新产品注册申请。
心脏脉冲电场消融仪由发生器、控制器(可选)、脚踏开关(可选)、EGM线缆、一次性使用导管接口线缆组成。一次性使用心脏脉冲电场消融导管由电极、管身和手柄组成。
上述两个产品配套使用,利用脉冲电场的非热效应原理,治疗药物难治性、复发性、症状性阵发性房颤或药物难治性、复发性、症状性持续性房颤(发作持续时间小于1年)。与传统的射频消融及冷冻消融产品相比,该产品可实现对心肌组织的选择性破坏,避免温度传递导致的周围组织损伤风险。
二、NMPA最新获批器械产品明细
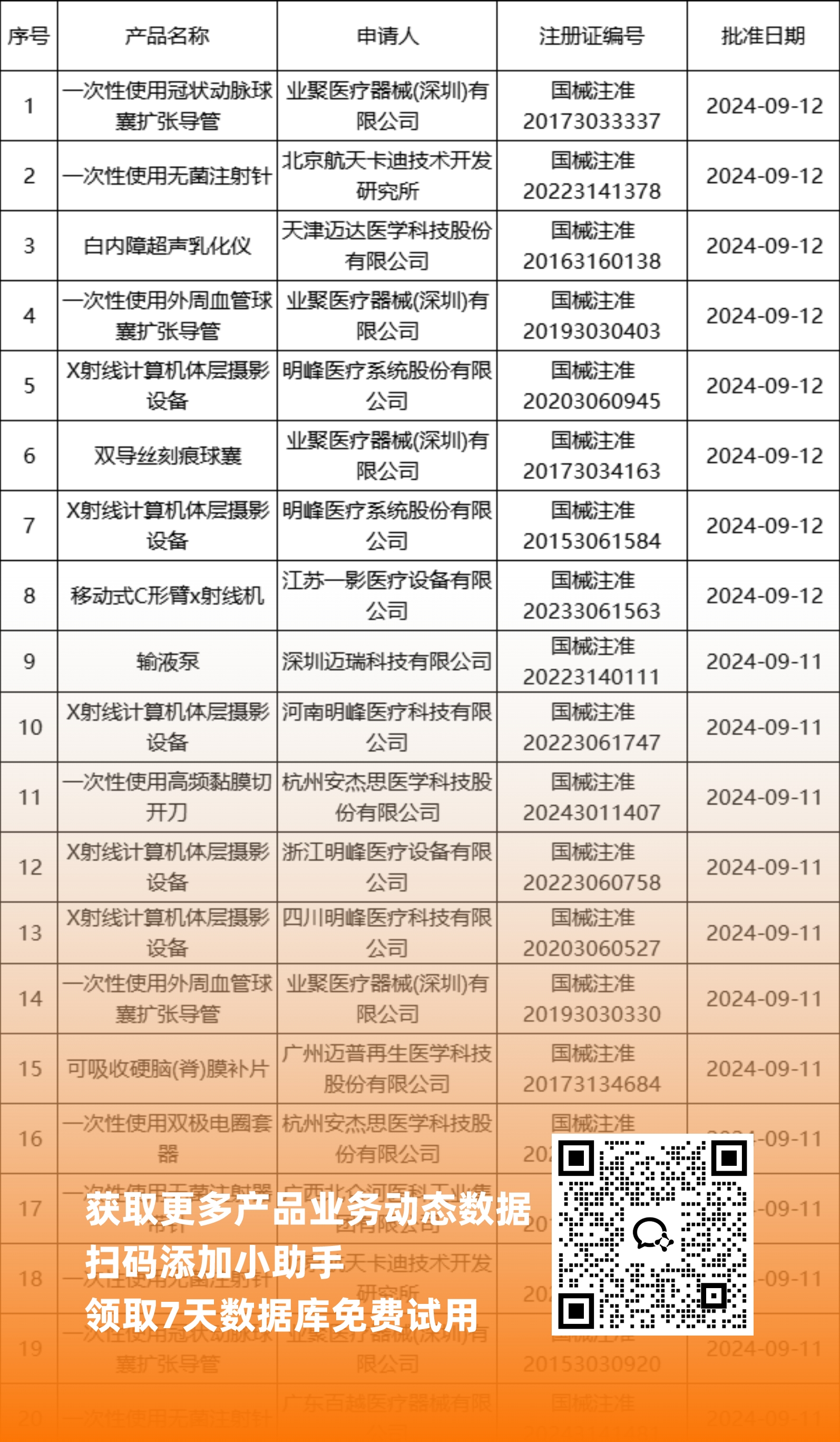
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉橙仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。
国科恒泰与动脉网携手打造爱经销模式推广会暨渠道交流会,满足医疗器械生产企业与经销商之间对接需求,同步在成都、太原、杭州、西安等地举办线下专场,点击图片立刻对接↓