
商务合作

动脉网APP
2024年11月22日至11月28日,动脉橙产业智库重点整理了医疗器械产品国内外获批资讯及数据,涉及7个器械获FDA批准,两个器械获欧盟及其它批准,两个器械获NMPA创新产品批准,另有556个器械获NMPA批准注册文件。
海外获批
一、FDA
1. 首款,医疗设备公司S4 medical电生理消融食管保护装置获FDA批准上市
S4 Medical的esolution获FDA批准,作为首款预防电生理消融中食管损伤的设备。通过临床研究验证,该产品可显著降低食管热损伤发生率,提高消融手术安全性,并有望与新技术HPSD结合,进一步提升治疗效果。
2. 皮肤美容公司Novoxel宣布Tixel设备获FDA批准 ,用于睑板腺功能障碍治疗
Novoxel的Tixel设备已获得FDA批准,用于治疗由睑板腺功能障碍(MGD)引起的蒸发性干眼症。它使用适用于所有肤色的热机械作用(TMA)技术,通过局部热量和压力改善眼睛润滑。优点包括无麻醉,偶联凝胶或明亮的闪光,简单和安全。一项临床研究显示出显着的益处,包括改善泪液破裂时间,睑板腺评分和减轻症状。
3. 脑机接口系统开发商Neuralink BCI控制辅助机械臂临床获FDA批准
Neuralink获得FDA批准,启动新的可行性试验,评估使用其N1 BCI植入物控制研究性辅助机械臂。该植入物可让患者用思想控制计算机或移动设备,并已通过首次人体植入测试。
4. LifeSignals的可穿戴生物传感器获得FDA批准
总部位于加利福尼亚州的医疗技术公司LifeSignals的可穿戴生物传感器已获得FDA批准,其用于连续无线远程患者监测的UbiqVue 2A多参数系统。佩戴在胸部的生物传感器收集13个生理参数的数据,包括SpO₂水平,脉搏,呼吸频率,PPG和体温。数据经过加密并安全传输到基于云的系统,由医疗保健专业人员通过门户网站访问。
5. 比格威医疗BVD6600系列干眼检测仪获批FDA
2024年11月25日获悉,比格威医疗自主研发的BVD6600系列干眼检测仪成功获批美国食品药品监督管理局(FDA)注册证。这一成就标志着该产品正式迈入了国际医疗市场的大门,同时也彰显了“中国制造”在全球医疗科技领域的卓越实力和创新精神。BVD6600是一款采用大盘Placido环方案的干眼检查设备,操作便捷友好,可为患者进行泪河高度、泪膜破裂时间、脸板腺、脸缘、眼红、脂质层、角膜染色等全面检查,采用先进算法实现精准量化分析,为临床干眼症的检查诊断提供客观的检查结果。产品特点:覆盖范围广、AI分析功能、功能全面、报告通俗易懂、内置问卷、云平台架构、长期跟踪随访。
6. 医疗器械研发生产商Zimmer Biomet宣布Oxford®无骨水泥部分膝关节获得FDA批准
Zimmer Biomet Holdings, Inc.宣布,美国食品和药物管理局(FDA)已批准Oxford®非骨水泥部分膝关节的上市前批准申请(PMA)补充批准。该批准得到了研究设备豁免(IDE)研究和非临床测试的安全性和有效性数据的支持。与骨水泥型相比,Oxford无骨水泥部分膝关节提供了更好的固定效果,更好的长期植入物存活率,并提高了手术室的效率。凭借20多年的临床经验和全球30多万次手术,它现在是美国唯一一种FDA批准的非骨水泥部分膝关节植入物。
7. 美敦力最新一代糖尿病系统获得FDA批准
美敦力推出新Smart MDI糖尿病管理系统,包括InPen智能胰岛素笔、InPen应用程序和Simplera连续血糖监测仪,已获FDA批准。此外,美敦力与雅培合作开发新CGM技术,以改善糖尿病患者护理。
二、欧盟及其它
1. 心通医疗VitaFlow Liberty®在韩国获批上市,带来“中国智造”之选
心通医疗的VitaFlow Liberty®作为全球唯一电动可回收TAVI系统,在韩国获批上市,展示科技创新实力,有望重塑当地市场,造福更多心脏病患者。该产品已进入20个国家和地区,治疗超万名患者。
2. 微创脑科学四款重要产品在墨西哥获批上市,开启出海新旅程
微创脑科学旗下四款神经介入产品在墨西哥获批上市,覆盖出血性和急性缺血性卒中关键领域,将惠及当地脑血管病患者。
国内获批
一、创新器械获批
1. 陡脉冲治疗设备和一次性使用陡脉冲消融针创新产品获批上市
2024年11月27日,国家药品监督管理局批准了杭州睿笛生物科技有限公司的陡脉冲治疗设备和一次性使用陡脉冲消融针2个创新产品注册申请。陡脉冲治疗设备由主机、电动悬臂机构、脚踏开关组成,与一次性使用陡脉冲消融针及连接线组配套使用。陡脉冲治疗设备采用纳秒高压脉冲电场发生装置,利用线性调制技术,通过脉冲成形网络存储能量并形成脉冲,具有电场强度高、脉宽短的特性,属于国内首创。通过非热消融技术,使消融针经皮穿刺作用于靶区,产生高压脉冲电场,使细胞产生不可逆的穿孔效应、快速凋亡,实现肝脏恶性实体肿瘤消融。该技术属于微创介入类肿瘤治疗的新技术,对于改善患者生活质量、提高患者生存率具有重要意义。
2. 超声诊断系统创新产品获批上市
2024年11月27日,国家药品监督管理局批准了深圳迈瑞生物医疗电子股份有限公司的超声诊断系统创新产品注册申请。该产品由主机、探头和选配件组成,在线阵探头基础上同步输出近红外激光,使被测组织受热膨胀产生特定频率的超声信号,并将其强度和特征转化为图像显示,获得被测区域组织中血氧分布情况,用于临床超声和光声诊断检查。该产品为国内首个融合超声和光声成像技术的双模态成像产品,可在一个成像周期内,同时显示超声组织结构图像和光声图像,为医生诊断患者病情提供更丰富的组织结构和功能信息。
二、NMPA最新获批器械产品明细
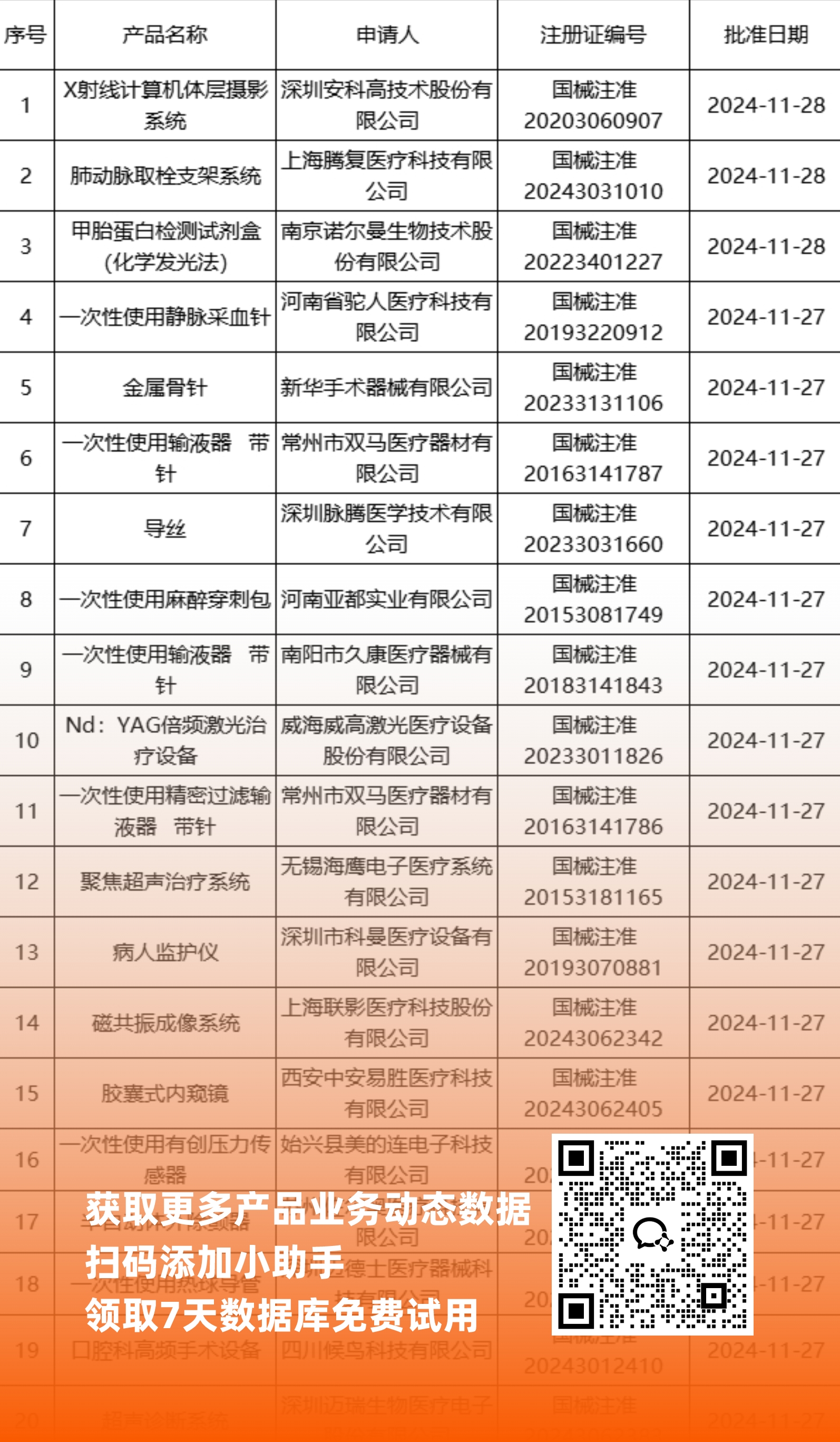
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉橙仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。
————🔓点击图片,解锁【手术导航系统】资源对接专场————