
商务合作

动脉网APP
2025年5月2日至5月8日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及4个器械获FDA批准,2个器械获欧盟及其它批准,另有299个器械获NMPA批准注册文件。
海外获批
一、FDA
1. GE医疗,全球首款获批
GE医疗推出新一代核医学成像系统Aurora及深度学习重建技术Clarify DL,获FDA认证,标志着核医学向精准诊疗与效率提升迈进,为疾病管理提供新方案。
2. AI加持的可穿戴心律转复除颤器获FDA批准
加州医疗技术公司Element Science研发的Jewel Patch可穿戴心律转复除颤器获FDA批准,将助力全球心脏性猝死防治。
3. 心脏医学新突破:FDA批准首个无症状主狭TAVR瓣膜
FDA批准Edwards Lifesciences的TAVR瓣膜用于治疗无症状的严重主动脉瓣狭窄,为心脏病患者带来新希望。
4. 眼科设备开发商OcuSciences视网膜健康扫描仪获FDA批准
2025年5月2日获悉,美国食品药品监督管理局(FDA)已批准OcuSciences的视网膜健康评估设备OcuMet Beacon。该非侵入式设备适用于检眼镜扫描,用于视网膜的红外和自发荧光成像,无论是否使用散瞳剂。OcuMet测量黄素蛋白荧光(FPF)可作为青光眼等视网膜疾病中线粒体功能障碍的生物标志物。据该公司介绍,使用该设备扫描通常在几分钟内完成,内置屏幕会在完成后提供分析结果。在获得FDA批准之前,OcuMet已接受过多项评估。纽约西奈山医院的一项研究发现,青光眼患者的FPF显著高于正常眼,尤其是在早期青光眼病例中,因为早期青光眼的损伤通常难以察觉。早期发现青光眼被认为是最大限度地提高患者治疗效果的关键。
二、欧盟及其它
1. Merit Medical宣布加拿大卫生部批准 WRAPSODY®细胞不可渗透性内假体装置
全球医疗技术领导者麦瑞通医疗系统公司宣布,其Wrapsody细胞不可渗透性内假体(CIE)已获得加拿大卫生部的监管批准。该公司计划立即通过其位于多伦多的分销中心开始在加拿大全面推广该设备。WRAPSODY CIE旨在解决狭窄问题,这是透析患者常见且可能危及生命的并发症。它采用独特的三层设计,这一设计源于麦瑞通对以往设备失败原因的调查,发现PTFE层内的组织侵入是一个重要因素。
2. 威高介入金属药物支架系统正式获得俄罗斯医疗器械注册证
威高介入旗下公司金属药物支架系统获得俄罗斯医疗器械注册证,标志国际认可,助力开拓欧亚市场,彰显公司创新与质量实力,及服务全球医疗决心。
国内获批
NMPA最新获批器械产品明细
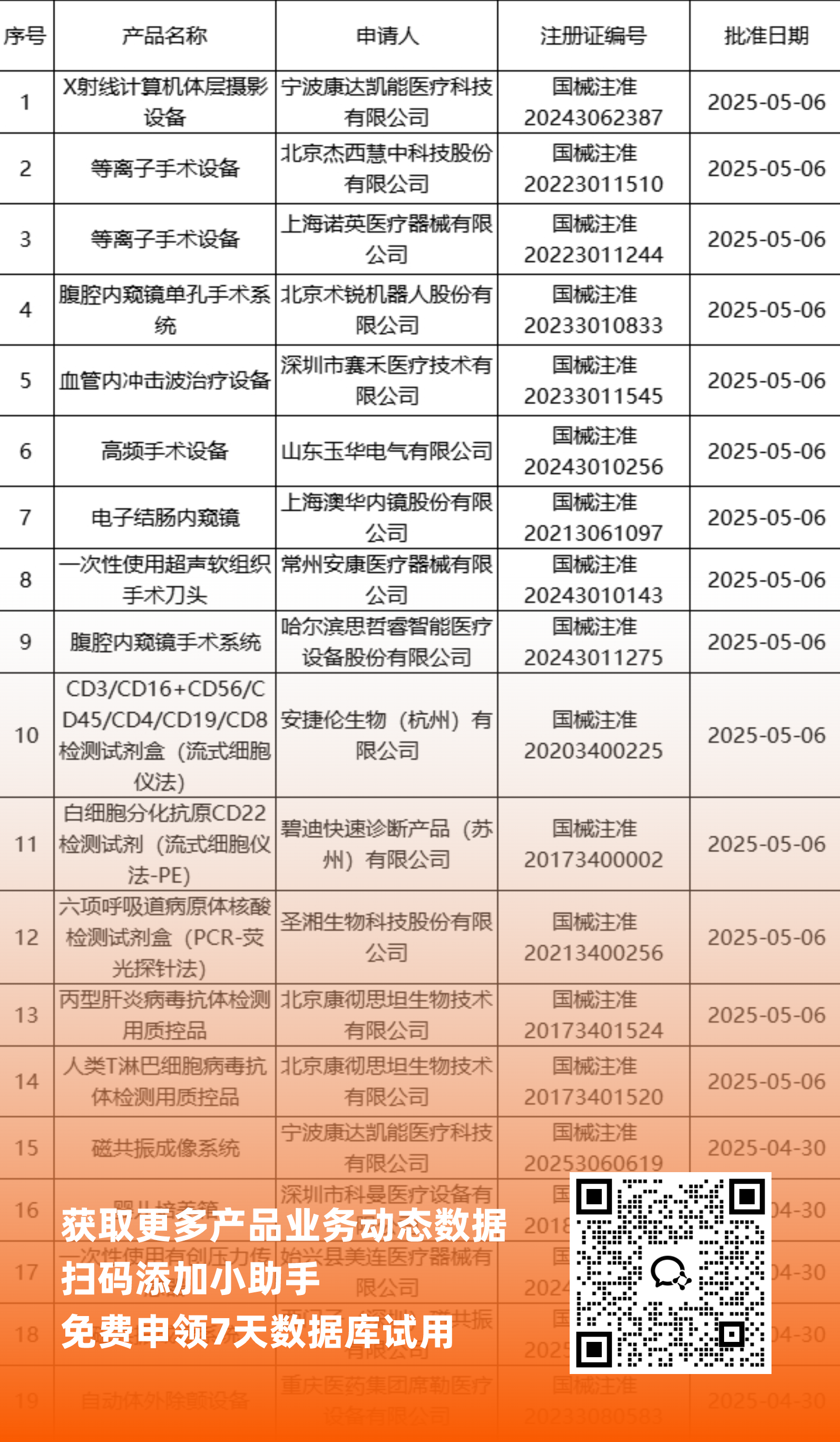
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。