
商务合作

动脉网APP
2025年7月11日至7月17日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及11个器械获FDA批准,1个器械获欧盟及其它批准,另有416个器械获NMPA批准注册文件。
海外获批
一、FDA
1. Fasikl腕带获得FDA许可,全球首个且唯一用于治疗特发性震颤的AI赋能设备
Fasikl公司开发的Felix NeuroAI腕带获FDA许可,成为全球首个治疗特发性震颤的AI设备。该设备通过AI动态调节神经信号,可显著改善患者日常活动能力,为药物或手术无效者提供新选择。FDA的许可是基于有力数据支持,显示其显著减轻震颤并改善用户日常活动能力。
2. FDA重磅批准全球首个用于经导管手术AI,心脏手术进入“AI导航”时代
FDA批准Caranx Medical的AI软件TAVIPILOT Soft用于经导管心脏瓣膜植入实时引导,提高手术精度与成功率,降低并发症风险,助力心脏病治疗进入“AI导航”新时代。
3. 精准医疗技术研究商Tempus AI射血分数软件获FDA 510(k)许可
美国食品药品监督管理局(FDA)已授予Tempus AI公司的ECG-Low EF软件510(k)许可,该软件利用人工智能检测左心室射血分数(LVEF)较低的个体。这款软件是该公司一系列旨在识别各类心血管疾病高危患者的心电图-AI设备中的最新成员。Tempus的ECG-AI解决方案与现有的心电图平台和电子健康记录(EHR)集成,将AI洞察直接嵌入临床工作流程。其EF模型基于超过93万份心电图和逾17万名个体的数据进行训练。对于通过Tempus的ECG-Low EF检测呈阳性的个体,在进行超声心动图评估时,近五分之二的患者会被确认为LVEF低于或等于40%。
4. 医疗技术开发商RIVANNA下一代超声引导平台和人工智能驱动的成像软件获得FDA 510(k)许可
RIVANNA®是一家基于成像的医疗技术开发商,其Accuro® 3S诊断超声系统和SpineNav-AI™图像处理软件已获得FDA 510(k)许可。Accuro 3S是一款便携式超声系统,配备Dual-Array™凸形探头,可优化解剖结构可视化,并支持标准B模式成像。SpineNav-AI是一款基于机器学习的软件,用于辅助腰椎肌肉骨骼成像评估,提供自动化的关键脊柱解剖标志检测与识别。此项许可允许这两项技术在美国医院和临床环境中用于针头或导管放置期间的解剖引导。
5. 微创手术技术公司Arthrex NanoScope™系统获得骨科、腹腔镜手术的儿科许可
Arthrex是一家微创手术技术的领导者,其NanoScope手术关节镜系统已获得FDA批准,可用于儿科骨科和腹腔镜手术。NanoScope系统配备高分辨率移动成像平台,拥有一个独特的高清尖端芯片摄像头,称为NanoNeedle Scope,专为满足儿科患者的解剖和手术需求而设计。这项技术正在改变诊断和最小侵入性手术治疗方式,其扩展适应症至儿科骨科和腹腔镜领域被视为一项重大进步。该系统可用于常见的儿科病例,如普通膝关节镜检查、半月板治疗、前交叉韧带重建、普通肩关节镜检查以及疝气或诊断性腹腔镜手术。
6. Piccolo Medical公司获得FDA对其第二代SmartPICC®技术的批准
Piccolo Medical, Inc.是血管通路技术的领导者,已获得美国食品药品监督管理局(FDA)批准,可将其下一代SmartPICC®导丝和PM2+™系统投入市场。这标志着在外周插入中心静脉导管(PICC)的安全性、效率和成本效益方面取得了重大进展,使患者和医疗服务提供者均能受益。SmartPICC®技术利用患者的心脏电活动,在床旁实时准确确认导管尖端位置,无需进行确认性胸部X光检查,从而简化了PICC确认流程。该技术还采用离子稀释技术,在导管插入过程中提供实时引导。Piccolo Medical首席执行官Augustus Shanahan表示,该技术在优先考虑患者安全的同时,也缓解了医疗系统的经济负担。
7. LibAirty:能治疗慢性肺病的“背心”获FDA批准上市
LibAirty,一种新型气道清除系统,获FDA批准上市,可治疗慢性肺病。该系统结合可控呼吸与精准胸压,通过APP引导和可穿戴背心实现深度气道清除,简便有效,可居家使用,每天短时治疗即可提高患者生活质量。
8. 血压监测革新,首款FDA批准无袖带血压计来袭
首款FDA批准的无袖带血压计Hilo Band,运用PPG技术和CALFREE算法实现精准测量,可自动化高频测量并实时呈现数据,获权威认可。
9. 强生PFA新技术获FDA批准
强生宣布FDA批准其VARIPULSE的灌溉流量升级方案。这项技术升级新体现了强生在真实临床实践基础上推动PFA技术创新的承诺。最近强生在PFA领域取得一系列进展,除了这次新技术获FDA批准外。其本月在亚太地区推出VARIPULSE消融平台,以及任命新首席医疗科学官。这些进展都将快速推动强生在PFA领域布局,在加上强生深厚电生理基础,将加速追赶波科和美敦力步伐,从而大大提高未来反超几率。
10. FDA批准InspireMD的CGuard Prime为首款获得CMS覆盖的网状覆膜颈动脉支架
美国食品药品监督管理局(FDA)已批准InspireMD的CGuard Prime,这是一种用于预防中风的网状覆盖颈动脉支架。这是首个获得FDA批准的此类设备,据报道在类似技术试验中具有最低的不良事件发生率。美国医疗保险和医疗补助服务中心(CMS)还扩大了对该设备的覆盖范围。CGuard Prime提供了比传统开放手术侵入性更小的替代方案,并旨在减少支架置入过程中的并发症。随着CMS的覆盖,预计该技术将在符合条件的患者中得到更广泛的采用。
11. 直觉医疗Vessel Sealer Curved用于达芬奇系统获FDA批准
美国食品药品监督管理局 (FDA) 已批准 Intuitive 公司的 Vessel Sealer Curved,这是一种与公司达芬奇手术系统兼容的高级能量器械。这是该公司首个获批用于淋巴管切断的器械。这款全腕式双极电外科工具设计多功能且精准,具有弯曲、纤细的钳口,可在狭窄区域提升可视性和控制力。其批准的用途包括组织分离、双极凝固以及直径不超过 7 毫米的血管、淋巴管和组织束的机械切断。
二、欧盟及其它
1. LigaSure RAS:美敦力机器人版本大血管闭合器获CE批准上市
美敦力推出机器人版大血管闭合器LigaSure RAS,获CE批准上市,可与Hugo手术机器人配合,提升手术精准度与患者安全性,已在全球广泛应用。
国内获批
NMPA最新获批器械产品明细
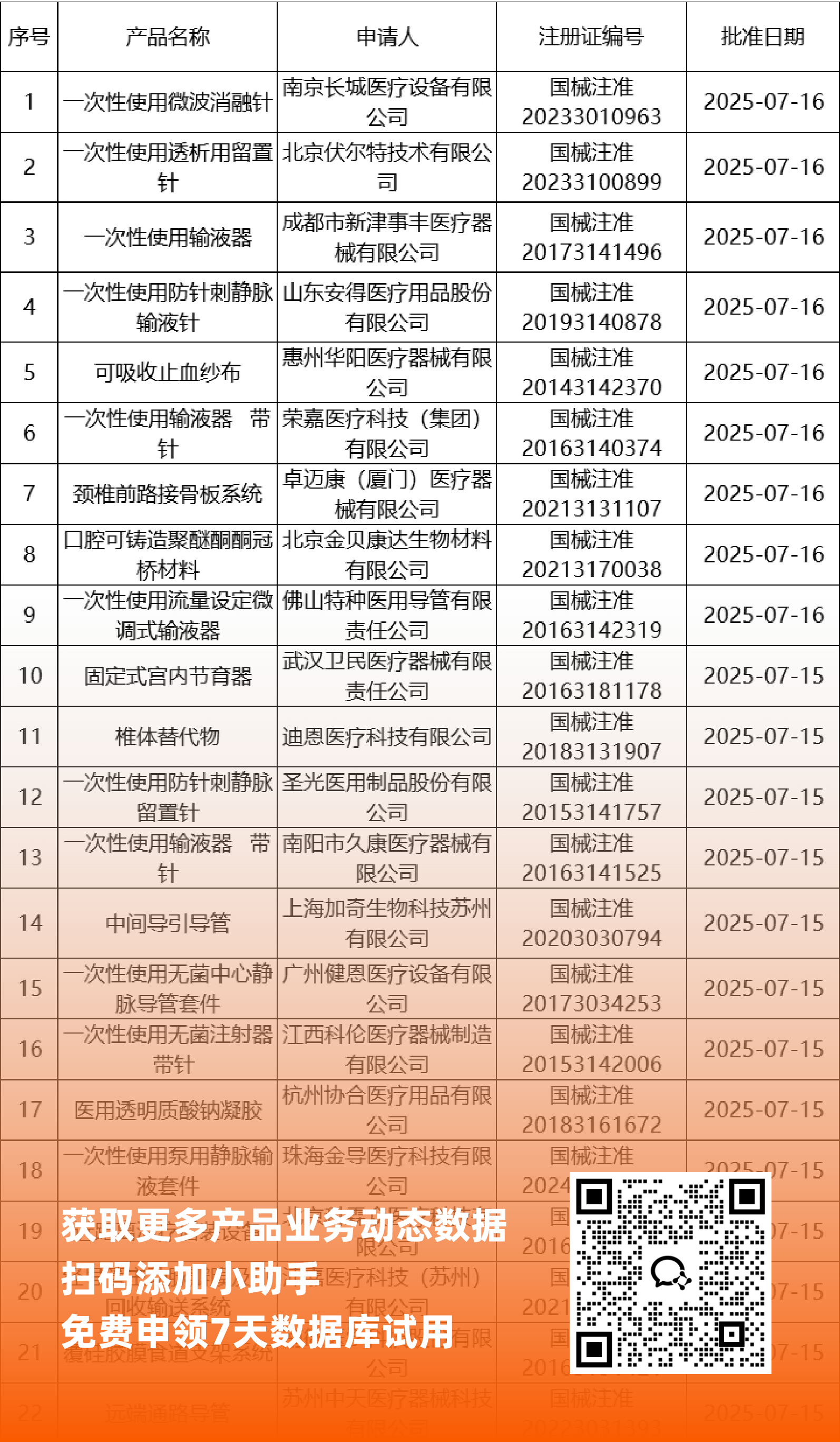
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。