
商务合作

动脉网APP
2025年7月18日至7月24日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及4个器械获FDA批准,2个器械获欧盟及其它批准,1个器械获NMPA创新产品批准,另有409个器械获NMPA批准注册文件。
海外获批
一、FDA
1. Minnesota Medical Technologies宣布其大便失禁设备获得FDA 510(k)许可
2025年7月24日,Minnesota Medical Technologies宣布其粪便失禁装置“StaySure™”获得了FDA 510(k)许可。这款一次性、易于使用且可自行插入的装置在管理粪便失禁和意外肠漏方面是一项重大进步,其采用100%硅胶材质和内置液体,提供了适应性和舒适性。首席执行官大卫·A·乔纳斯对美国监管许可表示兴奋,并赞扬了产品开发和法规事务团队。StaySure™为美国数百万患有这些病症的人群提供了一个实用而有效的解决方案。该装置自2021年起已在欧洲上市,并经过临床验证,安全有效。
2. FDA批准飞利浦的前列腺癌影像引导导航系统
美国食品药品监督管理局 (FDA) 已批准飞利浦最新的 UroNav 版本,该版本推动了前列腺癌治疗的影像引导导航技术。UroNav 将术前 MRI 与实时术中超声结合,提高了操作的精确性,并为目标区域提供了全面的视图。它同时支持经直肠和经会阴活检方法,使临床医生可以选择其偏好的方式。UroNav 还有助于局部治疗程序,提供一种微创的护理方法,并促进以 3D 形式审查活检目标和核心样本。
3. 首款生物降解胆胰支架获FDA批准上市
ARCHIMEDES成为首款获FDA批准的生物降解胆胰支架,其双引流系统设计可减少并发症,简化引流操作,有快速、中速、慢速降解三种型号,由Q3 Medical推出。
4. FDA 认证落定 | 霆升科技开启国产心腔内超声全球征程
霆升科技自主研发的心腔内超声诊断系统成功通过FDA审批,打破国际垄断,进军全球市场,展现中国医疗科技创新实力。
二、欧盟及其它
1. 奥精医疗OssaNova™人工骨修复材料在越南获得注册证
奥精医疗发布公告,公司于2024年12月向越南卫生部递交了公司人工骨修复材料的注册申报资料。公司于近日收到越南卫生部通知,公司人工骨修复材料获得批准。本次获得越南注册证的OssaNova™人工骨修复材料是基于奥精医疗具有完全自主知识产权的体外仿生矿化技术研发和生产的一种仿生矿化胶原人工骨修复材料,在组成成分和微观结构上均对人体天然骨组织高度仿生。
2. 威高介入金属药物支架系统正式获得俄罗斯医疗器械注册证
威高介入旗下公司自主研发的金属药物支架系统获得俄罗斯医疗器械注册证,标志国际认可,助力开拓欧亚市场,彰显公司创新、质量实力及全球服务决心。
国内获批
一、创新器械获批
1. 雷帕霉素药物洗脱冠状动脉支架系统获批上市
2025年7月18日,国家药品监督管理局批准了中科益安医疗科技(北京)股份有限公司雷帕霉素药物洗脱冠状动脉支架系统创新产品注册申请。该产品由预装的药物支架和快速交换型球囊扩张导管输送系统组成。金属支架由高氮无镍不锈钢制成,药物涂层由雷帕霉素和乙交酯丙交酯共聚物(PLGA)组成,药物剂量为100μg/cm。输送系统由尖端、球囊、显影标记、远端内管、远端导管、过渡导管、近端导管、抗变形段、导管座和亲水涂层组成。 该产品适用于冠脉原发病变引致的缺血性心脏病患者,用以改善冠状动脉腔内直径,病变长度小于30mm,参考血管直径为2.5-4.0mm。
二、NMPA最新获批器械产品明细
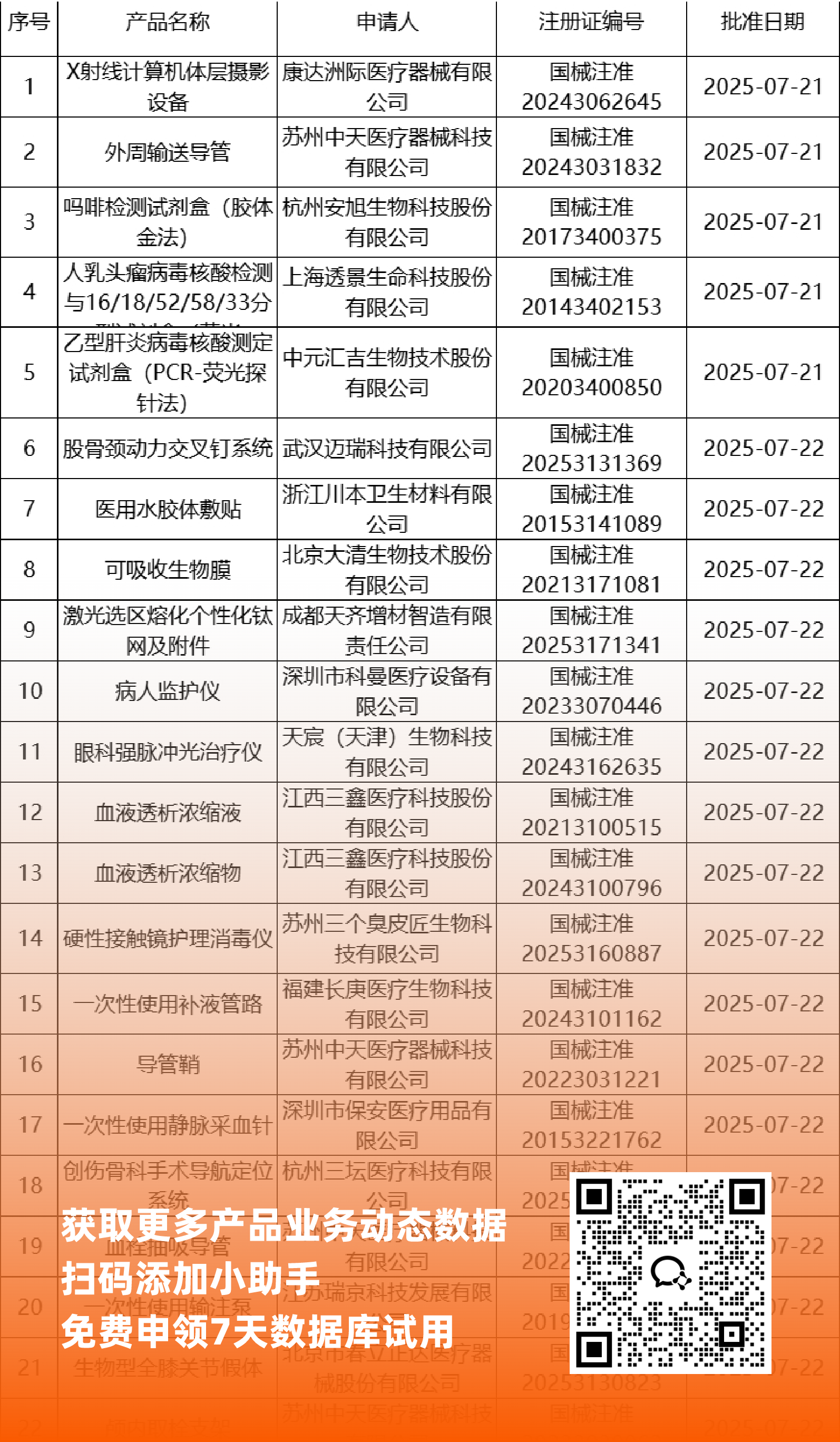
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。