
商务合作

动脉网APP
2025年8月1日至8月7日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及7个器械获FDA批准,2个器械获欧盟及其它批准,1个器械获NMPA创新产品批准,另有408个器械获NMPA批准注册文件。
海外获批
一、FDA
1. 可吸收栓塞剂开发商Instylla旗舰产品Embrace™水凝胶栓塞系统获得美国FDA上市前批准
Instylla公司宣布其旗舰产品Embrace™水凝胶栓塞系统获得FDA批准,用于外周动脉≤5mm的富血管性肿瘤的栓塞治疗。富血管性肿瘤常见于多个器官,具有异常增多的血管,通常与较低的存活率相关。其高血管性因出血风险而给手术带来挑战。Embrace HES由两种低粘度液态前体组成,在栓塞过程中能够血管内交联,为患者提供了新的治疗选择。
2. RadNet子公司DeepHealth的远程扫描解决方案 TechLive™获美国食品药品监督管理局(FDA)批准
RadNet全资子公司DeepHealth宣布,已获得 FDA 510(k) 批准的 TechLive™,这是一种远程扫描解决方案,可实现对磁共振(MR)、计算机断层扫描(CT)、正电子发射断层扫描(PET/CT)和超声波程序的集中操作和监督。TechLive™ 通过使技术人员能够同时为多个地点进行扫描,解决了放射技术员短缺的问题,提高了运营效率,延长了工作时间,并增强了对复杂程序的访问能力。目前,RadNet 的 300 多台影像系统已经连接到该解决方案,通过实时远程匹配专家人员与复杂设备,进一步提升了患者通量和检查质量。
3. BD高通量性病分子检测试剂获批
美国FDA批准BD公司的高通量性病分子检测试剂BD CTGCTV2在BD COR平台运行,可检测沙眼衣原体、淋病奈瑟菌和阴道毛滴虫DNA,适用于多种样本类型,提高检测效率。
4. 首款“三合一”无创心脏监测获批FDA
Cardiosense的“三合一”无创心脏监测设备CardioTag获FDA认证,可同时采集ECG、PPG和SCG三种心脏生理信号,为医生提供更立体、精确的心功能评估,并计划通过AI算法预测心血管风险。此外,Cardiosense 还计划基于 CardioTag 采集的数据,部署 AI 算法,预测心血管事件风险、优化药物疗效评估,并实现远程动态管理。
5. FDA批准首个用于类风湿关节炎的迷走神经刺激装置:难治性疾病的新希望
FDA批准SetPoint Medical的迷走神经刺激装置用于治疗难治性类风湿关节炎,该装置利用迷走神经的抗炎特性,为自身免疫疾病提供新的非药物治疗选项。临床试验显示,该装置可显著改善患者症状并减少药物依赖。
6. 强生、GE医疗入股,首个创新外科产品获批
强生、GE医疗入股的GI Windows公司开发的Otoloc磁加压吻合系统已获得美国食品和药物管理局(FDA)510(k)许可(编号:K250541),成为首个通过自成型磁铁控制肠切开术并实现即时管腔吻合的技术。这一突破标志着微创手术领域40余年来的首次重大技术革新,为传统缝合线与吻合器的临床应用提供了颠覆性替代方案。
7. 罗氏首款采用TAGS技术的呼吸检测获FDA批准,用于SARS-CoV-2、甲型流感、乙型流感和RSV
罗氏首款采用TAGS技术的呼吸检测已获得FDA 510(k)许可。它能够同时检测并区分四种最常见的呼吸道病毒:SARS-CoV-2、甲型流感、乙型流感和呼吸道合胞病毒(RSV)。这一创新的综合征PCR测试解决方案为实验室提供了定制测试面板的灵活性,并包含“数字反射”选项以获取更多结果。该测试提供准确的PCR结果,有助于制定针对性的治疗方案,改善患者护理,同时简化实验室工作流程并优化资源利用。
二、欧盟及其它
1.Body Vision Medical在新加坡获得LungVision®的上市前批准,推动用于早期肺癌诊断的AI成像技术
Body Vision Medical是一家人工智能驱动的术中成像领域的领导者,宣布其LungVision高级成像平台已获得新加坡卫生科学局(HSA)的上市前批准,从而可以在新加坡实现全面商业化。这标志着该公司在全球范围内提升早期且精准的肺癌诊断使命中迈出了重要一步。肺癌在新加坡是一个重大的健康问题,大多数患者在晚期才被诊断出来,影响了治疗效果和生存率。LungVision将标准的二维荧光成像系统转化为人工智能驱动的三维成像系统,提供实时导航和更清晰的可视化,从而提高支气管镜手术的准确性。
2. 医疗器械公司Carmat全人工心脏再获CE批准上市
Carmat的全人工心脏Aeson获得CE批准,可在欧盟销售至2027年5月,这是其面临破产后的唯一好消息,Aeson是欧洲唯一上市全人工心脏,给心衰患者带来希望。但仍需解决诸多问题以实现长期或永久植入。
国内获批
一、创新器械获批
1. 磁共振成像系统创新产品获批上市
2025年8月1日,国家药品监督管理局批准了西门子医疗有限公司的“磁共振成像系统”创新产品注册申请。磁共振成像系统由7T超导磁体、梯度系统、射频系统、射频线圈、工作站、生理信号门控系统、检查床、电子柜组成,主要用于临床核磁共振成像诊断。该产品采用深度学习技术,在7T高场磁共振成像系统基础上增加了静动态多通道发射平台与多核成像功能,可提供头部钠图像、四肢肌肉和肝脏的磷核波谱数据。该产品利用多通道与多核成像优势,实现图像的实时调节,可有效提高以中枢神经系统疾病为主的影像诊断效能,提高相应疾病治疗水平。
二、NMPA最新获批器械产品明细
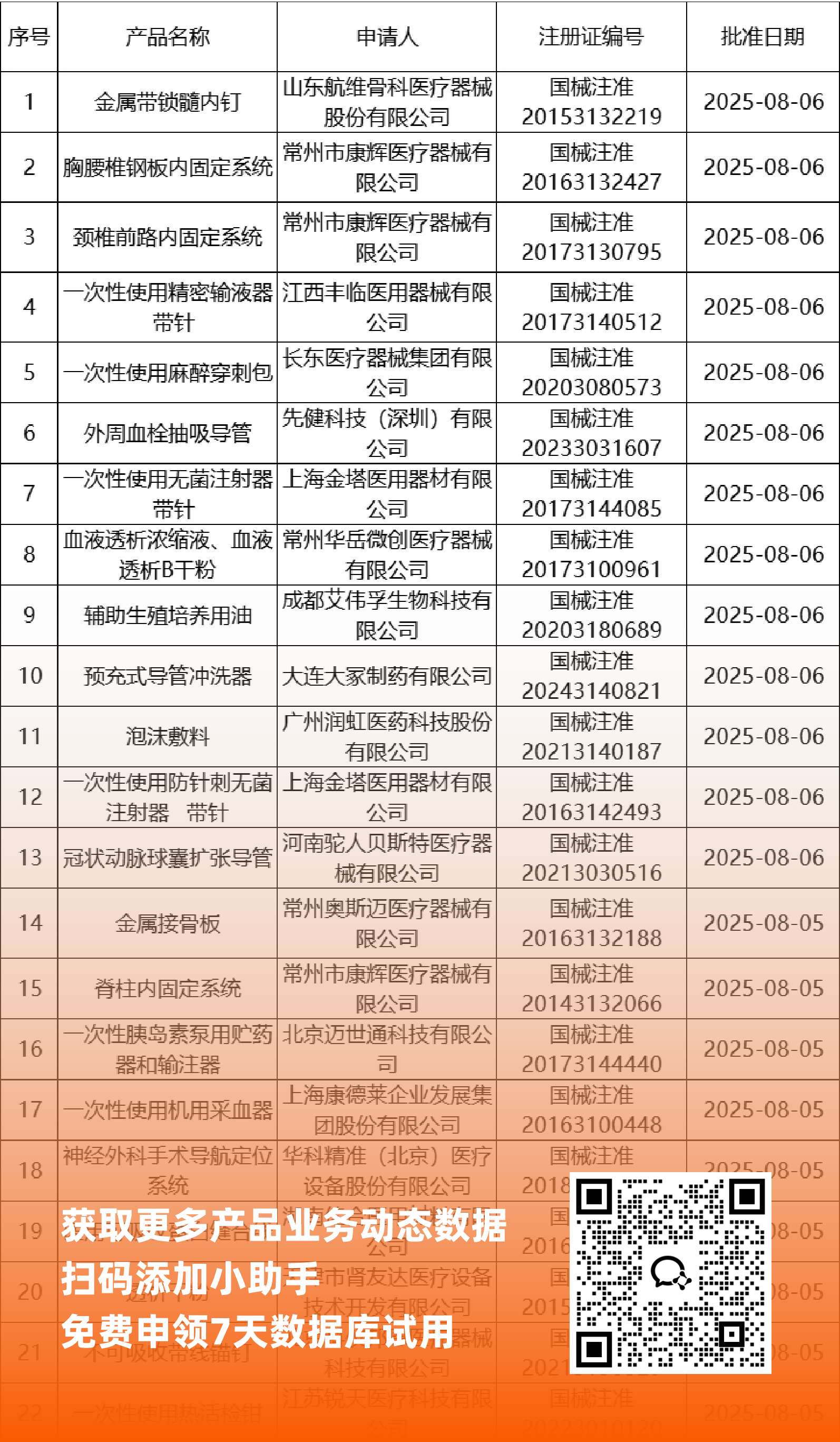
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。