
商务合作

动脉网APP
2025年9月5日至9月11日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及10个器械获FDA批准,5个器械获欧盟及其它批准,另有328个器械获NMPA批准注册文件。
海外获批
一、FDA
1. Naitive Technologies获得FDA 510(k)批准,用于评估骨骼健康的AI驱动OsteoSight软件
医疗技术公司Naitive Technologies是一家专注于人工智能驱动的骨科解决方案的企业,近日通过其AI赋能的软件OsteoSight获得了美国食品药品监督管理局(FDA)的510(k)许可,达成了一个关键的监管里程碑。OsteoSight旨在通过现有医学影像数据评估骨骼健康,利用先进的AI算法提供洞察,无需额外扫描或程序。该软件的目标是帮助医疗保健提供者在常规影像评估中识别可能存在骨质疏松等疾病风险的患者。获得FDA批准后,OsteoSight现在可以在美国的临床环境中推广和使用,显著扩大其在医疗系统中的潜在影响。
2. 数字治疗平台提供商Neurocare group的Apollo TMS治疗设备现已获得美国FDA批准,治疗患有重度抑郁症的青少年
个性化心理健康领域的先驱Neurocare Group AG已获得美国食品药品监督管理局(FDA)批准,其Apollo TMS治疗设备可用于治疗青少年重度抑郁症(MDD)。这种创新的经颅磁刺激(TMS)系统为每年约500万名受重度抑郁影响的美国青少年提供了一种安全、无创且无需药物的替代方案。目前针对该年龄段的治疗选择有限,仅有两种口服抗抑郁药获得FDA批准,但两者均因自杀风险增加而带有“黑框警告”,并且在实现缓解方面的有效率仅为约35%。许多患者因副作用或缺乏疗效而停止服用这些药物。相比之下,临床研究表明,约60%的患者通过TMS治疗可实现缓解,且没有黑框警告或药物相关副作用。Neurocare的先进TMS技术在德国开发,提升了磁场的效率,增强了治疗效果,为其他治疗失败的青少年提供了前景广阔的新选择。
3. Tempus AI获得FDA批准,更新 Pixel以提高心脏成像的准确性和效率
Tempus AI获得了美国食品药品监督管理局(FDA)对其升级版Tempus Pixel的510(k)许可,这是一款由人工智能驱动的心脏成像平台。此次更新通过生成T1和T2在线图谱来增强心脏磁共振图像分析,这些图谱为组织特性提供了精确的数值。这一进步提高了心脏磁共振图像查看和自动生成报告的效率与准确性,有助于流场可视化、功能分析及组织特征描述。与传统的磁共振图像不同,T1和T2图谱能够帮助检测纤维化、炎症或水肿等细微状况。即使扫描仪本身不支持这些功能,Tempus Pixel现在也能直接从原始MRI数据生成这些图谱,并创建用于全面组织评估的详细DICOM图谱。这款人工智能赋能的放射学工具支持临床医生更快、更明智地做出决策,并提供个性化的患者护理。
4. 世和基因世和一号^®泛实体瘤高通量测序基因检测试剂盒于美获批上市
南京江北新区企业世和基因自主研发的世和一号^®泛实体瘤高通量测序基因检测试剂盒,已正式获美国食品药品监督管理局(FDA)批准上市,成为我省首个打入国际核心市场的高通量测序大Panel体外诊断试剂。该产品能全面检测425个实体肿瘤相关基因,提供基因变异全景图谱,为多种实体肿瘤及罕见癌种提供关键信息。此前,该产品已通过中国国家药品监督管理局(NMPA)创新审批,获得第三类医疗器械注册证,并取得欧盟CE认证。此次获批,使其成为全球首个同时获得NMPA、FDA、CE三大认证的肿瘤高通量测序大Panel检测产品。世和一号^®核心指标达国际领先水平,价格不到美国三分之一,公司正推进在美国合作实验室的产品落地,并启动美国医保准入。
5. FDA批准Obagi saypha MagIQ透明质酸注射凝胶用于美容用途
专注于美学治疗的Croma-Pharma GmbH公司宣布,美国食品药品监督管理局(FDA)已批准Obagi saypha® MagIQ,一种基于透明质酸的可注射凝胶。这是Obagi saypha®品牌下首款获得FDA批准的产品,标志着在微创美学医学领域的重要进展。该批准于2025年9月10日确认,使Croma-Pharma GmbH能够将该产品引入美国市场,增强其在受监管医学美容领域的地位。透明质酸是Obagi saypha® MagIQ的主要成分,因其保湿和增加体积的特性,被广泛用于皮肤填充剂。然而,关于该产品的具体应用或可用性的更多细节尚未披露。
6. 手术消融设备开发商AtriCure治疗疼痛的冷冻消融“夹”获FDA批准上市
AtriCure宣布推出创新冷冻消融产品cryoXT,该产品于今年四月获FDA批准上市,旨在管理截肢术后疼痛。专家评价其能在手术期间有效应对疼痛,改善患者康复和生活质量。高管称其体现了公司承诺,为患者和医疗从业者提供差异化解决方案,弥补截肢术后护理空白,也开拓了公司新的增长路径。美国每年超18.5万例截肢手术,约60%患者有残肢痛,85%有幻肢痛,目前治疗有限且以药物为主,效果不佳还易产生依赖性。cryoXT是Atricure cryoSPHER技术升级,采用全新尖端和多表面冷冻技术,可精准作用于大直径暴露外周神经,其“F”形末端专用于处理暴露外周神经。
7. GE,双喜临门
GE医疗集团近日双喜临门:先是Revolution Vibe CT系统获FDA 510(k)认证,该系统专为心脏检查设计,具备动态降噪、自适应扫描及高精度算法,可捕捉稳定图像,穿透钙化层显影,集成无限次单次心脏成像与AI工具,提升检测精准度与患者舒适度,还优化了CCTA检查,股价随之上涨;后是与CDL核技术集团达成新型心脏PET成像剂Flyrcado™注射液分销协议,Flyrcado™作为首款靶向线粒体复合体I的18F标记心肌灌注示踪剂,通过正电子发射显示血流量与线粒体密度分布,为冠心病及心肌缺血诊断提供可视化依据,且空间分辨率更高、背景干扰更低。
8. 首个大口径肺栓塞抽吸导管获批FDA
Imperative Care宣布其Symphony血栓切除系统获FDA 510(k)批准,成为首个用于治疗肺栓塞的大口径抽吸导管系统,适应症从静脉血栓扩展到肺栓塞,可为静脉血栓栓塞症患者提供全面治疗方案。肺动脉栓塞是临床上一种凶险的急重症,未经治疗的死亡率为20-30%,在心血管疾病致死率中位居前3。全球每年有超1000万肺栓塞病例,常规抗凝和药物溶栓治疗对大面积肺栓塞效果有限且出血风险高,还可能导致后遗症。肺动脉取栓手术是针对急性肺动脉栓塞的治疗方法,机械取栓分为支架取栓与抽吸式取栓,抽吸式取栓更适用于肺动脉内较大体积的血栓清除。
9. 脉冲场消融领域迎新黑马:Kardium Globe系统获FDA批准,开启房颤治疗新篇章
Kardium公司的Globe脉冲场消融(PFA)系统获美国FDA上市前批准,配套导引器护套与映射软件也同步通过510(k)许可,成为美国房颤治疗市场新竞争者。该系统全球首创单导管实现“标测+消融”一体化,球形导管表面密布122个独立电极,可实时采集电信号并精准定位异常电活动,同步释放高压脉冲破坏心肌细胞,且不损伤周围组织。其还能单次完成肺静脉隔离,大幅缩短手术时间,降低术后复发风险。关键PULSAR研究数据显示,针对阵发性房颤患者,1年随访期内“无房性心律失常发生率”达78%,且未发生任何设备相关主要安全事件。
10. FDA批准全球首款一次性血管介入机器人
Microbot Medical公司宣布其一次性血管介入机器人LIBERTY获FDA批准上市,成为全球首款用于外周血管介入手术的单次使用远程操作血管介入机器人。公司高管称这是Microbot Medical的决定性时刻,也是血管介入机器人领域的重大突破,公司已为加速市场进入做好充分准备,将切入美国每年约250万例的外周血管手术市场,并积极拓展全球市场。LIBERTY不仅临床效果优异,操作简便,且无需大设备投入,导航到达靶病变成功率达100%,医生辐射暴露量降低92%,有望提升手术效率、降低成本并提高护理质量。LIBERTY体积小巧,具有“一次完成”的设计,可回收处理,旨在降低医院固定资产投入。
二、欧盟及其它
1.瓦里安宣布其微球产品Embozene已获CE批准上市
瓦里安宣布其微球产品Embozene已获CE批准上市,成为首个且目前唯一专门针对GAE(膝关节动脉栓塞术)获CE批准的栓塞剂,用于治疗膝骨关节炎。膝骨关节炎全球报告病例数近3.75亿例,现有治疗方法存在局限,GAE旨在填补治疗空白,通过输送Embozene微球减少炎症区域血流以缓解疼痛。Embozene微球由不可吸收外覆Polyzene-F涂层聚合物的水凝胶制成,具有消炎和抗菌作用,且采用独特颜色编码增强可视化。此前,该微球已用于治疗动静脉畸形、富血管性肿瘤、前列腺动脉栓塞术等,2021年还获FDA“突破性设备”称号,是瓦里安2019年从波科收购而来。
2. 可穿戴医疗设备研发商Lifeward第七代个人外骨骼产品ReWalk 7已获得欧洲CE认证
Lifeward宣布其第七代个人外骨骼产品ReWalk 7获得欧洲CE认证,正式进入欧洲市场销售,这彰显了其在脊髓损伤患者康复领域的技术创新与市场拓展能力。ReWalk 7在云连接与智能控制、可调步态速度、楼梯与人行道无缝激活等方面进行了技术升级,还新增治疗师手持设备,提升了康复体验,且电池续航能力也得到增强。目前,欧洲市场占其外骨骼销售的40%,德国市场尤为重要,公司已与德国主要保险公司达成报销协议。ReWalk 7的推出反映了医疗器械行业在康复领域的快速发展,但高昂的价格仍是患者和医疗机构面临的主要障碍。
3. 心血管解决方案开发商Neurescue治疗心脏骤停介入球囊获CE批准上市
Neurescue宣布其创新器械NEURESCUE device获CE批准上市,该产品被誉为心肺复苏术问世以来复苏医学领域的重大突破,是首款专为非可电击性心脏骤停患者设计的救治设备。全球每年81%的心脏骤停患者无法接受除颤治疗,存活率仅4%,而NEURESCUE device能恢复患者自主心律,为后续治疗争取时间。设备采用自动充盈技术和传感器引导反馈机制,确保操作精确安全。临床研究显示其成功率达100%,平均操作时间仅五分钟。此外,该设备是首个AI辅助、无需透视的球囊导管,可延长急救时间30分钟,且主要由球囊导管和控制器组成,无需其他器械辅助,具有自动充水排水、压力监测和操作简便三大优势。
4. 华睿博视电阻抗成像仪荣获日本注册批准
北京华睿博视医学影像技术有限公司由清华电子工程系成果转化设立,专注非放射性、高安全性医学影像设备研发,包括电阻抗、低频超声与多物理场联合成像等。其自主研发的Infivision 1900是全球首款商用三维胸部电阻抗成像仪,已获中国医疗器械注册证,具备三维动态成像能力,可无创、连续监测肺部通气与血流灌注,为急危重症及呼吸管理等临床场景提供床旁可视化诊疗方案。此前,华睿博视已凭借Infivision ET系列打破进口技术垄断,确立了其在国内胸部电阻抗成像仪国产化进程中的关键推动者和技术原研领航者地位。近日,其电阻抗成像仪又荣获日本注册批准。
5. 医疗技术公司ONWARD Medical家用无创刺激器获CE批准上市
ONWARD Medical宣布其可穿戴神经刺激器ARC-EX获CE批准上市,用于改善因不完全性脊髓损伤(C2-C8节段)导致慢性非进展性神经功能缺损的成年患者的手部力量与感觉功能,允许患者医院及家庭使用。ARC-EX获CE批准得益于其强大临床证据支持,Up-LIFT关键研究显示90%受试者力量或功能改善,87%生活质量提升,且伤后34年患者仍能获益。Pathfinder2研究显示,ARC-EX结合康复训练,一年后上肢力量等显著改善。此外,ARC-EX去年已获FDA批准上市,ONWARD已启动在美国诊所的分阶段推广,初期用户反馈积极。ONWARD的ARC疗法旨在恢复脊髓损伤患者功能,提高生活质量,两个技术平台均获FDA“突破性设备”称号。
国内获批
一、NMPA最新获批器械产品明细
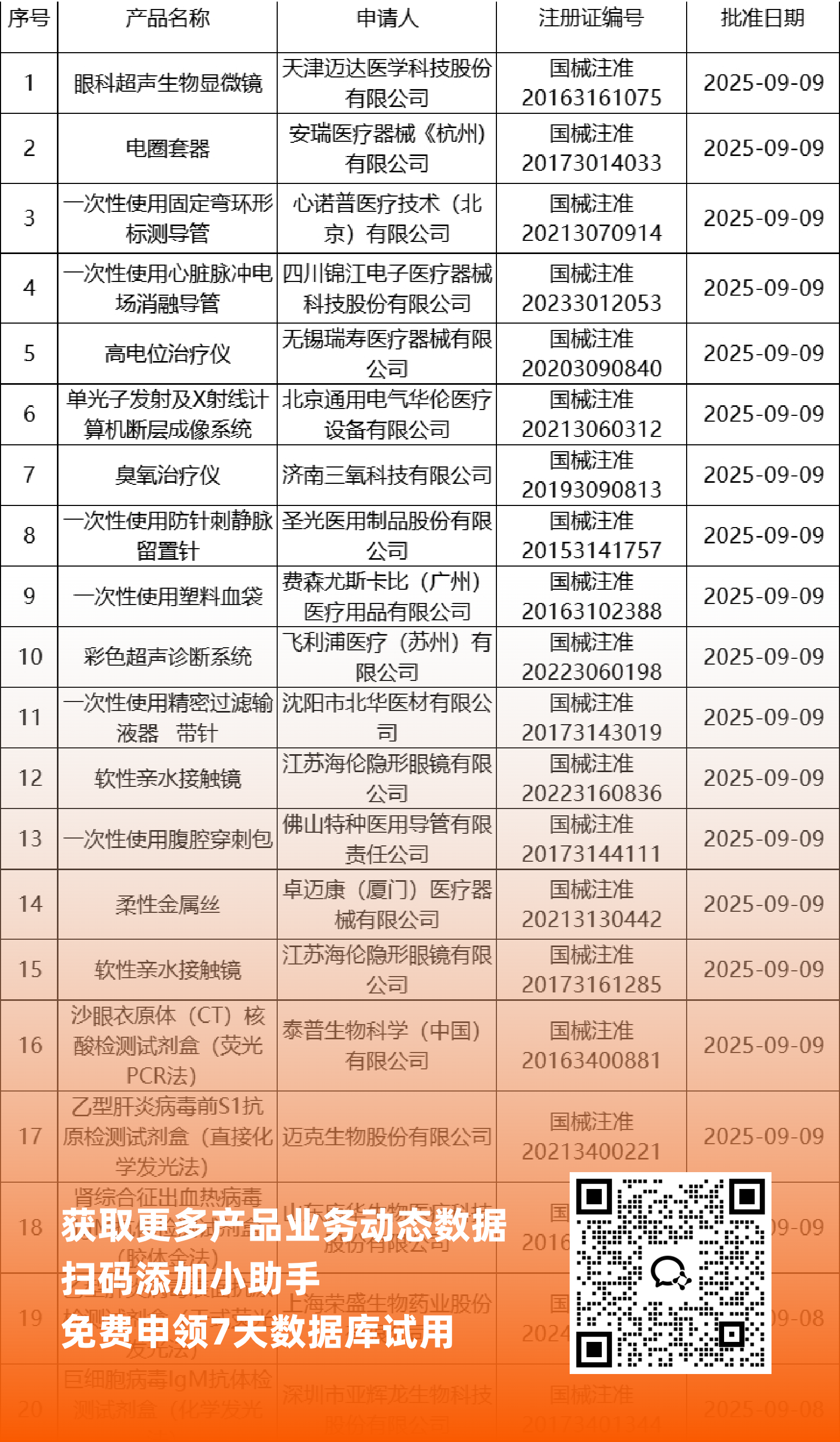
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。