
商务合作

动脉网APP
2025年10月24日至10月30日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及4个器械获FDA批准,2个器械获欧盟及其它批准,1个器械获NMPA创新产品批准,另有384个器械获NMPA批准注册文件。
海外获批
一、FDA
1. 医疗器械公司Vascular Flow螺旋状人工血管获FDA批准上市
Vascular Flow宣布其研发的螺旋状人工血管SLF AV获FDA批准上市,为FDA批准的首款螺旋状人工血管,适用于动静脉瘘建立。全球每年超200万肾脏疾病患者依赖血液透析,动静脉内瘘是透析病人的“生命通道”,但术后失败率较高,早期失功发生率约40%,失败多因湍流致血栓形成,后期失功与静脉高压和血管壁张力有关。如何避免或延缓内膜增厚是延长动静脉内瘘寿命关键,但现有方案无法满足临床需求。SLF AV采用膨体聚四氟乙烯制备,独特之处在于静脉端螺旋状设计,能重塑血流为螺旋层流形态,降低湍流能量,使血流更接近生理状态,显著降低血管内湍流,减小管壁压力与负荷。
2. 戈尔TIPS支架新规格获批上市
戈尔公司宣布其VIATORR TIPS支架新规格(6-10mm)获FDA批准上市,为医生提供更大治疗灵活性,满足患者个体化需求。专家认为,新规格可在特定患者中使用更小分流道,减少潜在不良风险,同时保持卓越疗效,提高实现目标门静脉压力梯度的能力。VIATORR拥有超20年临床性能和超500篇出版物支持,采用戈尔专有ePTFE覆膜,能一致且可定制控制分流道直径,保持恒定直径至少10年。此前VIATORR直径只有8-10mm,新规格为临床医生在平衡门静脉压力梯度与过度分流风险时提供更多选择,让TIPS手术更易实现平衡。戈尔是一家致力于改变行业和改善生活的全球性材料科学公司。
3. 医疗器械公司YorLabs无线ICE获FDA批准上市,零设备成本
YorLabs宣布其无线ICE导管XC11 ICE获FDA批准上市,为FDA首次批准的无线ICE导管。该导管是首创零资本支出超声平台,旨在简化导管室工作流程、降低成本、提升手术效率。它支持单人操作,提供高清心内成像,其无线设计可无缝集成到导管室,实现可视化及治疗引导方式的飞跃。XC11 ICE优势包括零资本支出部署、单人操作控制、零空间占用集成等,满足电生理和结构性心脏病手术对更高可视化、安全性及精准度的需求。YorLabs计划2026年在美国限量投放,随后开展更广泛商业推广及临床合作。
4. 泰尔茂首款双模一体化腔内成像导管获FDA批准上市
泰尔茂首款双模一体化腔内成像导管DualView及成像系统OPUSWAVE获FDA批准上市,这是泰尔茂首个腔内成像产品获FDA批准,其腔内影像产品此前已在日本上市,且日本腔内影像技术应用率全球领先。OPUSWAVE将光学频域成像(OFDI)与血管内超声(IVUS)整合于单一导管,DualView成像导管具备150毫米最大回撤长度、2.6Fr微型化成像轮廓,兼容6Fr指引导管,支持最高40毫米/秒可调回撤速度,OFDI轴向分辨率20μm,IVUS轴向分辨率120μm,可同步并排显示OCT和IVUS图像,实现OCT三维重建,还能利用算法实现IVUS和OCT图像自动融合显示,集成IB-IVUS功能补充组织及斑块成分信息。泰尔茂是医疗技术领域全球领导者,业务遍及全球。
二、欧盟及其它
1. 东方基因,海外又拿下36证
2025年10月27日,东方生物发布公告,其及子公司Healgen Scientific LLC等多款时间分辨荧光免疫产品,近期在欧盟、哥伦比亚、印度尼西亚、沙特等国取得医疗器械产品注册证,共计36证。东方生物2005年成立,专业从事体外诊断产品研发、生产与销售,属高端医疗设备与器械领域,主营POCT即时诊断试剂,应用于传染病(含新冠病毒检测产品)、毒品等多个检测领域,传染病检测和毒品检测是两大核心产品系列。公司销售网络深入120多个国家和地区,2019年境外销售收入占比95%,已取得境外认证/备案300余项、国内注册/备案证书70余项。
2. 心脉医疗Hercules/通天杖Low Profile直管型支架在厄瓜多尔获批上市
心脉医疗™Hercules®/通天杖™Low Profile直管型覆膜支架及输送系统近日在厄瓜多尔获得注册批准,进一步丰富了心脉医疗在厄瓜多尔的产品组合,助力拉美地区业务拓展。该支架适用于血管直管段的主动脉瘤治疗,输送系统采用Low Profile设计,适应狭窄迂曲入路动脉,内置覆膜软鞘,多种锥度设计更好贴合解剖形态。该产品2015年在中国上市,2020年获欧盟CE认证,已在海外30个国家临床应用。此前心脉医疗已有Castor®等多款产品进入厄瓜多尔市场,此次新支架获批有望使更多当地主动脉疾病患者获益。未来,心脉医疗将继续推广优质创新产品至全球市场。
国内获批
一、创新器械获批
1. 磁共振监测半导体激光治疗设备、一次性使用激光光纤套件和立体定向手术计划软件创新产品获批上市
2025年10月29日,国家药品监督管理局批准了杭州佳量医疗科技有限公司的磁共振监测半导体激光治疗设备、一次性使用激光光纤套件和立体定向手术计划软件3个创新产品注册申请。磁共振监测半导体激光治疗设备由主机和配件组成。一次性使用激光光纤套件由医用光纤导管组件和冷却水管组成。立体定向手术计划软件由安装U盘、密钥组成。磁共振监测半导体激光治疗设备与一次性使用激光光纤套件配合,用于对药物难治性癫痫患者(局灶性发作,有明确的致痫区部位或明确的癫痫传导途径)的局部病灶进行激光治疗。立体定向手术计划软件与磁共振监测半导体激光治疗设备配合,用于头部立体定向手术计划制定。
二、NMPA最新获批器械产品明细
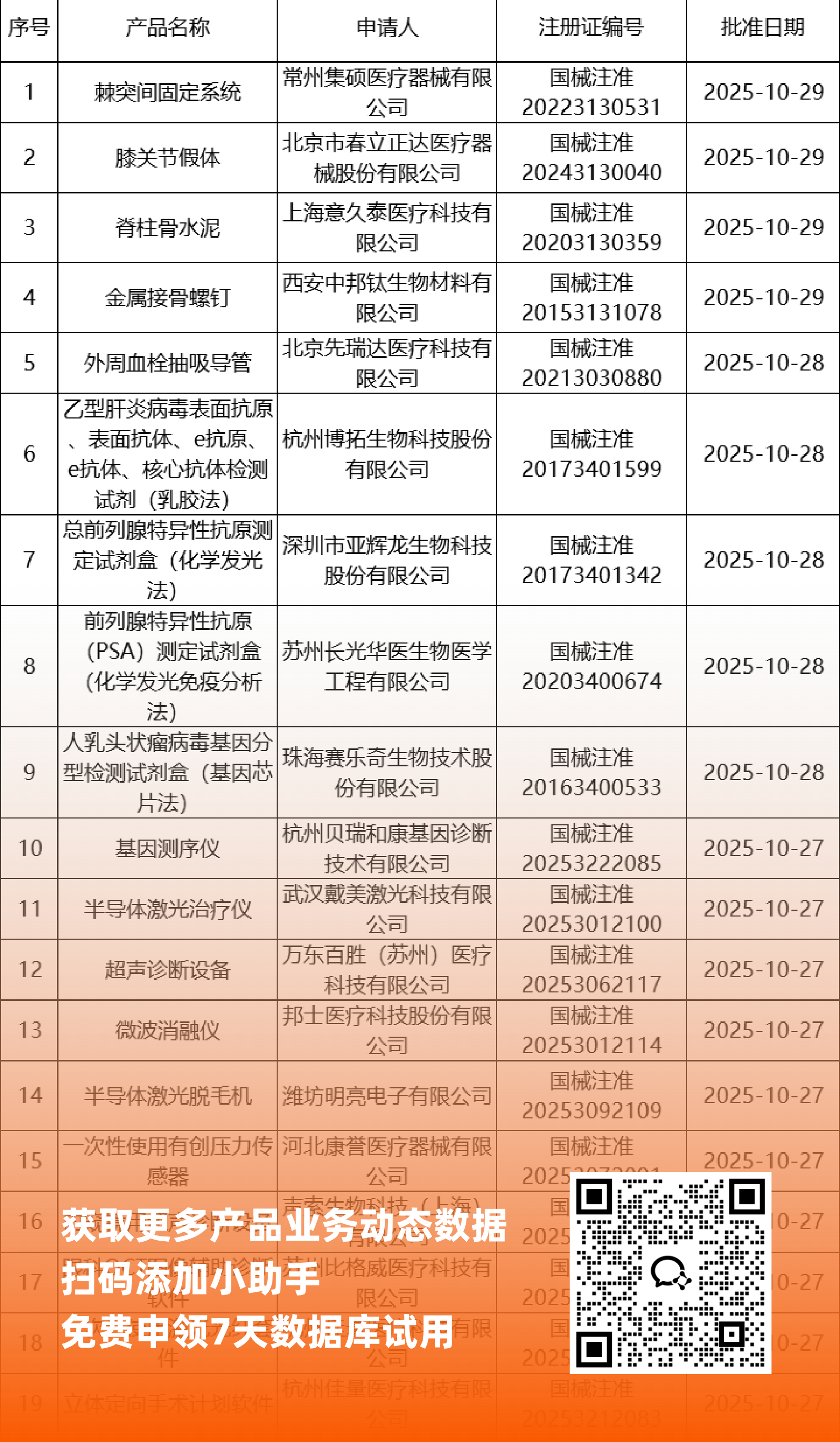
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。