
商务合作

动脉网APP
2025年12月5日至12月11日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及5个器械获FDA批准,另有390个器械获NMPA批准注册文件。
海外获批
一、FDA
1. 美FDA批准首个电刺激抑郁治疗设备,将于2026年上市
美国FDA批准瑞典Flow Neuroscience的家用脑刺激设备FL-100用于治疗抑郁症,为传统抗抑郁药提供替代方案。美国抑郁症发病率十年激增60%,影响超2000万成年人。FL-100重量轻,可远程监督家庭治疗,是美国首个获批同类设备,获批用于18岁及以上中重度抑郁症患者,可单一或联合治疗,但不包括药物抵抗型患者。Flow计划2026年二季度以处方形式在美国上市,零售价500至800美元,正与保险机构谈判。该设备通过严格PMA流程获批,已在多地销售超5.5万人次。FDA批准基于中期临床研究,患者需遵循12周治疗方案,副作用较轻且暂时,市场对脑刺激技术兴趣上升。
2. Ceribell获得FDA 510(k)许可,推出首个谵妄监测解决方案
医疗技术公司CeriBell专有的谵妄监测解决方案已获得美国FDA的510(k)许可,该设备是首个也是唯一获得FDA批准用于筛查和监测谵妄的设备。这一批准巩固了Ceribell系统作为人工智能驱动的脑监测平台的地位,将其益处扩展到更多重症患者,并为那些有癫痫和谵妄风险的人提供额外的诊断信息。谵妄会带来显著风险,包括死亡率增加、住院时间延长以及长期认知障碍,给家庭和医疗系统带来沉重负担。当前的检测方法是间歇性的且劳动强度大,依赖于容易出现人为错误的床旁评估。CeriBell的解决方案能够持续分析脑电图片段,提醒临床医生注意与谵妄相关的模式,从而实现及时且可靠的评估和持续监测。这项创新有望加强谵妄的检测和管理,同时降低因漏诊或延误诊断而产生的高昂成本。
3. 全球唯一可调弯关节磨钻Articulator获FDA批准上市
Joint Preservation Innovations宣布其可调弯磨钻Articulator获FDA批准上市,为首个且唯一关节式旋转切割器械。传统直磨钻存在诸多不便,而Articulator可精确掌控,提升手术精度、扩大操作范围,契合行业趋势。该器械实现关节镜下骨切除技术飞跃,切割表面积提高601%,能处理狭窄、弯曲或受阻骨骼区域。它采用440c不锈钢材制备,切割效率更高,专有微型机械加工接头可减轻过热现象,保持刚度。此外,Articulator设置三个调弯角度,总切割表面积远超直头磨钻。其优势包括实现直磨钻无法完成的骨切除操作,提升手术效率,降低学习曲线,助力复杂重塑手术,特别适用于髋、肩、踝、肘等关节保留手术。
4. 美敦力旗下Hugo™机器人辅助泌尿外科手术系统获FDA批准上市
美敦力旗下Hugo™机器人辅助泌尿外科手术系统获FDA批准上市,可用于前列腺切除术等微创泌尿外科手术,这些手术在美国每年约23万例。Expand URO试验证明其满足泌尿外科手术主要安全性和有效性终点。美敦力计划将其应用扩展到更多外科专科,预计用于普通和妇科外科手术。美敦力对Hugo带来的收入增长较有信心,其董事长兼CEO称将在今年下半年及以后实现更大收入增长。此外,美国是全球最大手术机器人市场,2020年市场规模46亿美元,占全球55.1%。2000年达芬奇手术机器人获FDA批准后稳坐头号宝座,2025年Q3直觉外科收入25.1亿美元,美敦力Hugo手术机器人2019年推进,2021年登陆欧洲市场。
5. Axogen可再生生物型人工神经支架获FDA批准上市
Axogen宣布其可再生生物型人工神经支架AVANCE获FDA批准上市,用于治疗1个月及以上儿童及成人患者的感觉、混合及运动外周神经断伤。AVANCE从人体组织产品转变为生物制剂,巩固了监管地位,确认了其作为可接受治疗选择的地位,且已通过严格评估,安全有效,益处大于风险。AVANCE基于在感觉神经断伤中的结果获加速批准,持续批准取决于验证性临床试验结果。它是一种即用型脱细胞神经支架,保留了细胞外基质结构,具有桥接神经缺损、重塑为患者自身组织、避免额外手术并发症、提供多种规格及无菌供应保质期长等优势。Axogen计划于2026年第二季度初开始商业化AVANCE。
国内获批
一、NMPA最新获批器械产品明细
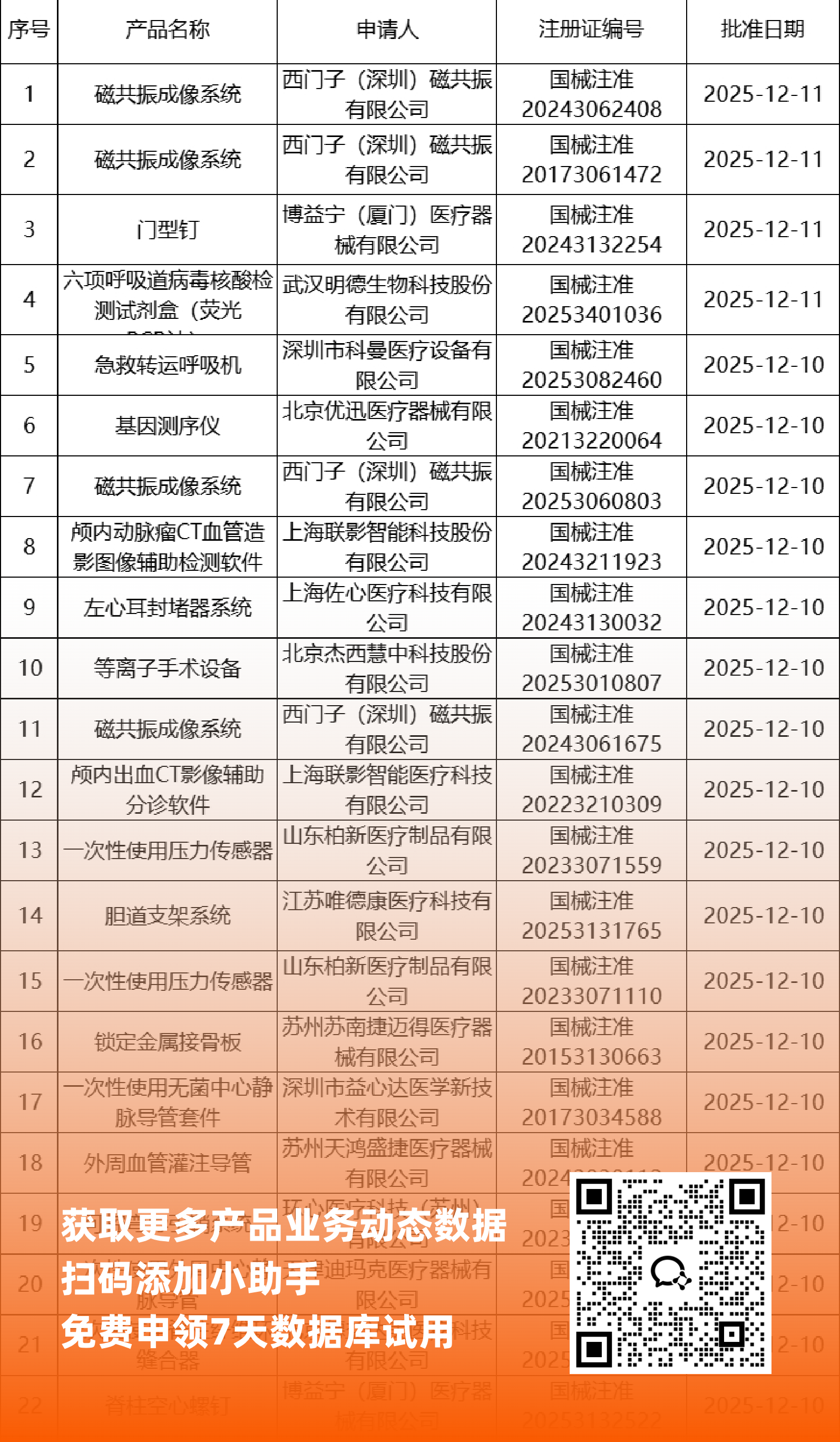
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。