
商务合作

动脉网APP
2025年12月12日至12月18日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及14个器械获FDA批准,5个器械获欧盟及其它批准,4个器械获NMPA创新产品批准,另有324个器械获NMPA批准注册文件。
海外获批
一、FDA
1. 雅培双重获批,结构性心脏病封堵器集采落地
雅培宣布其Amplatzer Piccolo™ Delivery System同时获FDA批准与CE认证,用于优化早产儿动脉导管未闭(PDA)的经导管治疗流程,为结构性心脏病微创介入在极低体重人群应用提供新工具。PDA是常见先天性心脏病,胎儿期动脉导管出生后未闭合会形成持续左向右分流,加重呼吸负担,引发呼吸困难等问题,其症状与导管大小等因素相关,严重者诊断处理关乎生存。PDA治疗从外科结扎发展到经导管封堵技术,但早产儿尤其是极低体重者治疗长期面临挑战,约20%早产儿PDA需干预治疗,专用解决方案有明确临床需求。Amplatzer Piccolo™ Delivery System专为早产儿设计,配合Amplatzer Piccolo™ Occluder使用。
2. Gordian Surgical带缝合功能的腹腔镜穿刺器获FDA批准上市
Gordian Surgical宣布其带缝合功能的腹腔镜穿刺器TroClose 2.0获FDA批准上市。腹腔镜手术切口疝发生率高达7%,传统闭合方法成本高且耗时,TroClose 2.0能让切口疝发生率降至0%,杜绝患者切口疝发生。其临床研究显示,该产品不仅减轻术后患者疼痛,术后12个月穿刺孔处切口疝发生率为0%。TroClose 2.0包括套管和穿刺针,内置缝线和可吸收锚定,采用独特的180度缝线布放系统,组织张力显著降低75%,可降低患者术后一周疼痛感。此外,它还能实现自动化预设闭合,消除摆动运动难题,确保闭合更顺畅精准,且是市场上唯一无需维持气腹或可视化就能安全高效闭合穿刺孔的产品。
3. 强生液体栓塞剂TRUFILL n‑BCA新适应症获FDA批准
强生宣布其液体栓塞剂TRUFILL n‑BCA新适应症获FDA批准,用于脑膜中动脉栓塞术治疗症状性亚急性与慢性硬膜下血肿(cSDH),此前美敦力的Onyx LES也获批相同适应症。TRUFILL n‑BCA新适应症获批基于MEMBRANE随机对照试验,研究显示其治疗有效性优于标准方案且安全性得到证实。专家评价其满足了慢性硬膜下血肿新治疗方案的需求,高管称此次获批巩固了产品价值,体现了公司承诺。慢性硬膜下血肿在老年及抗凝治疗患者中常见,传统手术复发率较高,脑膜中动脉栓塞术作为微创方法可治疗该疾病。TRUFILL n‑BCA已有超25年历史,此次适应症扩大使其性能可应用于慢性硬膜下血肿治疗。
4. CMR Surgical新一代腔镜手术机器人获批FDA
2025年12月17日,CMR Surgical宣布其Versius Plus机器人辅助手术系统获美国FDA 510(k)批准,可用于胆囊切除等软组织微创手术,此批准建立在此前通过FDA De Novo审查基础上,标志着CMR在美国监管路径的关键进展。CMR Surgical成立于英国剑桥,产品策略区别于传统大型手术机器人,选择模块化、可扩展、贴近现有腹腔镜体系的技术路线,先在欧洲积累经验再推进美国市场。Versius Plus并非全新平台,是在原有架构上的系统级升级,重点在于“更好用、更好落地”。其延续模块化床旁设计,机械臂灵活布置,降低医院改造成本;操作端采用开放式控制台,适配教学医院和多学科团队;成像与能量能力上,系统支持荧光成像。
5. 朗视FusionScanner SU系列口腔数字印模仪获美国FDA二类医疗器械注册认证,品牌全球化战略再添里程碑
朗视仪器自主研发的FusionScanner SU系列口腔数字印模仪获美国FDA二类医疗器械注册认证,这是朗视产品矩阵中首张FDA市场准入许可,标志着其成功通过全球顶级医疗监管体系核验,迈出布局国际高端市场关键一步。美国FDA是全球医疗审核最严格、标准最高的监管机构之一,获此认证是对该产品在技术安全性、临床有效性及数据精准度上的最高级别认可。该产品兼顾“高效临床操作”与“舒适诊疗体验”,硬件上微米级扫描精度、高帧率搭配超大景深,性能上AI算法引擎提供硬核支撑。朗视将以此为契机,持续推进产品国际合规布局,推动中国“智”造口腔设备走向世界。
6. RIVANNA宣布Accuro 3S针头引导套件获FDA批准
医疗技术开发商RIVANNA®宣布,其Accuro® 3S针头引导套件耗材已获得FDA的510(k)许可,标志着在提升超声引导下针头放置的安全性和有效性方面迈出了重要一步。该套件专为与Accuro 3S超声系统和Dual-Array™探头配合使用而设计,包含无菌、一次性使用的组件,有助于感染控制和提高工作流程效率。其患者覆盖布配有稳定带,可在针头接近过程中固定探头,实现免手持支持,简化单人操作流程,并允许临床医生双手保持在针头上以获取触觉反馈。Dual-Array探头通过其中央孔径促进中线放置,同时集成的探头罩隔离插入部位,防止污染,确保受控的操作区域。RIVANNA联合创始人兼首席执行官Will Mauldin博士强调了公司致力于提供直观工具以提高手术精度和患者安全性的承诺,并突出了其单人操作效率解决方案的独特市场优势。
7. Medivis颅骨导航平台获得FDA 510(k)许可
外科智能领域领导者Medivis宣布其颅骨导航平台已获得FDA 510(k)许可,成为全球首个获批用于颅脑神经外科术中引导的增强现实(AR)系统。这是继Medivis今年早些时候获得脊柱导航平台FDA许可后的又一进展。Medivis平台利用AR技术将患者的影像叠加到手术区域,为外科医生提供关键解剖结构和计划手术路径的实时视图。该技术提升了决策效率,减少了工作流程中断,并降低了对外部显示器的依赖。其便携式设计可在传统系统无法有效运作的环境中(如ICU)提供可靠的影像引导,将精准医疗扩展到更多临床场景。早期临床应用表明,该平台可显著降低外脑室引流管(EVD)的错置率,目前这一比率高达30%,从而提高患者安全性、加快干预速度并提升神经外科护理标准。
8. BlueWind Medical升级版胫骨神经刺激器获FDA批准上市
BlueWind Medical宣布其升级版Revi胫骨神经刺激器获FDA批准上市,该设备旨在为急迫性尿失禁患者提供更有效治疗和长期症状缓解。新版Revi采用简约易用设计,配备智能友好的用户界面,保留简易三键操控,提升患者使用便捷性。其优势包括个性化治疗方案、显著缓解症状(79%患者症状减少≥50%)、卓越患者满意度(97%患者表示满意)和出色安全性(无严重不良事件)。Revi由微型植入刺激器和移动可穿戴设备组成,通过小切口植入,手术仅需30分钟,刺激器体积小,具有无电池、无线、微型、闭环刺激等优势。患者每天在家进行两次半小时治疗,即可改善膀胱过度活动症。
9. P&F经导管双上腔静脉瓣膜系统TricValve获FDA批准开展TRICAV II关键性试验
P&F Products and Features GmbH宣布其经导管双上腔静脉瓣膜系统TricValve获FDA批准开展TRICAV II关键性试验,该试验旨在比较TricValve联合优化药物治疗与单纯药物治疗的疗效,标志着产品临床开发进入新阶段。PI和高管均给予高度评价,认为其是拓展TR治疗选择的重要里程碑,为严重TR患者带来新希望。美国约160万人受严重TR影响,许多患者因各种原因不适合手术或现有经导管治疗,缺乏有效介入治疗选择。TricValve已获CE批准,在约70个国家上市,累计治疗超3000名患者。它由两个自膨胀生物瓣膜组成,适用于极度危险或不能手术治疗的患者,不对三尖瓣进行干预。
10. 九安医疗2款呼吸道联检产品获FDA许可
九安医疗公告称,其美国子公司iHealth Labs Inc.的呼吸道四联检(甲型流感、乙型流感、COVID-19及RSV呼吸道合胞病毒,含家用、专业用试剂盒)、三联检(甲型流感、乙型流感及COVID-19病毒,含家用、专业用试剂盒)产品,均收到美国FDA 510(K)上市前通知,获准在美国市场正常销售。四联检试剂盒拓展了公司可检测病毒类别,满足美国市场多元化需求;三联检试剂盒在准确度等关键性能指标上有所提升,且不因EUA终止而失效,可在EUA终止后持续销售。上述产品获FDA许可,代表公司核心战略业务进一步拓展,丰富了IVD领域产品线,有助于提升核心竞争力。
11. 首款12导联无线心电获批
HeartBeam宣布其创新型12导联心电图(ECG)系统获美国FDA 510(k)批准,为首个获批的12导联无线心电系统。该系统通过捕捉三个非共面维度心脏电信号合成标准12导联心电图,突破传统设备局限,支持患者居家自主采集,数据由认证专家即时审核。临床验证基于VALID-ECG研究数据,审批周期优于同类器械。获批后,公司计划2026年第一季度在美国启动有限度商业化,首批合作机构包括礼宾诊所和预防心脏病中心。技术拓展方向包括开发可延长佩戴的12导联贴片原型等。行业分析师指出,此项批准或推动远程心脏监测市场变革,预计2027年全球规模将突破85亿美元。
12. FDA批准为小至7个月的儿童使用人工耳蜗植入物
美国食品和药物管理局(FDA)批准了MED-EL人工耳蜗的扩展适应症,允许其用于低至7个月大、患有双侧感音神经性耳聋(SNHL)的儿童。这使得MED-EL成为该年龄段婴儿唯一获得FDA批准的选择,能够让他们更早接触声音并促进语言发育。此次批准还扩大了12个月及以上儿童的听力学和语言适应症。这一决定基于一项涉及123名儿童(7至71个月)的试验,结果显示,在第一年中,植入人工耳蜗的临床成功率达到81%至88%,且严重并发症的发生率较低。12个月以下儿童与年龄较大的儿童的并发症发生率相似,且均为已知风险。计划开展一项批准后研究,以进一步评估符合新标准的儿童。MED-EL美国公司总裁兼首席执行官约翰·斯帕拉西奥(John Sparacio)强调了早期接触声音对儿童未来发展的重要性。
13. 全球唯一冠脉取栓支架获FDA批准上市
Vesalio宣布其冠脉取栓支架enVast获FDA批准上市,并将于不久后在美国商业上市。enVast是首个也是唯一获准用于心脏循环系统机械血栓切除术的装置,专为高血栓负荷患者设计,重新定义了冠状动脉血栓切除术。该装置基于支架式血栓捕获结构设计,经由专有捕获区技术增强,能安全捕获并清除所有类型冠状动脉血栓,恢复缺血心肌血流灌注。其取栓部分由Drop Zone、FLOW RESTORATION ZONE和CLOSE DISTAL BASKET组成,分别提供不同功能,确保有效收集血栓,提高首次通过成功率,改善患者预后。enVast拥有多种尺寸,可满足不同解剖结构的STEMI患者需求,已被证明可消除大量血栓负荷,并在85%病例中立即实现再灌注。
14. 美FDA批准首个电刺激抑郁治疗设备,将于2026年上市
美国FDA批准瑞典Flow Neuroscience的家用脑刺激设备FL-100用于治疗抑郁症,为传统抗抑郁药提供替代方案。美国抑郁症发病率十年激增60%,影响超2000万成年人。FL-100重量轻,可远程监督家庭治疗,是美国首个获批同类设备,获批用于18岁及以上中重度抑郁症患者,可单一或联合治疗,但不包括药物抵抗型患者。Flow计划2026年二季度以处方形式在美国上市,零售价500至800美元,正与保险机构谈判。该设备通过严格PMA流程获批,已在多地销售超5.5万人次。FDA批准基于中期临床研究,患者需遵循12周治疗方案,副作用较轻且暂时,市场对脑刺激技术兴趣上升。
二、欧盟及其它
1. 雅培双重获批,结构性心脏病封堵器集采落地
雅培宣布其Amplatzer Piccolo™ Delivery System同时获FDA批准与CE认证,用于优化早产儿动脉导管未闭(PDA)的经导管治疗流程,为结构性心脏病微创介入在极低体重人群应用提供新工具。PDA是常见先天性心脏病,胎儿期动脉导管出生后未闭合会形成持续左向右分流,加重呼吸负担,引发呼吸困难等问题,其症状与导管大小等因素相关,严重者诊断处理关乎生存。PDA治疗从外科结扎发展到经导管封堵技术,但早产儿尤其是极低体重者治疗长期面临挑战,约20%早产儿PDA需干预治疗,专用解决方案有明确临床需求。Amplatzer Piccolo™ Delivery System专为早产儿设计,配合Amplatzer Piccolo™ Occluder使用。
2. Hyperfine宣布Swoop®系统在印度获得监管批准
健康技术公司Hyperfine已获得印度中央药品标准控制组织 (CDSCO) 的监管批准。这一批准使得Swoop®系统能够在印度全国范围内商业化,满足了这一全球规模最大且增长最快的医疗市场对先进脑成像的重大未满足需求。Hyperfine 将与领先医疗设备分销商 Radiosurgery Global, Ltd. (RSG) 合作分销该系统,RSG在先进医学影像领域拥有专业能力,并在印度医疗系统中具备强大的网络。RSG董事总经理Kapil Kalra强调,此次合作将把Hyperfine创新的便携式脑部MRI技术转化为可扩展的解决方案,推动其在印度的广泛应用,从而提升全国神经影像服务的提供方式和覆盖范围。
3. 海利生物控股子公司产品在印度尼西亚获得注册证
海利生物公告,其控股子公司陕西瑞盛生物科技有限公司的GORORISE天然骨移植材料,获印度尼西亚卫生部医疗器械注册证。该产品用于颌骨缺损修复,多孔结构和天然成分可引导新骨生成并牢固结合,是具良好骨组织再生修复能力的植入性医疗器械。此次产品获注册证,有利于瑞盛生物拓展东南亚市场,但获得注册证仅代表产品具备在印度尼西亚销售的准入条件,目前尚未形成实际销售。且产品销售会受到海外法规政策、市场环境变化及汇率波动等不确定因素影响,利润贡献具有不确定性,尚无法预测其对公司未来业绩的具体影响。
4. 迈捷生命旗下“骨填充材料”获批“越南D类”医疗器械注册证
迈捷生命自主研发的“预充型可注射骨填充材料”获越南卫生部D类医疗器械注册证,此前已获国家药监局批准。该材料是迈捷布局全球市场的首款重磅产品,作为国内首创,性能超越多款传统人工骨产品,此次获批为中国医疗器械企业拓展东南亚市场树立新标杆。迈捷生命科学成立于2017年,聚焦生物医用材料等领域,依托两大技术平台构建多学科产品矩阵。可注射骨填充材料原料源于天然猪松质骨,保留天然骨小梁结构,骨诱导性能优异,创新预填充形式可缩短手术时间,便捷性和生物特性超越现有产品。该材料接连获批是羟基磷灰石赛道蓬勃发展的缩影。
5. Suturion革命性腹部缝合器Suture-TOOL获CE批准上市
Suturion宣布其革命性腹部缝合器Suture-TOOL获CE批准上市,该产品将使欧洲腹壁缝合标准化、高效且安全,有望改善患者预后并降低医疗成本。Suturion首席执行官表示,此次认证是向欧洲推广该技术的关键一步,采用小针距缝合技术可减少并发症,为医疗系统节省开支。Suture-TOOL首阶段将重点在英国、北欧及比荷卢三国推出,已与多家经销商合作确保临床可及性。欧美每年超700万患者接受开腹手术,约三分之一出现可避免并发症,主要因腹壁筋膜愈合缓慢,对缝合质量要求高,而传统人工缝合学习曲线长。Suture-TOOL作为首创缝合器,精确度高,可减少并发症,其手持式设计,由两个钳口组成,针自动转移,缝合过程简便。
国内获批
一、创新器械获批
1. 经导管主动脉瓣系统获批上市
2025年12月12日,国家药品监督管理局批准了沛嘉医疗科技(苏州)有限公司“经导管主动脉瓣系统”创新产品注册申请。该产品主动脉瓣的定位键设计预期可实现瓣膜精确定位与锚定;流出端大网孔设计预期可降低低冠状动脉患者后期冠脉再介入治疗的难度;流入端菱形网孔高密度设计预期可提供良好的封堵效果。输送器的可调弯设计和可旋转设计预期可提高瓣膜定位和释放的精确性。产品适用于经心脏团队评估认为有症状、重度主动脉瓣反流(大于等于3级),不适合进行常规外科手术置换瓣膜、年龄大于等于70岁的患者。
2. 一次性使用无菌导尿管获批上市
2025年12月12日,国家药品监督管理局批准了泰州度博迈医疗器械有限公司“一次性使用无菌导尿管”创新产品注册申请。该产品分为单腔、双腔和三腔型。导尿管管身外表面含有聚赖氨酸涂层,基于聚赖氨酸与细菌细胞膜的电荷相互作用机制,以直接接触方式发挥抑菌作用,减少细菌在导尿管表面的定植和生长。
3. 质子治疗系统获批上市
2025年12月15日,国家药品监督管理局批准了瓦里安医疗系统粒子治疗有限公司的质子治疗系统注册申请。该产品由加速器子系统和治疗子系统组成,加速器子系统包括主加速器系统、能量选择系统和射束传输系统,治疗子系统包括360°旋转束治疗系统和治疗计划系统,适用于治疗全身实体恶性肿瘤及特定良性疾病。该产品采用悬臂式机架的小型化设计,可节约质子设备的空间、提高治疗效率。
4. 植入式脑深部神经刺激系统获批上市
2025年12月15日,国家药品监督管理局批准了景昱医疗科技(苏州)股份有限公司的植入式脑深部神经刺激器、植入式脑深部神经刺激电极导线、植入式脑深部神经刺激延伸导线注册申请。植入式脑深部神经刺激器与植入式脑深部神经刺激电极导线、植入式脑深部神经刺激延伸导线联合使用,组成植入式脑深部神经刺激系统,该系统对伏隔核和内囊前肢进行刺激,用于难治性的中重度阿片类药物成瘾患者的防复发辅助治疗。植入式脑深部神经刺激系统填补了物理性干预阿片类药物成瘾治疗的技术空白,为阿片类药物成瘾患者的治疗提供了更多选择。
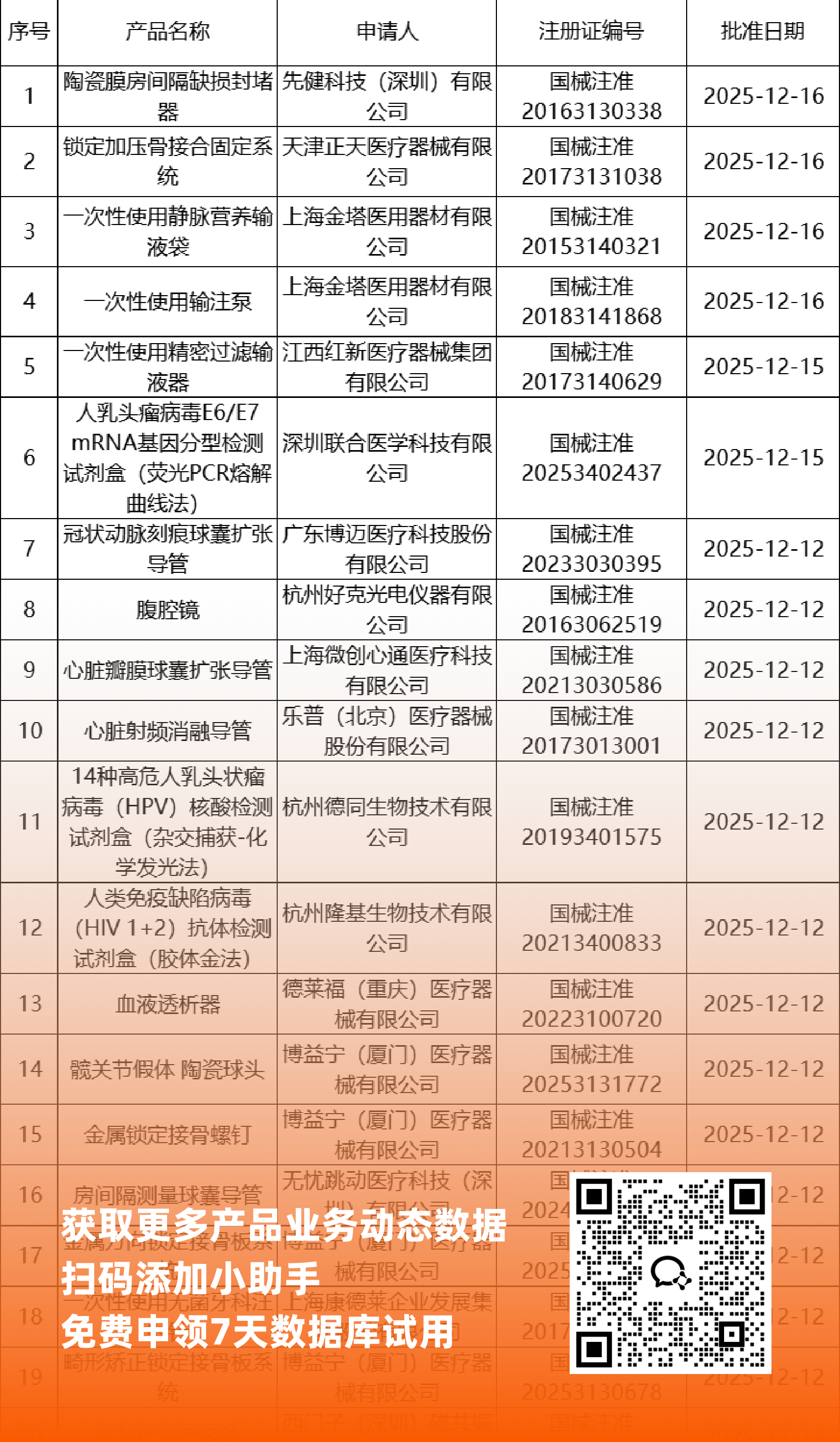
二、NMPA最新获批器械产品明细
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。