
商务合作

动脉网APP
2026年1月23日至2026年1月29日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及3个器械获FDA批准,2个器械获欧盟及其它批准,5个器械获NMPA创新产品批准,另有494个器械获NMPA批准注册文件。
海外获批
一、FDA
1. FDA批准无创碎石:肾结石治疗首次进入“无麻醉门诊路径”
2026年1月,FDA通过510(k)路径批准SonoMotion的Break Wave™体外碎石系统用于肾结石治疗,这是首款完全非侵入、无需麻醉、可在清醒状态下实施的超声碎石设备,推动肾结石治疗从“手术室+麻醉依赖”向“门诊级干预”拓展。Break Wave™适用于肾脏、输尿管结石及有症状或潜在风险的结石患者,可在普通诊室完成治疗,无需麻醉、切口或留置输尿管支架。其技术平台围绕“低压聚焦超声+实时影像引导”展开,与Stone Clear™组合构成完整无创治疗路径。Break Wave的FDA批准基于多项临床与前期研究成果,未观察到严重不良事件,为患者提供无需等待自然排石即可立即治疗的新选择。SonoMotion成立于2014年,试图重写碎石逻辑。
2. 全球首个,Aidoc获FDA认证,开启临床AI新纪元
医疗AI领域迎来重磅消息,Aidoc获FDA认证,推出全球首个医疗行业全面AI分诊解决方案,标志医疗AI发展迈入新阶段。Aidoc自2016年在以色列创立,怀揣用AI革新医疗行业的梦想,初期聚焦医学影像分析领域,不断优化算法,后持续加大研发投入,拓展业务范围,技术能力与产品矩阵日益丰富。此前,Aidoc在临床AI领域已硕果累累,多款产品获FDA批准,如世界首个获批的脑部CT AI辅助分诊工具,以及颈椎骨折、肺栓塞等人工智能产品,其AI肺栓塞筛查方案还被纳入医院工作流程。
3.便携式新生儿保温箱获批FDA
2026年1月,英国mOm Incubators公司核心产品Essential Incubator获FDA 510(k)上市许可,成为少数获美国认可的便携式新生儿保温箱系统之一,可正式进入美国市场,为早产儿等提供连续稳定体温管理。该设备定位可移动温控系统,面向产房、基层医院、转运护理、农村偏远地区及人道主义救援等非NICU场景,强调从分娩到产后护理的连续使用。其核心创新是围绕新生儿护理流程进行系统性重构,体现在轻量化可移动设计、连续恒温与多电源支持、开放式结构与易用性、符合安全与合规基础、适配多种护理模式等方面,还已先后获得CE认证与FDA 510(k)批准。
二、欧盟及其它
1. HighLife宣布经导管二尖瓣置换系统HighLife TMVR获CE批准上市
HighLife宣布其经导管二尖瓣置换系统HighLife TMVR获CE批准上市,适用于中重度或重度二尖瓣反流且不适合外科修复/置换及经导管缘对缘修复术的成人患者。PI评价其性能稳定,结合经股动脉入路和可预测的瓣膜功能,为患者提供新选择;手术方案直观易重复,适配导管室环境。高管称获CE批准将为欧洲患者提供新选择,将以审慎态度推进商业化。该系统采用独特双组件瓣中环设计,覆盖最广泛原生二尖瓣瓣环尺寸范围(30-53mm),将在欧洲分阶段推广。HighLife TMVR成为第三款海外上市的经导管二尖瓣置换系统,随着更多产品上市,二尖瓣反流治疗将开启百花齐放时代。
2. 从中国首创到走向欧洲:西湖欧米IGF-I临床质谱诊断产品获欧盟CE认证
西湖欧米在临床蛋白质谱体外诊断(IVD)领域迎来又一重要里程碑——公司自主研发的胰岛素样生长因子I(IGF-I)检测试剂盒(液相色谱-串联质谱法,LC-MS/MS),正式完成欧盟CE认证,并已收录于欧洲医疗器械数据库EUDAMED,获准进入欧盟市场。这一进展,标志着中国原创的临床蛋白质谱诊断产品,在完成国内注册后,进一步通过了欧洲医疗器械法规体系的系统性审查,实现了从中国首创走向国际合规的关键跨越。这是中国大分子临床质谱精准诊断领域进展的一小步,是西湖欧米成长的一大步。
国内获批
一、创新器械获批
1. X射线计算机体层摄影设备获批上市
2026年1月23日,国家药品监督管理局批准了上海联影医疗科技股份有限公司的X射线计算机体层摄影设备注册申请。该产品由扫描架、两套高压发生器、两套X射线管组件、两套探测器、检查床、激光定位灯、控制台、限束器、电源柜、生理信号门控单元、选配件和附件组成,用于常规临床CT检查,支持冠状动脉CT血管造影和能谱检查。该产品是国内首个采用双源双宽体探测器技术的CT,具有容积覆盖宽和高时间分辨率的双重优势,可提升CT心脏扫描能力,降低CT心脏检查对患者的要求。
2. 一次性使用外周血管血栓旋切导管获批上市
2026年1月23日,国家药品监督管理局批准了江苏金泰医疗器械有限公司的一次性使用外周血管血栓旋切导管注册申请。该产品由旋切导管装置、驱动回收装置、无菌收集袋及无菌覆盖布组成,与外周血管血栓旋切设备配合使用,适用于外周动脉血管(不含肺血管)急性、亚急性、慢性血栓经皮腔内去除。该产品采用磁耦合传动技术,导管电机分离及双刀构型设计,相比传统血栓减容方式,具有操控简便、高效的优势。该产品为国内首创,并达到国际先进水平,为外周血管血栓性疾病治疗提供了新的解决方案。
3. 射频穿刺发生器获批上市
2026年1月29日,国家药品监督管理局批准了慧扬医疗科技(苏州)有限公司的射频穿刺发生器注册申请。该产品由射频主机、脚踏开关及中性电极线组成,与一次性使用射频房间隔穿刺针配合使用,利用射频电流的热效应用于右心房至左心房的房间隔穿刺。该产品利用射频能量穿透房间隔,穿刺无需较大机械力,提高了操作的安全性。该产品的上市为患者提供了更多的治疗选择。
4. 一次性使用心腔内超声成像导管获批上市
2026年1月29日,国家药品监督管理局批准了上海微创电生理医疗科技股份有限公司的一次性使用心腔内超声成像导管注册申请。该产品由一次性使用心腔内超声成像导管(含换能器)、操作手柄和连接尾线组成,与便携式数字化彩色超声诊断仪配合使用,可用于心脏及心脏大血管、心内解剖结构的超声成像;与三维心脏电生理标测系统配合使用时,可提供导管定位信息。该产品为具有磁定位功能的心腔内超声成像导管,用于心脏超声成像的同时还可以提供导管定位信息并进行超声建模,可给医生提供更多术中信息。
5. CT引导穿刺手术定位系统获批上市
2026年1月29日,国家药品监督管理局批准了杭州微引科技有限公司的CT引导穿刺手术定位系统注册申请。该产品由主机和工作站组成,用于CT引导的成人肺部及腹部穿刺手术过程中穿刺针的定位和进针控制。该产品可以辅助医生提升穿刺水平。
二、NMPA最新获批器械产品明细
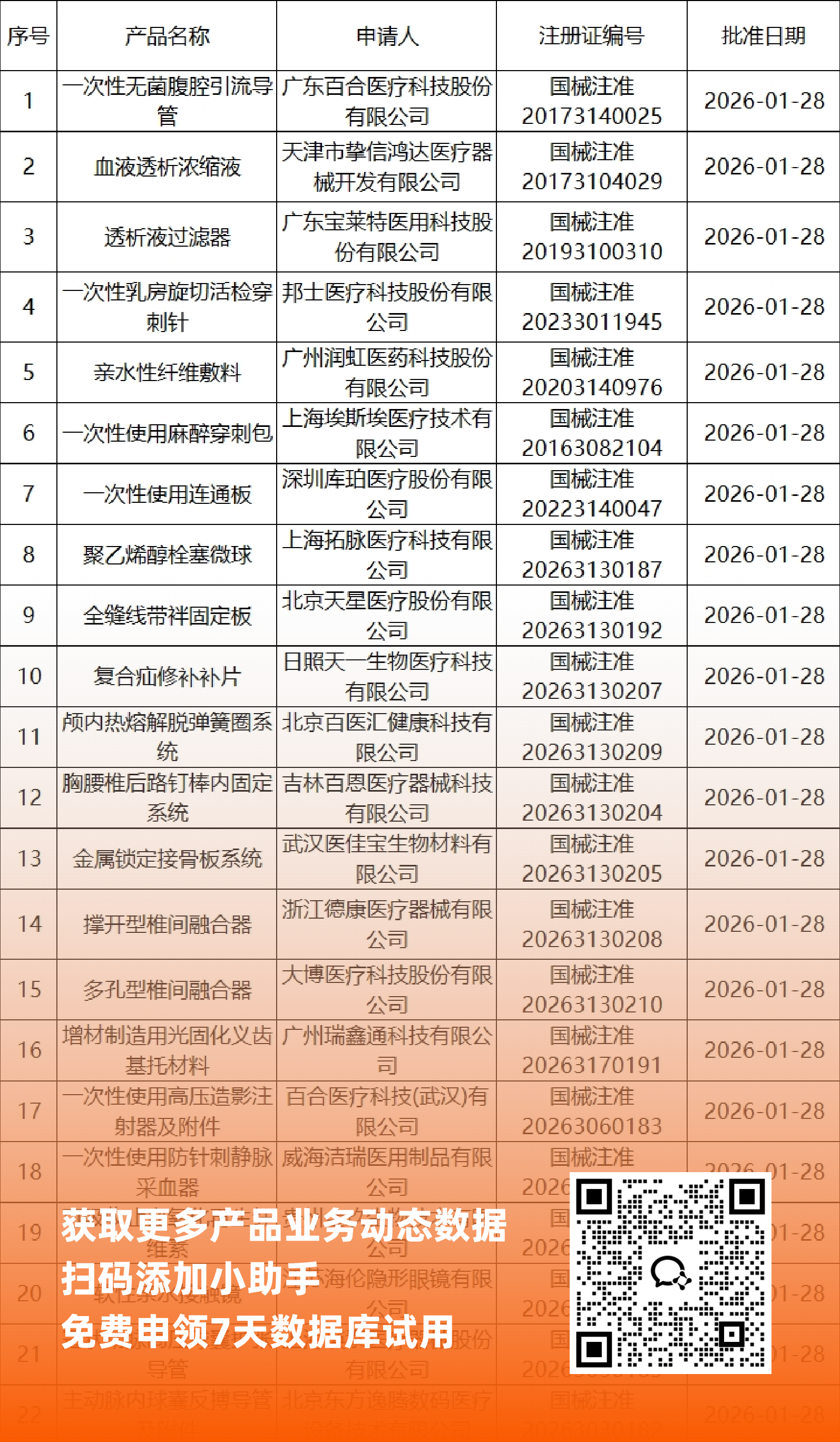
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。