
商务合作

动脉网APP
2026年2月13日至2月26日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及6个器械获FDA批准,4个器械获欧盟及其它批准,另有430个器械获NMPA批准注册文件。
海外获批
一、FDA
1. Catalyst OrthoScience宣布其Archer®患者特定肩关节置换手术器械获得FDA 510(k)许可
专注于肩关节置换术的医疗技术公司Catalyst OrthoScience Inc近日其Archer®患者专用器械(PSI)获得了美国FDA 510(k)许可。该产品由Catalyst与3D-Side合作开发,包含一套完整的肱骨和肩胛盂导板,能够根据每位患者的解剖结构进行定制,帮助骨科医生在手术中以更高的精确性、一致性和信心实施3D术前规划。Catalyst是少数几家提供针对肩胛盂和肱骨的患者专用导板的公司之一。当与Archer® 3D规划软件配合使用时,Archer PSI可提高术前规划的准确性并提升术中效率。它适用于解剖型和反向肩关节手术,使医生能够在保持高效工作流程的同时定制植入物位置。Catalyst首席技术官Ephraim Akyuz强调,将PSI整合到Archer系统中是为外科医生提供临床和运营价值的重要进步,可实现更精准的术前规划执行并节省宝贵的手术时间。Catalyst已开始通过选定的外科医生合作伙伴对Archer PSI进行有限市场发布。
2. Allurion获得美国FDA批准
Allurion Technologies宣布,FDA已批准其 Allurion Gastric Balloon System的上市前批准申请。公司创始人兼首席执行官Shantanu Gaur博士强调,这一批准标志着美国肥胖症护理领域的一个重要里程碑,旨在通过帮助患者减重、保持肌肉和防止体重反弹,实现代谢健康的减重效果。Allurion智能胶囊受到50多项全球专利保护,为GLP-1药物和减肥手术提供了一种非侵入性替代方案。患者在短暂的门诊就诊期间吞服该胶囊,无需手术、内窥镜检查或麻醉,胶囊会在胃中停留约四个月,通过增强饱腹感来减少食物摄入。在此期间结束后,胶囊会自然排出体外,两个月后可再次服用另一粒胶囊。这种疗法通过单次给药提供大约四个月的治疗效果,不同于每日或每周用药的方案。
3. 全球首款轻量化肝脏脂肪定量检测设备获批
意领科技有限公司正式宣布,旗下FattaLab®肝脏脂肪测量仪获得美国食品药品监督管理局(FDA)510(k)注册批准。作为全球首款轻量化肝脏脂肪定量检测设备,此次获批标志着中国原创肝脏健康监测技术正式迈入国际消费医疗赛道,推动肝脏健康管理进入精准、便捷、可及的3.0时代。依托南京江宁的全球超级工厂与产业化基地,FattaLab®将快速实现规模化交付,服务全球家庭与健康管理市场。FattaLab®聚焦脂肪肝早筛与长期管理痛点,采用AutoIntra‑FocusFusion专利肝脏脂肪检测算法,搭配自动ROI调节技术,可有效排除非肝脏组织干扰,30秒快速输出定量检测结果。设备仅重约120克,无线便携、操作极简,大幅降低对专业人员与场地的依赖,真正实现医疗级检测从医院到家庭、社区、健康管理中心等多元场景的无缝延伸,尤其适配肥胖人群、代谢综合征人群的常态化监测需求。
4. Lex Dx获得 FDA 510(k)认证及 CLIA豁免,用于即时检测 PCR系统和呼吸道测试
Lex Diagnostics宣布,其Velo即时分子诊断系统和针对甲型流感、乙型流感及COVID-19的多重检测已获得FDA的510(k)许可和CLIA豁免。该基于卡盒的系统于今年6月提交给FDA,利用超快速PCR技术可在六到十分钟内从拭子样本中提供实验室质量的结果。Lex Dx首席执行官Ed Farrell强调,Velo系统将通过使医疗保健提供者获得快速且高质量的结果来变革即时检测,从而促进更快的临床决策和更好的患者预后。总部位于英国的TTP集团旗下的Lex Diagnostics计划今年在美国启动商业活动,该系统适合集成到包括初级保健、紧急护理诊所、药房和医生办公室实验室在内的各种医疗环境中。去年投资Lex Diagnostics并计划在FDA批准后以高达1.4亿美元收购该公司的QuidelOrtho预计,Velo系统在克服初始产品推出挑战后将提升其毛利率。
5. 美敦力宣布FDA批准Infuse™骨移植材料用于一至两节段的经椎间孔腰椎椎间融合术(TLIF)脊柱手术
美敦力(Medtronic)宣布其INFUSE™骨移植产品在经椎间孔腰椎椎体间融合术(TLIF)中获得FDA上市前批准(PMA),适用于L2-S1节段的一个或两个水平的手术,并兼容PEEK和钛合金椎间融合器。这一批准增强了INFUSE™的多功能性,使其成为唯一获得PMA批准的生长因子骨移植产品,可用于ALIF、OLIF以及现在的TLIF手术,同时也是唯一获批用于脊柱融合的产品,包括双节段TLIF结构。INFUSE™的TLIF适应症于2024年4月获得FDA突破性设备认定,认可了其在治疗退行性腰椎疾病方面的潜在优势。该认定促进了与FDA的深入合作并获得了优先审查。美敦力于2025年8月18日提交了一份小组跟踪PMA申请,FDA在180天后的2026年2月13日批准了该申请,进一步凸显了支持INFUSE™在TLIF应用中的强有力临床证据。
6. 美敦力获得FDA批准的Stealth AXiS™手术系统,这是首个用于脊柱手术的集成规划、导航和机器人平台
美敦力宣布其Stealth AXiS™手术系统获得美国食品药品监督管理局(FDA)批准。这一下一代平台集成了规划、导航和机器人技术,专为美国的脊柱手术设计。该系统在等待监管机构批准的情况下,还计划支持未来的颅脑和耳鼻喉科应用,适应不同外科医生的偏好、临床复杂性和护理环境,能够在医院和门诊手术中心使用,而无需依赖多种独立的技术。基于美敦力在手术导航和机器人领域50年的专业经验,Stealth AXiS™将熟悉的导航工作流程与模块化的机器人设计相结合,使医疗机构能够从基础功能起步,并随着临床需求的变化扩展能力。脊柱手术专家、美敦力付费顾问小罗纳德·A·莱曼博士强调,该系统通过提高精确性和适应性,解决了脊柱手术中的一项关键挑战,推动了导航与机器人技术的整合进程。
二、欧盟及其它
1. 锦波生物胶原蛋白产品获境外医疗器械注册证
锦波生物发布公告称,公司近日获得马来西亚主管当局颁发的D类医疗器械注册证,获批产品为重组Ⅲ型人源化胶原蛋白冻干纤维,此次获批产品规格丰富,涵盖了2mg/瓶、4mg/瓶、6mg/瓶、8mg/瓶、10mg/瓶、12mg/瓶、16mg/瓶、20mg/瓶以及24mg/瓶,共计9个不同规格。此次获证标志着锦波生物的胶原蛋白产品正式获得进入马来西亚市场的资质。
2. 健世科技:两款产品获得新西兰注册批准
健世科技在港交所公告,其两款产品经导管主动脉瓣置换系统Ken-Valve、经血管三尖瓣置换系统LuX-Valve Plus,近日成功取得新西兰药品和医疗器械安全局的注册批准。这一成果标志着健世科技在医疗器械领域的研发与注册工作取得重要进展,两款产品具备在新西兰上市销售的资格。目前,健世科技正积极推进这两款产品在新西兰的商业化进程,力求尽快将产品推向市场,为当地患者提供更先进的治疗选择,同时也为公司开拓国际市场、提升国际影响力奠定基础。
3. Alpha Tau Medical获得日本市场批准,用于治疗无法切除的局部晚期或局部复发性头颈癌的Alpha DaRT®
Alpha Tau Medical是创新的阿尔法辐射癌症疗法Alpha DaRT®的开发者,近日获得日本厚生劳动省颁发的监管上市许可(Shonin),用于治疗无法切除的局部晚期或复发性头颈部癌症。此项批准是在日本药品和医疗器械管理局(PMDA)审核后授予的,标志着Alpha DaRT平台首次在以色列以外地区获得批准。作为批准的一部分,Alpha Tau将在日本五个领先的临床中心开展一项涉及66名患者的上市后监测(PMS)研究。该研究旨在进一步评估Alpha DaRT在真实世界环境中的安全性和临床表现,并与日本医生合作生成更多证据。Alpha Tau首席执行官Uzi Sofer强调了这一里程碑的重要性,指出日本在头颈肿瘤学方面的临床专长,并对HekaBio和六个日本医学协会在整个审批过程中的支持表示感谢。
4. 中生北控生物科技附属中生医疗自主研发的BioCyte系列流式细胞仪获发马来西亚医疗器械注册证
中生北控生物科技附属中生医疗自主研发的BioCyte系列流式细胞仪,近日成功获得马来西亚医疗器械注册证(编号IVDA9463526–225393),标志着该产品具备在马来西亚合法上市、销售及使用的资格。流式细胞技术广泛应用于临床诊断及科研领域,BioCyte系列凭借稳定性能及检测准确性已在国内市场获得应用。马来西亚对医疗器械准入有严格监管标准,中生医疗依当地法规完成产品检测、技术资料提交及审核程序,产品将通过当地授权代表推进市场布局。此次获证有助于推动产品拓展至东南亚市场,提升集团在国际市场的品牌影响力及市场覆盖范围,符合集团国际化发展策略。
国内获批
一、NMPA最新获批器械产品明细
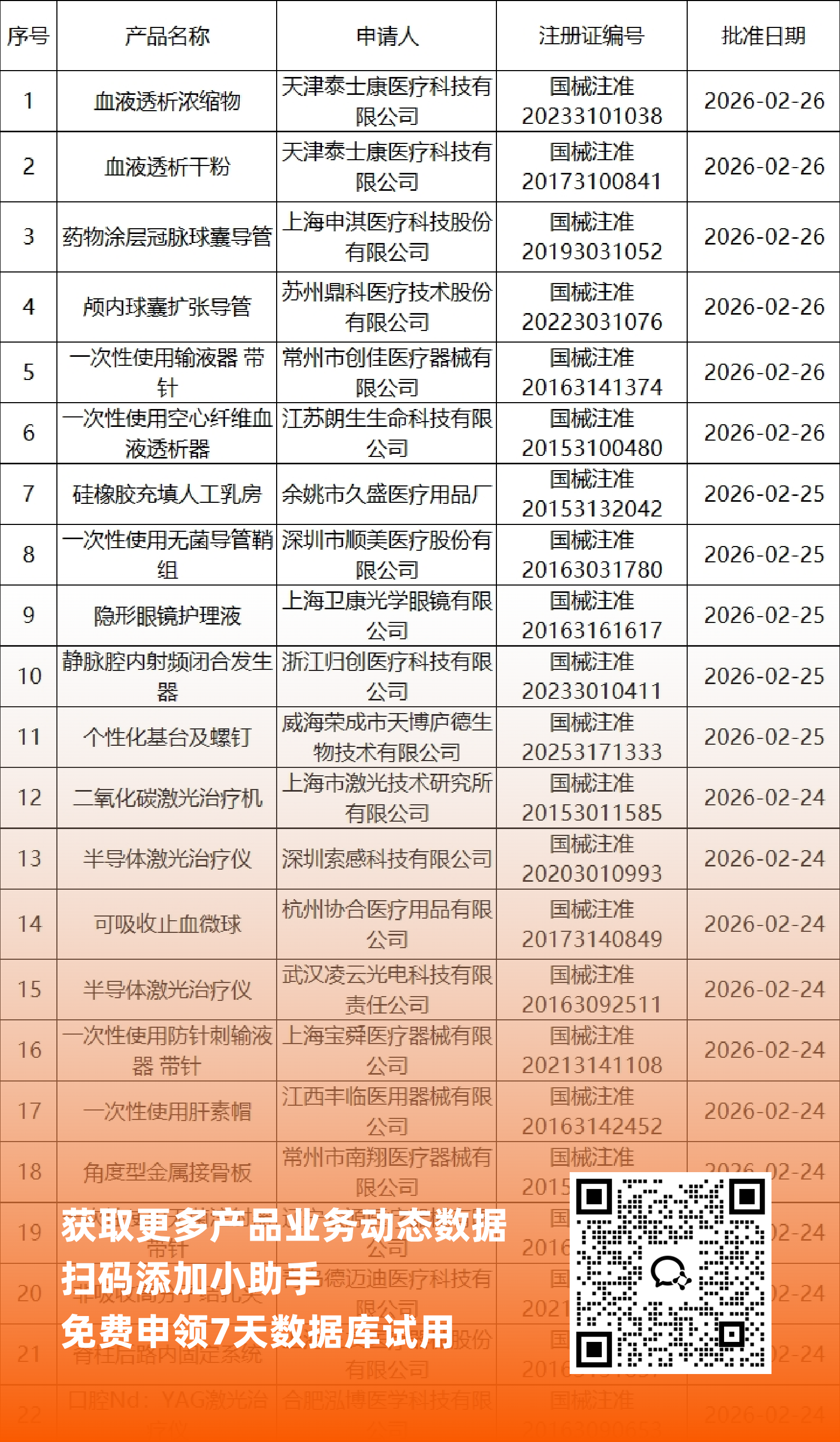
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。