
商务合作

动脉网APP
2026年3月13日至2026年3月19日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及6个器械获FDA批准,2个器械获NMPA创新产品批准,另有286个器械获NMPA批准注册文件。
海外获批
一 、FDA
1. 首次牙科MRI设备获得FDA批准
Dentsply Sirona和西门子医疗宣布其牙科核磁共振成像系统 MAGNETOM Free.Max Dental Edition 已获得美国食品药品监督管理局 (FDA) 的批准。公告强调了一项临床试验的关键发现,验证了该系统在各类牙科专业领域的潜力。试验突出了该系统针对牙科成像需求的专门特性,包括专注于牙颌面结构的视野范围,能够在不捕捉脑组织的情况下实现精确成像。临床试验展示了该系统区分活动性炎症与健康组织和疤痕组织的能力,并能够以非侵入方式评估牙髓活力,从而补充了椅旁测试和临床观察。此外,该系统还可以对牙齿进行成像并评估其相对于邻近牙齿和附近神经的位置。MAGNETOM Free.Max Dental Edition 标志着牙科成像领域的一项重大进步,它提供了其他成像方法难以清晰显示的牙科结构详细信息,且没有电离辐射的相关风险。
2. 美敦力宣布FDA批准MiniMed Flex™,这是该公司最小的胰岛素泵,采用首款智能手机控制设计
美敦力宣布其下一代胰岛素泵MiniMed Flex™获得FDA批准。这款小巧、可通过智能手机控制的设备约为之前MiniMed™ 780G系统的一半大小,旨在无缝融入日常生活。MiniMed Flex™是该公司首款无屏幕胰岛素泵,由糖尿病患者共同参与开发,以确保提供直观且适应生活方式的使用体验。它配备了先进的SmartGuard™自适应算法和Meal Detection™技术,可实时自动调整和校正胰岛素输送,临床表现超越了全球范围内对葡萄糖目标范围内时间(Time in Range)的推荐标准。在商业发布时,MiniMed Flex™将兼容最新的传感器产品组合,包括Simplera Sync™传感器和雅培的Instinct传感器,进一步提升其功能性和用户体验。
3. Mammotome获得FDA批准,推出行业首创的室内MR真空辅助乳腺活检系统及全新HydroMARK™ Plus MR活检部位标记物
Mammotome已获得FDA批准,推出了两项基于磁共振引导的乳腺活检创新技术:Mammotome Prima™ MR双真空辅助乳腺活检系统和HydroMARK™ Plus磁共振乳腺活检部位标记物。Mammotome Prima™ MR是业界首个设计为可直接放置在MRI扫描室患者旁边使用的系统,能够提升临床医生的协作与沟通效率,同时在整个手术过程中保持对患者的专注。HydroMARK™ Plus标记物专为与Mammotome Prima™系统的通用定位装置配合使用而设计。继在欧洲成功推出后,这两款产品将在2026年乳腺影像学会(SBI)研讨会上向美国临床医生展示,提供乳腺活检技术和患者护理方面的进步。
4. Endo Tools Therapeutics获得 FDA 510(k)许可,用于下一代 endomina® EZFuse系统
内窥镜医疗设备开发商Endo Tools Therapeutics宣布,美国食品药品监督管理局(FDA)已为其下一代endomina® EZFuse系统授予了510(k)许可。这项新技术通过更直观的设计增强了公司的缝合平台,能够更快、更高效地完成胃肠道软组织的对合程序。ETT首席执行官Alexandre Chau强调,EZFuse系统代表了一个重要的里程碑,引入的改进简化了工作流程并提升了医生的使用体验。早期的手术经验表明,EZFuse系统显著减少了缝合时间,将总手术时间缩短了多达50%。这使医生能够更高效地完成手术,而无需改变其既定方法。该系统的单动作缝合机制通过消除不必要的步骤简化了工作流程,减轻了工作人员和操作负担。
5. 沛嘉医疗DCwire微导丝获FDA 510(k)许可
沛嘉医疗发布公告,其附属公司加奇生物独立设计开发的DCwire®微导丝,已成功获得美国食品药品监督管理局(FDA)的510(k)许可。这一许可标志着DCwire®微导丝在安全性、有效性等方面得到了FDA的认可,具备进入美国市场的资格。作为沛嘉医疗-B首个获得FDA许可的产品,DCwire®微导丝不仅彰显了公司在医疗器械研发领域的实力,更是公司全球化战略推进过程中的一个重要里程碑,为沛嘉医疗进一步拓展国际市场、提升品牌影响力奠定了坚实基础。
6. 强生获得TECNIS PureSee人工晶状体的白内障手术批准
强生已获得美国食品药品监督管理局(FDA)对其TECNIS PureSee人工晶状体(IOL)的批准,这是一种专为白内障手术设计的扩展焦深(EDOF)镜片。该镜片不仅解决了与白内障相关的视力障碍,还改善了老花眼症状——一种影响眼睛近距离聚焦能力的状况。预计将于今年晚些时候在美国上市,TECNIS PureSee IOL提供更广的视力范围,支持清晰的远距离和中距离视力,并具备一定的近视力能力。临床研究表明,大多数患者在植入后视觉干扰极小。此外,该镜片保持了与非球面单焦点IOL相当的对比敏感度,在低光或雾天条件下区分物体尤为关键,确保术后视力更加清晰可靠。基于TECNIS平台,它结合了先进的光学设计和专有材料,旨在减少患者对眼镜的依赖。
国内获批
一、创新器械获批
1. 首款侵入式脑机接口医疗器械获批上市
2026年3月13日,国家药监局批准了博睿康医疗科技(上海)有限公司植入式脑机接口手部运动功能代偿系统创新产品注册申请,实现脑机接口医疗器械全球首发上市,标志着国际首个侵入式脑机接口医疗器械进入临床应用阶段。该产品由脑机接口植入体、植入式脑电电极套件、脑电信号收发器、气动手套设备、一次性手术工具包、脑电解码软件、医用测试软件、临床管理软件组成。适用于颈段脊髓损伤所致四肢瘫患者,通过气动手套设备辅助实现手部的抓握功能代偿。患者需满足以下条件:18岁到60岁,C2~C6颈段脊髓损伤评级A~C级的四肢瘫,疾病确诊超过1年且经规范治疗后病情稳定至少6个月,手部无法完成抓握,上臂尚存部分功能。该产品采用硬脑膜外微创植入与无线供能通信技术,临床试验结果显示,受试者通过该产品实现了手部抓握能力的明显提高,进而改善患者生活质量。
2. 植入式眼部肌肉神经刺激器获批上市
2026年3月17日,国家药品监督管理局批准了超目科技(北京)有限公司的植入式眼部肌肉神经刺激器注册申请。该产品由刺激器、接收线圈、电极阵列、环状电极和内磁铁组成,与特定体外供电设备联合使用,用于8周岁及以上患者先天性水平型眼球震颤症状的改善。该产品采用植入式眼外肌神经肌肉刺激技术,通过电极对眼外直肌的电刺激,以改善水平型眼球震颤症状,与现有临床治疗方案相比具有局部创伤小、可控性较强、治疗效果稳定的特点,为全球首创产品。该产品的上市为先天性水平型眼球震颤症状改善提供了新的治疗路径。
二、NMPA最新获批器械产品明细
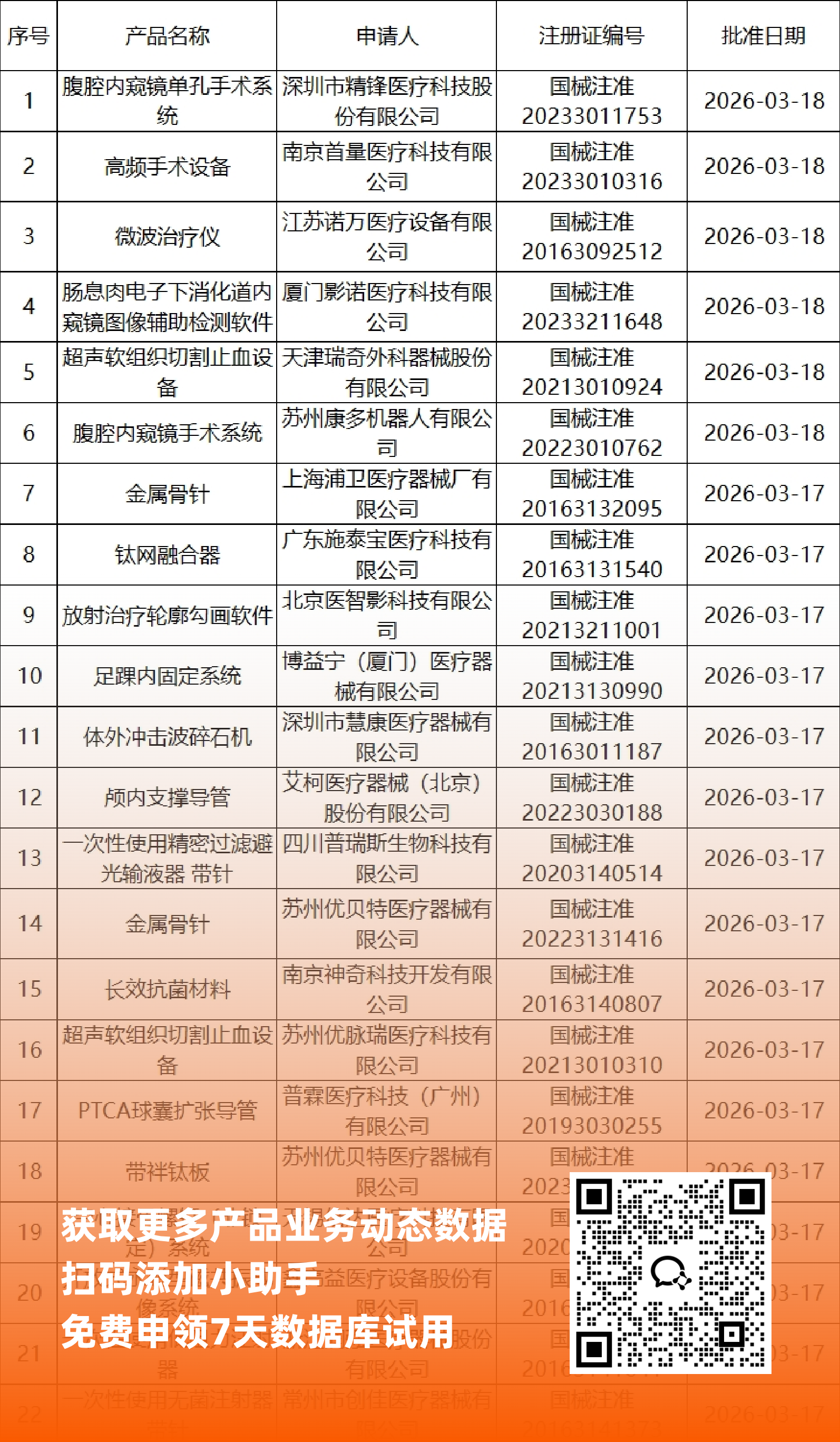
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。