
商务合作

动脉网APP
2026年3月20日至2026年3月26日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及3个器械获FDA批准,2个器械获NMPA创新产品批准,另有346个器械获NMPA批准注册文件。
海外获批
一 、FDA
1. FDA批准了飞利浦在复杂微创心脏瓣膜修复过程中提供实时指导的人工智能解决方案
全球健康技术领导者皇家飞利浦宣布其搭载DeviceGuide的EchoNavigator R5.0获得FDA 510(k)许可。DeviceGuide是一款由人工智能驱动的软件解决方案,该工具在复杂的微创二尖瓣修复手术中提供实时引导,这是介入心脏病学中技术要求极高的领域。DeviceGuide能够实时跟踪并可视化二尖瓣修复设备,并与飞利浦的Azurion影像引导治疗平台集成。该平台将影像、实时数据和智能软件整合到统一的工作流程中,提升了微创手术的一致性、效率和信心。DeviceGuide由飞利浦与结构性心脏创新领域的领导者爱德华生命科学合作开发,结合了飞利浦在影像和人工智能方面的专业知识以及爱德华在心脏瓣膜治疗开发中的技术优势。双方共同优化了二尖瓣经导管缘对缘修复(M-TEER)工作流程的影像引导,使这些手术更加直观和高效。DeviceGuide将在2026年美国心脏病学会(ACC)会议上展出。
2. CephX宣布获得FDA批准用于3D成像,并通过与DEXIS和Greyfinch的整合扩展其全球AI成像生态系统
Orca Dental AI,一家在人工智能驱动的正畸成像领域处于领先地位的公司,同时也是CephX平台的创建者,于2026年3月24日宣布获得了FDA对3D成像的批准。这一成就标志着该公司在将先进的人工智能诊断工具整合到日常临床实践方面迈出了重要的一步。凭借这一新批准,CephX成为唯一一家拥有FDA批准的2D和3D成像技术的正畸人工智能诊断支持公司。这一进展巩固了Orca Dental AI在市场中的地位,使其能够为正畸专业人士提供更全面的成像解决方案。该批准凸显了公司对创新和法规遵从的承诺,确保其技术在临床使用中符合最高的安全性和有效性标准。
3. 【里程碑】全球首创!一体化定位攻克AR锚定难题,JenaValve心脏瓣膜系统FDA获批
JenaValve研发的Trilogy经股动脉主动脉瓣反流(AR)专用介入瓣膜系统获美国FDA上市批准,用于治疗高危症状性重度AR患者,成为美国首个且唯一获此专门适应症批准的TAVR系统,此前已获欧盟CE认证。AR患者长期面临治疗“真空”,传统TAVR瓣膜因锚定机制依赖径向支撑力,难以用于AR患者,风险极高。Trilogy系统历经五代技术迭代,其核心价值在于全球首创的“定位键”设计,通过“叶式锚定”机制,主动精准捕获并夹持无钙化主动脉瓣叶,有效固定瓣膜并抵抗移位,解决了AR介入治疗的锚定难题,为高危AR患者提供了安全有效的微创治疗方案。
国内获批
一、创新器械获批
1. 经导管二尖瓣夹系统获批上市
2026年3月24日,国家药品监督管理局批准了应脉医疗科技(上海)有限公司经导管二尖瓣夹系统创新产品注册申请。该产品由二尖瓣夹及导管输送系统、可操控导引导管组成。二尖瓣夹及导管输送系统由二尖瓣夹、输送导管和可操控套管组成,二尖瓣夹各部件材料包括钴铬合金、镍钛合金、钛合金、纯钛和PET。可操控导引导管由导引导管、扩张器、紧固螺钉和硅胶垫组成。二尖瓣夹及导管输送系统根据同步控制夹片或单独控制夹片功能分为I型导管输送系统和II型导管输送系统。可操控导引导管根据手柄差异分为I型可操控导引导管和II型可操控导引导管。该产品采用经皮方式,适用于经心脏团队评估后认为存在外科手术高风险,且二尖瓣瓣膜解剖结构适合的退行性二尖瓣反流 (MR≥3+)患者。
2. 二氧化碳造影压力注射套装获批上市
2026年3月24日,国家药品监督管理局批准了阿迈特医疗器械(北京)股份有限公司二氧化碳造影压力注射套装创新产品注册申请。该产品由造影注射器、输注管路、双锁口过滤器三部分组成。造影注射器由带锁定装置的6%(鲁尔)内圆锥接头(进气口)、隔膜式压力表、开关旋钮、外壳、螺杆式调节手柄、带锁定装置的6%(鲁尔)外圆锥接头(出气口)、储气筒、活塞座组成。产品附件包括输注管路、双锁口过滤器。该产品用于向肾动脉、髂动脉、下肢动脉、前臂静脉、下腔静脉及髂静脉注射二氧化碳(纯度大于等于99.999%)进行血管造影。适用于碘造影剂过敏人群、慢性肾脏病三期至五期患者、甲状腺功能亢进(甲亢)患者。
二、NMPA最新获批器械产品明细
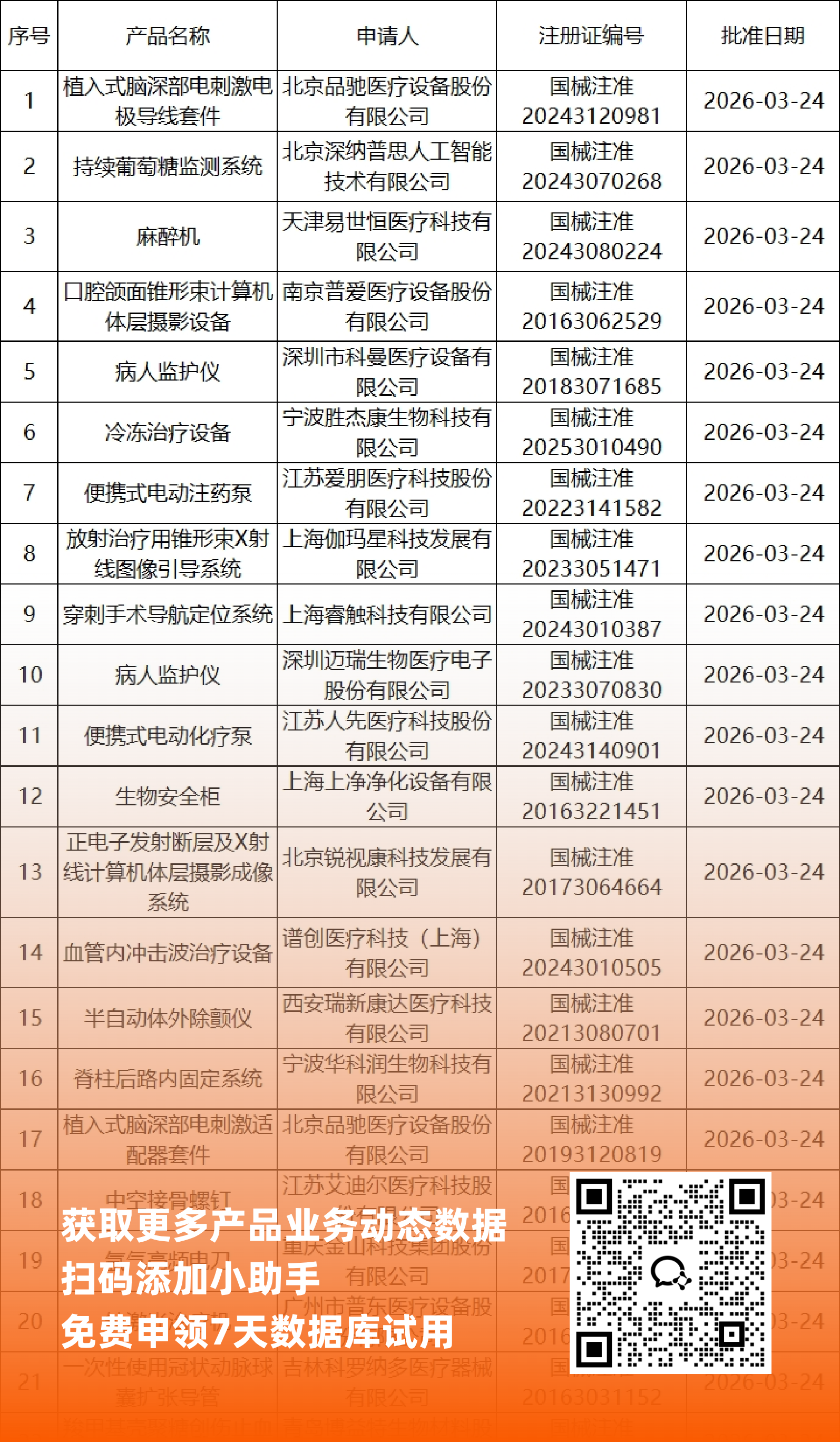
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。