
商务合作

动脉网APP
2026年3月27日至2026年4月2日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及7个器械获FDA批准,1个器械获NMPA创新产品批准,另有374个器械获NMPA批准注册文件。
海外获批
一 、FDA
1. 全球首个脑静脉支架获批:Serenity River支架为颅内高压患者带来新希望
2026年3月31日,Serenity Medical宣布其研发的River脑静脉支架获美国FDA人道主义器械豁免批准,成为全球首个获批治疗成人特发性颅内高压(IIH)的脑静脉支架,适用于对药物治疗抵抗或不耐受的严重IIH患者。IIH是罕见病,传统治疗以药物和反复腰椎穿刺为主,但部分患者无反应或无法耐受,外科手术创伤大、风险高且缺乏专用器械。River支架是自膨胀式镍钛合金支架,专为脑静脉窦系统设计,通过经股静脉路径植入恢复静脉回流、降低颅内压。其构造特点包括可变径向支撑力、低金属表面积、柔性连接结构,可适应静脉窦变化、降低血栓风险、顺应自然弯曲。
2. Zeto宣布Zeto New Wave™获得FDA 510(k)许可,推动门诊EEG效率提升
医疗技术公司Zeto, Inc最新EEG系统Zeto New Wave™已获得美国FDA 510(k)许可,专为门诊诊所和家庭使用设计。美国患者经常面临EEG预约的长时间等待,导致诊断和治疗延误,而诊所在缺乏专业EEG技术员的情况下,依赖缓慢且笨重的传统设备。Zeto New Wave™旨在通过提供覆盖全头部、适用于成人和儿童的用户友好型门诊EEG解决方案来应对这些挑战。该系统包含基于10-20系统的21个软尖电极,并配有内置显示屏和控制功能的紧凑型记录设备。它能够同步捕捉视频和音频,还可选配心电图(ECG)、眼电图(EOG)、肌电图(EMG)、方向传感器以及用于事件相关电位(ERP)的外部触发信号。Zeto New Wave™专为最长2.5小时的短期记录设计,提供了全面的解决方案以优化EEG测试和后续护理流程。
3. FDA批准全球最小除颤导线,1.6mm“铅笔芯”,改写心律失常治疗格局
FDA批准美敦力OmniaSecure除颤导线扩展适应症,允许其植入左束支区域,这是FDA史上首次批准可用于LBB区域的除颤导线。该导线直径仅1.6mm,是全球最小无腔除颤导线,比传统导线更细,能减少血管损伤,适配更细血管,为12岁以上青少年患者提供治疗可能,且保持了柔韧性和抗疲劳性。它并非首次获批,2025年4月已获FDA批准用于右心室植入,此次扩展适应症后,成为全球首个可植入左束支区域的除颤导线,既能治疗致命心律失常,又能实现“传导系统起搏”,简化手术流程,减少心功能损伤。
4. Restore Robotics获得FDA 510(k)批准,新增两款达芬奇Xi®机器人手术器械
Restore Robotics宣布已获得美国FDA的更多510(k)许可,可再制造两款达芬奇Xi机器人手术器械,进一步扩展其产品组合并巩固其在机器人器械再制造领域的领导地位。这些许可符合公司为医院和手术中心提供相较于原始设备制造商(OEM)购买全新机器人器械更具成本效益、高质量且可持续替代方案的使命。Restore Robotics首席执行官Clif Parker强调,这些批准标志着通过使医疗服务提供者能够在保持性能和可靠性的同时降低成本,从而改变机器人手术经济性的重大进展。通过与Encore Medical Device Repair合作,Restore Robotics将扩大其再制造器械在全国范围的分销,帮助医院在更广泛的机器人器械支出上实现更大的节省。参与该计划的机构通过器械重复使用,能够降低成本并提高可持续性,从中受益。
5. 罗氏获得FDA 510(k)批准,用于cobas® c703和cobas® ISE neo新一代分析单元,提升实验室的效率和能力
罗氏宣布其最新的分析单元cobas® c 703和cobas® ISE neo获得了美国FDA的510(k)许可。这些单元是可扩展和模块化的cobas® pro集成解决方案的一部分,旨在提升实验室自动化水平,并应对人员短缺、空间有限和测试量增加等挑战。cobas® c 703具备高通量效率,每小时可处理多达2000个测试,并支持多达70个试剂位置以优化测试性能。cobas® ISE neo每小时可执行多达1800个测试,通过自动维护减少人工干预。罗氏诊断北美区总裁兼首席执行官Brad Moore强调了罗氏致力于提供解决方案,帮助实验室在不降低性能的情况下处理更多样本,从而改进工作流程并提升患者护理水平。这些新单元体现了罗氏以科学为引领、提供创新诊断解决方案的决心。
6. 波士顿科学获得FDA批准的Asurys™液体管理系统
波士顿科学宣布,Asurys™流体管理系统已获得FDA 510(k)许可。这一新系统旨在为内窥镜泌尿外科手术(如输尿管镜检查、膀胱镜检查、经皮肾镜取石术(PCNL)和良性前列腺增生(BPH)治疗)提供冲洗和扩张功能。输尿管镜检查常用于诊断和治疗肾结石等泌尿道问题,但在此过程中需保持清晰视野的流体流动,同时维持较低的肾内压(IRP),以确保患者安全,这是一大挑战。高肾内压可能导致包括全身炎症反应综合征(SIRS)、败血症和肾脏损伤在内的并发症。Asurys系统是波士顿科学公司StoneSmart™解决方案生态系统的一部分,当与具备IRP监测功能的LithoVue™ Elite一次性数字柔性输尿管镜配合使用时,可有效帮助管理手术过程中的肾内压。
7. 美敦力获得FDA批准,用于颅脑和耳鼻喉手术的Stealth AXiS™手术系统
美敦力继其在今年二月获得脊柱手术批准后,最近又获得了FDA对其Stealth AXiS™手术系统在颅脑和耳鼻喉科手术中的许可。该系统将手术规划、导航和机器人技术集成到一个统一的智能平台中,提高了手术精度,并为外科医生在复杂手术过程中提供实时洞察。这一批准与美敦力的战略一致,即提供支持多学科手术的互联技术,集中于单一平台。美敦力颅脑和脊柱技术高级副总裁迈克尔·卡特(Michael Carter)强调,该系统通过AiBLE™智能生态系统提供先进的精确性和洞察力。其关键特性是支持人工智能的架构,能够在整个手术过程中实现高级规划和可视化,包括基于AI的自动纤维束成像技术,用于创建患者特定的大脑地图并可视化关键神经通路。该系统还通过GE HealthCare的bkActiv™整合了术中超声,以提供额外的实时数据支持。
国内获批
一、创新器械获批
1. 冷冻消融仪、一次性使用球囊型冷冻消融导管获批上市
2026年3月31日,国家药品监督管理局批准了心诺普医疗技术(北京)有限公司的冷冻消融仪、一次性使用球囊型冷冻消融导管注册申请。冷冻消融仪由冷冻消融仪主机及触摸屏组成。一次性使用球囊型冷冻消融导管由球囊型冷冻消融导管、同轴流体连接管、连接电缆组成。冷冻消融仪与一次性使用球囊型冷冻消融导管联合使用,用于成人患者药物难治性、复发性、症状性的阵发性房颤的治疗。该产品使用顺应性直径可调的球囊,属于国内首创,预期可提高肺静脉封堵成功率。
二、NMPA最新获批器械产品明细
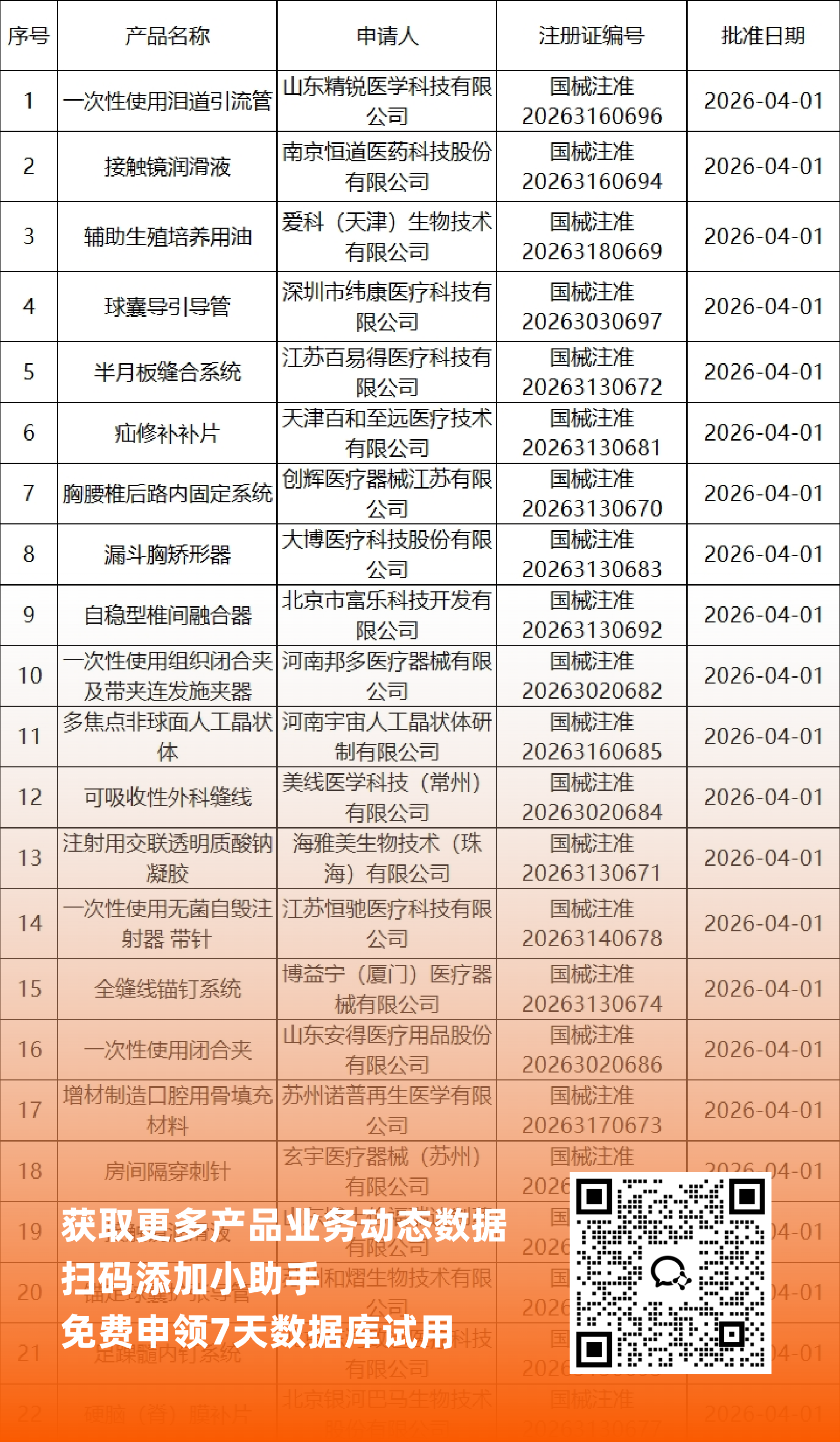
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。