
商务合作

动脉网APP
2026年4月3日至4月9日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及7个器械获FDA批准,5个器械获欧盟及其它批准,另有328个器械获NMPA批准注册文件。
海外获批
一、FDA
1. Sibel Health获得FDA批准的ANNE® Maternal,一个全面且完全无线的母婴监测平台
Sibel Health宣布其ANNE® Maternal平台获得FDA 510(k)许可,这标志着全球首个完全无线、综合性的母婴监测系统的诞生。该平台旨在对母亲和胎儿的健康状况进行持续、同步的追踪,集成了先进的可穿戴传感器技术和临床决策支持工具,目标是将连续的孕产妇监测确立为普遍的护理标准。ANNE® Maternal基于其姐妹产品ANNE® One的成功经验,后者已在家庭和医院环境中获得FDA许可,用于青少年和成人的连续监测。这一全新平台代表了母婴医疗保健领域的重大进步,提供了一种无创且用户友好的解决方案,有助于改善患者预后并优化临床工作流程。
2. MedCAD的AccuStride®获得FDA 510(k)许可,用于新的解剖学小腿区域胫骨/腓骨解决方案
总部位于达拉斯的MedCAD公司已获得FDA 510(k)批准,其AccuStride®小腿胫骨和腓骨系统可帮助外科医生获取针对患者的精密设备。该系统包含定制的规划和手术导板,旨在让骨科医生在单一手术中处理多种病理和截骨术。此次批准紧随MedCAD此前于2025年3月获批的足部和踝关节导板及规划系统,以及2025年11月获批的固定板之后,完善了AccuStride®下肢解决方案,涵盖胫骨/腓骨、足部和踝关节。MedCAD首席执行官兼总裁南希·海尔斯顿强调了该系统在复杂小腿手术中的独特性,并指出骨科专家对此表现出浓厚兴趣。公司预计,这些定制的3D打印设备将减少手术频率和时长,同时确保高质量和持久的效果。AccuStride™系统包括手术导板、固定板和解剖模型,由紫外线固化丙烯酸聚合物或钛合金材料制成。
3. Waters宣布FDA批准了最全面的家用宫颈癌筛查工具——Onclarity HPV自我采样套件和FDA批准的HPV检测方法
Waters宣布,美国食品药品监督管理局(FDA)已批准Onclarity HPV自采样试剂盒,并通过扩展基因分型认证允许BD Onclarity™ HPV检测用于家庭自检。这标志着在提升宫颈癌筛查可及性方面迈出了重要一步。BD Onclarity™ HPV检测被公认为是美国最全面的HPV筛查工具,提供扩展基因分型和全自动化的实验室工作流程。家庭自采样的引入解决了未筛查或筛查不足人群面临的重大障碍,这部分人群约占宫颈癌病例的60%。通过让患者和医生使用Onclarity™ HPV自采样试剂盒,沃特世公司旨在降低全国范围内的宫颈癌风险。这一进展至关重要,因为宫颈癌主要由人乳头瘤病毒(HPV)引起,而通过定期筛查和早期发现HPV,宫颈癌在很大程度上是可以预防的。
4. Royal Biologics宣布其Fibrinet® PRF伤口基质获得FDA批准,用于管理皮肤伤口
再生医学与高级伤口护理领域的领导者Royal Biologics宣布,其Fibrinet® PRF伤口基质已获得FDA批准,用于管理渗出性皮肤伤口,包括糖尿病溃疡和静脉溃疡。这种即时护理系统将患者的血小板和生长因子浓缩为持久的富血小板纤维蛋白基质(PRFM),使临床医生能够创建结构化的自体纤维蛋白支架,直接应用于伤口,以支持自然愈合。在医疗监督下,PRFM基质可局部用于各种伤口,包括糖尿病溃疡、静脉溃疡以及机械或手术清创的伤口。美国医疗保险和医疗补助服务中心(CMS)有一项政策,涵盖具有FDA批准的伤口管理适应症的PRP设备,例如糖尿病溃疡。尽管市面上有许多PRP设备,但Fibrinet® PRF伤口基质是少数几种获得FDA明确批准用于伤口管理的设备之一。
5. Artivion宣布美国FDA批准NEXUS®主动脉弓系统
心脏和血管外科公司Artivion, Inc宣布FDA批准了Endospan Ltd.的NEXUS®主动脉弓系统的上市前批准申请。这一批准使Artivion有可能在90天内收购Endospan。Artivion已获得1.5亿美元的贷款以资助此次收购,并在早期批准后积极评估该选项。NEXUS系统是一种分支型血管内支架移植物,专为微创治疗主动脉弓疾病(包括慢性主动脉夹层)而设计,为选择有限的患者提供了一种开胸手术的替代方案。FDA的决定得到了NEXUS TRIOMPHE IDE试验数据的支持,数据显示高危患者的病灶相关死亡生存率为90%,治疗一年后无致残性中风的比例为90%,因内漏需再次干预的自由率为98%。
6. InVera Medical公司获得FDA批准的InVera输注装置——一种用于慢性静脉疾病硬化剂增强输注的新型非热导管
专注于推进慢性静脉疾病微创技术的医疗器械公司InVera Medical已获得FDA 510(k)批准,推出了InVera输液装置,这是一款新型微创设备,旨在帮助医生更有效地为患病的腿部静脉(包括静曲曲张)提供治疗。CVD影响着四分之一的成年人,若不加以治疗可能导致疼痛性腿部溃疡,仅在美国和欧洲就影响超过1.2亿人。然而,每年仅有1%的静脉疾病患者接受治疗,显示出InVera希望填补的重大护理缺口。InVera输注装置是首个通过机械方式准备静脉壁的设备,可增强硬化剂注入更深的组织层,为CVD患者提供更安全、更有效的治疗方案。与现有的需要多次痛苦注射的热疗法以及通常需要重复操作或永久性胶水植入的非热疗法不同,InVera设备提供了一个前景广阔的替代方案。
7. FDA批准Stereotaxis Synchrony系统用于机器人辅助的血管内手术
Stereotaxis已获得美国食品药品监督管理局(FDA)对其Synchrony系统的批准,该系统是一种旨在提升血管内手术效果的机器人技术。公司也正式推出了该系统,标志着其研发和商业化过程中的重要成就。Synchrony系统旨在提高微创血管介入手术中的精确性和控制力,结合了先进的机器人技术和影像技术。这种集成旨在提高手术精度,同时减少患者和医护人员的辐射暴露。FDA的批准使Stereotaxis能够在美国市场推广和分销该系统,此前在开发过程中已进行过早期临床评估。这一监管里程碑支持了该公司在医疗程序中推进机器人辅助技术的努力。
二、欧盟及其它
1. 海利生物控股子公司瑞盛生物可吸收胶原膜获印度尼西亚注册证
海利生物控股子公司陕西瑞盛生物的GORORISE可吸收胶原膜产品,获印度尼西亚卫生部颁发的医疗器械注册证(编号KEMENKES RI AKL 30602620091),该产品为D类无源无菌医疗器械,是脱细胞基质材料,主要用于口腔种植手术中引导骨组织再生,此前已获中国国家药监局第三类医疗器械注册证及越南注册证。此次在印尼获批,意味着该产品具备了在印尼市场的销售准入资格,有助于海利生物拓展东南亚市场。不过,海利生物提示,该产品尚未在印尼形成销售,未来销售及业绩贡献受海外法规、市场环境、汇率等多重因素影响,存在不确定性。
2. ColonAiQ®正式获批马来西亚MDA注册,东南亚布局再下一国
鹍远生物结直肠癌液体活检产品ColonAiQ®继新加坡、泰国后,再获马来西亚MDA注册批准,斩获东南亚市场第三个官方注册,为当地结直肠癌早期检测筛查与术后监测提供全新无创精准选择。该产品通过检测五个基因甲基化状态,结合荧光探针定量PCR技术,可高效辅助诊断,提供重要参考,且仅需一管血,实现无创、便捷、高灵敏度检测,可用于术后复发风险动态监测,实现全病程管理。此次获批验证了其安全性、有效性和临床性能,彰显了鹍远生物技术实力,也为中国原研IVD产品在国际舞台上的竞争力提供例证。凭借马来西亚战略伙伴的渠道资源与推广能力,ColonAiQ®将快速进入当地市场,服务更多民众。
3. 金属药物支架系统正式获得俄罗斯医疗器械注册证
威高介入集团旗下深圳市金瑞凯利生物科技有限公司自主研发的金属药物支架系统,近日成功通过俄罗斯相关监管部门审核,正式获得俄罗斯医疗器械注册证。这一里程碑标志着该产品品质与安全性获国际认可,为开拓俄罗斯及欧亚市场奠定坚实基础。威高介入坚持创新驱动,严格遵循国际质量标准,此次注册证的取得,不仅彰显了公司在体系与合规方面的实力,更体现了服务全球医疗需求的决心。未来,威高介入将继续推动产品国际化应用,为更多医疗机构和患者提供优质服务。
4. 金属药物支架系统正式获得乌克兰医疗器械注册证
威高介入集团旗下深圳市金瑞凯利生物科技有限公司自主研发的金属药物支架系统,近日通过乌克兰监管部门审核,正式获得乌克兰医疗器械注册证,取得东欧市场准入资质。此次获证体现了威高介入在研发、生产与合规管理方面的综合能力,印证了其服务全球患者的坚定承诺。威高介入始终秉持创新驱动发展的理念,严格遵循国际质量标准。未来,威高介入将继续深耕国际市场,加大研发投入,提升产品品质,以更优质安全的产品服务全球患者,为国产医疗器械走向世界、扎根全球市场筑牢根基。
5. 心脉医疗多款重点产品首次在越南获批上市
心脉医疗多款主动脉介入重点产品在越南注册获批,首次进入越南市场,为业务拓展奠定基础,也标志着公司在东南亚市场取得突破,验证了产品体系的国际竞争力与临床认可度。获批产品包括Cratos®/通天镰™分支型支架、Talos®/通天眼™直管型支架、Minos®/定海塔™腹主动脉支架和Hercules®/通天锤™球囊扩张导管。其中,Cratos®/通天镰™分支型支架是国内首款近端可主动调节的分支型覆膜支架,传承了Castor®分支型支架的一体化分支结构和近端无裸段设计,并在多方面取得显著提升;Talos®/通天眼™直管型支架是全球首款“会呼吸”的覆膜支架,适用于Stanford B型主动脉夹层手术治疗;Minos®/定海塔™腹主动脉支架是国产首款将输送器外鞘直径降低到14F的产品。
国内获批
一、NMPA最新获批器械产品明细
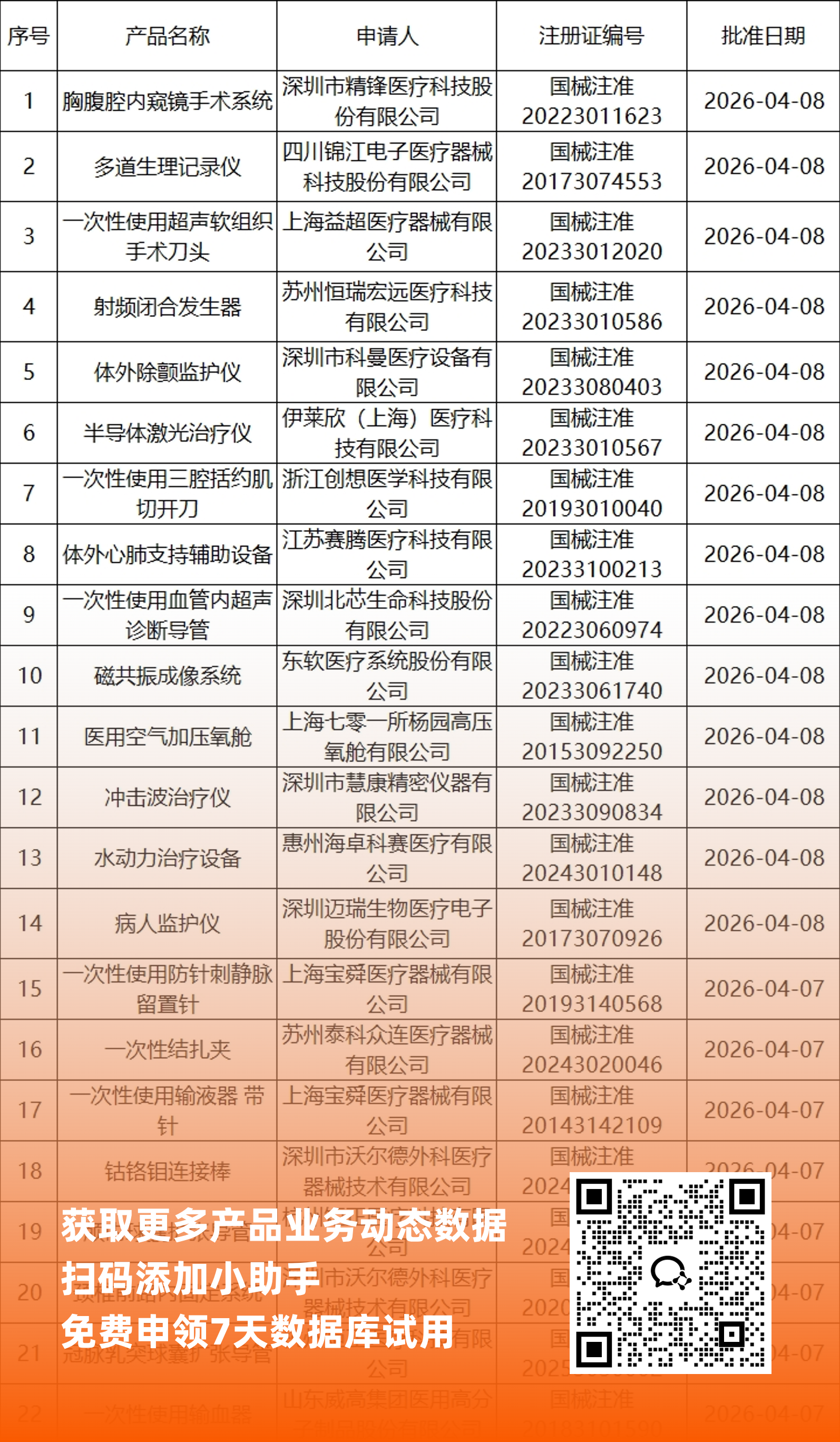
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。