
商务合作

动脉网APP
2026年4月10日至4月16日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及5个器械获FDA批准,5个器械获欧盟及其它批准,另有391个器械获NMPA批准注册文件。
海外获批
一、FDA
1. FDA紧急获批新AI,普通心电图就能揪出心脏“隐形杀手”
美国FDA正式批准Anumana公司全新AI模型,用于检测心脏淀粉样变性(CA)早期迹象,这已是该公司两周内第二次获FDA批准。心脏淀粉样变性是致命“隐形杀手”,因错误折叠的淀粉样蛋白沉积破坏心脏结构功能,引发心力衰竭等,且早期症状隐蔽,常与普通心脏病重叠,大量患者被漏诊、误诊,确诊时多错过最佳治疗时机。此次获批的AI操作简单,只需分析常规12导联心电图,就能快速识别CA高风险患者,此前已获FDA“突破性设备认定”。该AI准确性靠谱,FDA批准基于超大规模多中心研究,覆盖4家医疗系统、超25000名患者,检测成人CA迹象灵敏度达78。
2. Protaryx新型房间隔穿刺设备获FDA批准,心脏介入手术更安全高效
Protaryx Medical自主研发的房间隔穿刺设备获FDA 510(k)许可,正式登陆美国市场。房间隔穿刺术是心脏介入手术关键步骤,传统设备存在操作复杂、风险较高等问题,而Protaryx新产品针对性解决这些痛点:采用零交换递送技术,操作便捷;内置高回声、可伸缩无创定位探针,搭配标准化射频导丝,实现精准穿刺,且兼容性强;临床数据亮眼,安全性有保障。该设备可为二尖瓣修复与置换、左心耳封堵、心律失常消融等多种常见心脏介入手术提供支持。对Protaryx公司而言,此次获批是里程碑式的一步,标志着其产品安全有效,获进入美国市场“通行证”。
3. AIRS Medical的SwiftMR®获得FDA批准,可与OEM深度学习重建解决方案配合使用
AIRS Medical宣布其获得FDA 510(k)批准的、与供应商无关的MRI图像增强解决方案SwiftMR®,已获准与原始设备制造商(OEM)的深度学习(DL)重建管道配合使用。SwiftMR通过两种方式增强了OEM的DL解决方案:当安装了OEM的DL解决方案时,SwiftMR可进一步缩短扫描时间,例如在GE 3T扫描仪上使用AIR Recon DL将脑部扫描从15分钟减少到9分钟。此外,当OEM的DL解决方案未涵盖某些序列时,SwiftMR扩展了覆盖范围,能够在所有脉冲序列和身体部位实现AI驱动的图像增强和扫描时间缩短,并自2023年以来获得了完整的FDA批准。AIRS Medical首席战略官朴智娜强调,SwiftMR额外的扫描时间缩短可能会改变排程实践。产品主管郑宇进指出,通过对多个厂商的OEM DL处理图像进行广泛培训和测试,促成了这一新的FDA批准,确保质量并增强客户对部署SwiftMR与OEM DL解决方案的信心。
4. Cala宣布其下一代TAPS治疗可穿戴设备获FDA批准,用于治疗特发性震颤和帕金森病
生物电子医学领域的领导者Cala®其Cala kIQ® Plus系统已获得FDA批准。该系统是一种先进的可穿戴神经刺激设备,用于管理原发性震颤(ET)和帕金森病(PD)中的动作性手部震颤。新系统引入了创新的治疗模式和自适应校准功能,增强了震颤缓解效果,并通过个性化治疗提供更直观的患者体验。Cala首席执行官Deanna Harshbarger强调了公司通过可穿戴神经调节技术的进步来改善患者疗效与体验的承诺,使患者能够更好地掌控自己的治疗。支持Cala kIQ Plus有效性的最新数据将于2026年4月18日至22日在芝加哥举行的美国神经病学学会(AAN)会议上展示,其中具体报告定于4月20日中部时间上午11点45分进行。Cala还将在AAN 2026会议(展位号5024)上展示Cala kIQ Plus。
5. 沃特世居家检测HPV获FDA 510(k)上市许可
沃特世宣布,其BD Onclarity HPV自采试剂盒及检测法获FDA 510(k)上市许可。该检测产品可居家自行采集样本,大幅提升HPV检测可及性,能识别所有高危致癌型HPV基因型,并在BD COR系统上完成分析。沃特世公司曾与美国国家癌症研究所合作评估其准确性,该检测产品是收购碧迪医疗相关业务所得,已纳入联邦医保、医疗补助及多家商业保险覆盖范围,预计不久可通过处方获得,检测套装可邮寄至患者家中,患者自行采样后寄回实验室分析。沃特世公司副总裁称家用HPV自采检测将改变筛查便利性,利于临床医生更早发现风险、干预治疗。
二、欧盟及其它
1. 呼吸道核酸三联居家自测IVDR获批
苏州雅睿生物旗下迅睿生物Pocket PCR(析速达)产品获欧盟CE-IVDR证书,可家庭自测甲型流感、乙型流感、呼吸道合胞病毒(RSV)三项呼吸道病原体核酸。该产品能精准识别甲流常见亚型,区分甲/乙流感染,快速鉴别婴幼儿、老年人高风险人群常见病诱因;具有CE居家合规、三联检测高效(单样本最快22分钟出核酸级结果)、整合微流控等黑科技、全场景适配等亮点。雅睿生物深耕分子诊断25年,稳居行业头部,正聚焦三大板块持续深耕发力,已构建丰富产品矩阵,此次获证是其全球化布局重要一步,该产品将助力全球公共卫生与家庭健康防护。
2. 健适瑞奇破局电动吻合器同质化——全球首款90°弯转实时智能反馈电动腔镜吻合器欧洲获批
国内电动吻合器市场超三百品牌涌入,同质化严重,进口智能产品又因收费项目“水土不服”难普及。健适瑞奇全球首款90°弯转实时智能反馈电动腔镜吻合器获CE认证,国内NMPA获批在即。该产品以颠覆性技术打破行业内卷僵局,其90°超大弯转设计突破传统角度极限,攻克行业难题,在复杂手术中降低风险,提升患者生存质量,还能节约医疗成本;搭载全智能实时反馈控制系统,以毫米级精度实时感知组织厚度,实现自适应智能吻合,手柄智能显示屏让术者全程可视化精准掌控,针对复杂状况可精准识别异常、实时预警。目前已启动全国多中心临床研究,远销多国。
3. 糖吉医疗胃转流支架系统获菲律宾医疗器械注册证
糖吉医疗自主研发的胃转流支架系统在菲律宾正式获批上市,此前该系统已在多国接连获批,国际化进程提速。这不仅印证了产品安全性与有效性,更彰显中国原创介入减重疗法获全球市场认可,正成长为肥胖与代谢病治疗领域主流方案。作为代谢病介入治疗领军企业,糖吉医疗积极响应“一带一路”倡议,东南亚地区代谢性疾病高发,是公司全球化布局核心区域,此次开拓菲律宾市场完善了其在东盟地区的战略布局。未来,糖吉医疗将持续推进该系统在东盟及更多“一带一路”沿线国家的注册申报与临床落地,助力复制中国成熟诊疗模式。
4. 奥精医疗产品在泰国获得注册证
奥精医疗发布公告称,公司于2025年5月向泰国食品药品监督管理局(TFDA)递交了人工骨修复材料的注册申报资料,近日收到通知,该材料已获批准在泰国上市。此次获得泰国注册证,是奥精医疗海外业务拓展进程中的关键一步,标志着其产品正式获得进入泰国市场的合法资质。作为公司国际化战略的重要成果,这一进展不仅丰富了海外产品矩阵,更将直接推动人工骨修复材料在泰国及东南亚市场的销售布局,为后续深化国际合作、提升全球市场份额奠定基础,对公司海外业务增长具有积极促进作用。
5. 归创通桥ZENFLEX外周血管支架系统、ZYLOX Unicorn血管缝合器系统获巴西ANVISA批准上市
归创通桥自主研发的ZENFLEX™外周血管支架系统、ZYLOX Unicorn™血管缝合器系统获巴西ANVISA批准上市。ZENFLEX™用于治疗外周动脉疾病,设计独特,自欧盟上市后获认可;ZYLOX Unicorn™是国产首款自主研发的血管缝合器,缝合范围广,安全有效,可减少患者制动时间,降低并发症风险。近年来,归创通桥国际化业务发展迅速,商业网络覆盖全球80多个国家和地区,推动多款产品商业化及注册。2025年,其国际化业务营收大幅增长。未来,归创通桥将继续推进创新产品在国际市场的商业化布局,为全球患者提供高质量且可负担的创新医疗器械产品和解决方案。
国内获批
一、NMPA最新获批器械产品明细
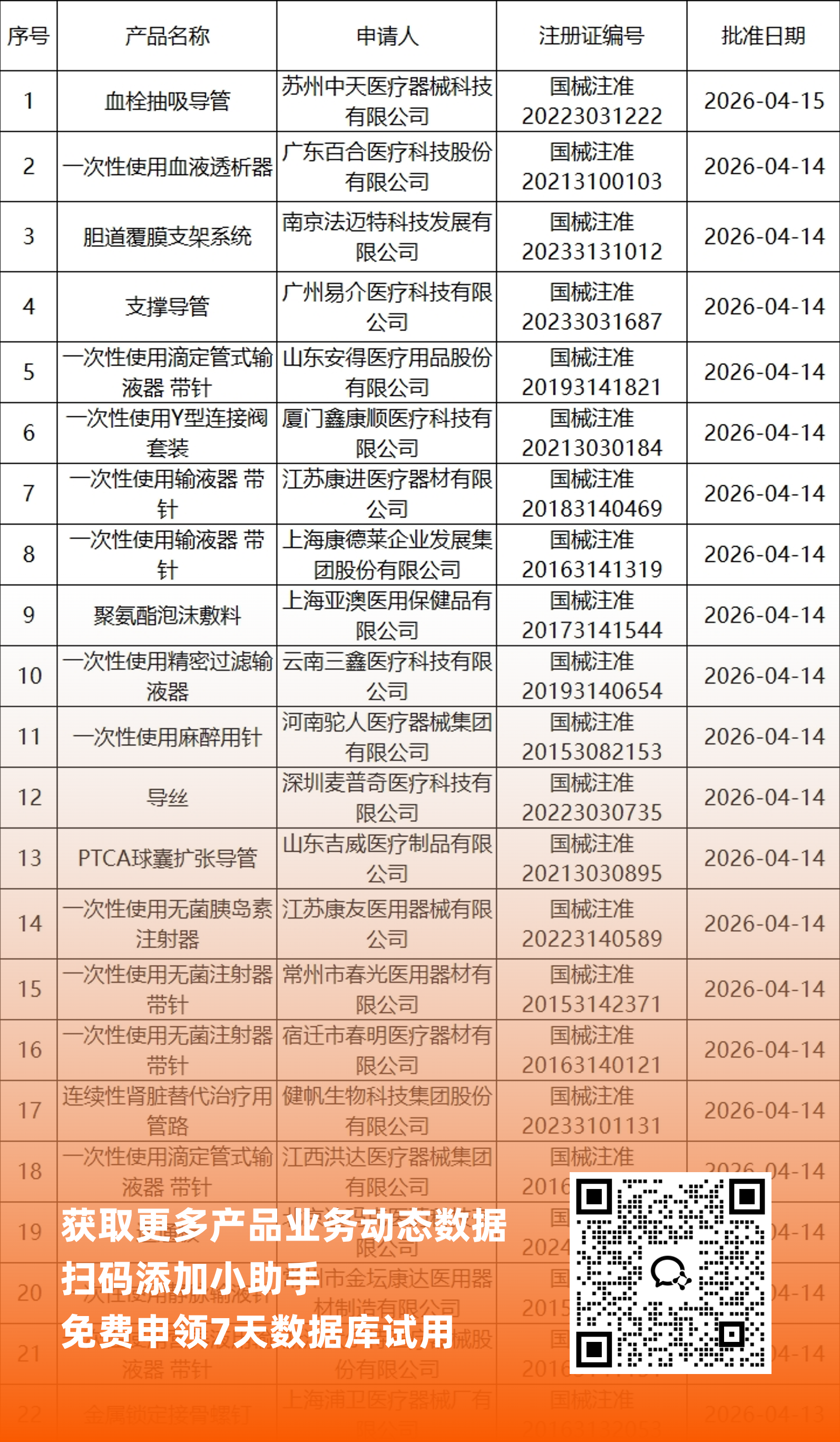
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。