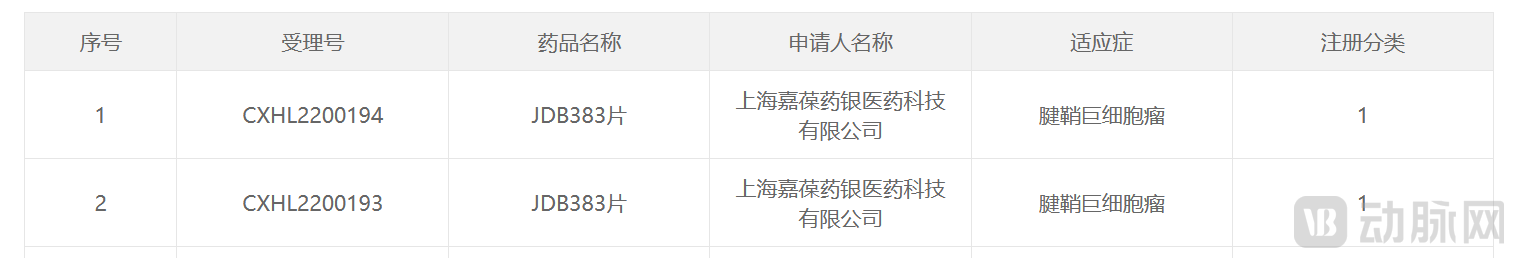
2022年6月2日,成都嘉葆药银的全资子公司上海嘉葆药银医药科技有限公司自主研发的口服、高选择性、1类靶向抗肿瘤小分子创新药JDB383片收到国家药品监督管理局核准签发的药物临床试验批准通知书,获批适应症为腱鞘巨细胞瘤。
JDB383是经首创人源化PDX模型验证的集落刺激因子(CSF1R)抑制剂,CSF1是一种由二硫键连接而成的二聚体糖蛋白,主要存在于骨髓腔内,负责巨噬细胞的生长、增殖和分化等细胞过程,CSF1R作为CSF1的细胞表面受体可有效调节巨噬细胞的存活、增殖和分化。JDB383经临床前人源化PDX模型验证药效显著,并呈剂量依赖性增长,临床前药代显示JDB383吸收较快,生物利用度较好。

嘉葆药银于2019年成立,致力于开发临床急需的国家Ⅰ类创新药物,目前主要的研发管线包括:全球临床安全性最高的耐药肺结核药物;全球首创的肿瘤免疫+抗肿瘤血管生成药物,可挽救PD-1失效患者;超高选择性、极佳透脑效果的BTK抑制剂;经过全球首创PDX模型验证的集落刺激因子抑制剂等。嘉葆了解患者真实需求,以临床为导向,解决临床实际问题,持续在诸多疾病治疗领域深耕。




























