2017年,复星凯特刚刚成立,希望能够从美国Kite公司引进CAR-T药物Yescarta®,并通过技术转移在中国进行本地化生产与销售。
孙敏敏作为复星凯特创始高管,凭借多年的研发项目管理和注册法规经验,成功推动了Yescarta®在中国的产业化申报,并参与了国内细胞治疗法规政策的制定以及指南的编写。
复星凯特的经历只是孙敏敏在细胞治疗行业发展立足的起点。据WHO统计,2020年全球新发癌症近1930万例,死亡近1000万例。孙敏敏看到了在实体肿瘤治疗领域,存在着巨大的未被满足的临床需求,在天时地利人和的环境下,于2020年9月与合伙人一起创立易慕峰,致力于开发能够攻克实体瘤的细胞治疗药品。

缘始于复星凯特,进发于易慕峰
在加入复星凯特前,孙敏敏曾在复宏汉霖参与推动中国首个生物类似药利妥昔单抗“汉利康®”的批准上市,并负责多个抗体药物的申报,积累了丰富的药品研发项目管理与药政法规注册管理经验。
这也让她获得了参与复星凯特创立的发展机会。然而2016年的魏则西事件引爆舆论,彼时的细胞治疗行业一片混乱,也没有一款真正的CAR-T药物在国内外上市,这让孙敏敏对CAR-T治疗的未来充满了犹豫。
不过,当看到Yescarta®出色的关键临床试验数据,而且Kite正准备向美国FDA申报BLA时,孙敏敏意识到了CAR-T治疗的未来——这一疗法的规范化发展,能够为肿瘤患者带来治愈性希望。
从2017年到2020年,孙敏敏亲历了Yescarta®的技术转移以及与国家药监局的密切沟通,参与了国内CAR-T细胞治疗相关指导原则的讨论和制定,并在2020年年初新冠疫情爆发期,主导了该产品在国内的NDA申报。
在复星凯特的三年时间,让孙敏敏对细胞治疗行业有了更全面的认知,熟悉了CAR-T治疗从研发到工艺开发,再到申报商业化的全流程。
这三年,也是国内细胞治疗蓬勃发展的三年。2017年,《细胞治疗产品研究与评价技术指导原则(试行)》发布,初步规范了细胞治疗产品的研究、开发与评价方法,对混乱的细胞治疗行业进行了全面整顿,推动了国内细胞治疗产业的发展和壮大。
根据Clinicaltrials.gov网站提供的数据,中国在2017年9月就成为注册CAR-T临床试验最多的国家。目前,中国注册CAR-T临床试验数量已超过600项。
身处国内细胞治疗发展黄金期的孙敏敏,不仅看到了这一领域的发展前景,也清楚认识到CAR-T治疗的局限性,“那时候我意识到,CAR-T治疗在血液瘤已经获得了突破,而实体瘤有着更大的未被满足的临床需求。”于是,易慕峰应运而生。
目前,易慕峰已经拥有一支将近50人的专业团队,形成了战略、研发、质量与生产、临床、申报等职能全面的组织架构,部门负责人的平均产业经验超过10年。其中,易慕峰的质量与生产负责人、联合创始人沈青山,更是和孙敏敏共同经历过复星凯特Yescarta®技术转移的核心成员。创始团队从早期研发到产业化的全流程覆盖,为易慕峰在免疫治疗领域的发展奠定了人才基础。
凝练降维打击策略,致力攻克实体瘤
目前,CAR-T治疗赛道竞争愈发激烈,除了一批企业扎堆血液瘤治疗以至于出现同质化竞争外,专注实体瘤治疗以及研发通用型CAR-T产品的企业也逐渐涌现。
但是,CAR-T治疗实体瘤有很多问题需要解决,诸如缺乏特异性靶点、肿瘤异质性、肿瘤微环境、肿瘤浸润差等问题,使得用于实体瘤治疗的CAR-T产品开发面临挑战。
面对激烈的行业竞争与CAR-T治疗实体瘤亟需解决的问题,易慕峰已经走出了差异化定位。
当很多企业尝试通过调控、改构、扩增等方式增强CAR-T产品的效应时,易慕峰首先看到的是潜在安全性风险对增强CAR-T产品功能的限制。目前用于CAR-T开发的实体瘤靶点大多为肿瘤相关抗原,其在正常组织也有一定水平的表达,CAR-T细胞在杀伤肿瘤的同时不可避免会对正常组织产生毒性,也就是“中靶脱瘤”效应。“CAR-T想要攻克实体瘤,首先要解决安全性问题,之后才能更好地解决有效性问题”,孙敏敏强调。
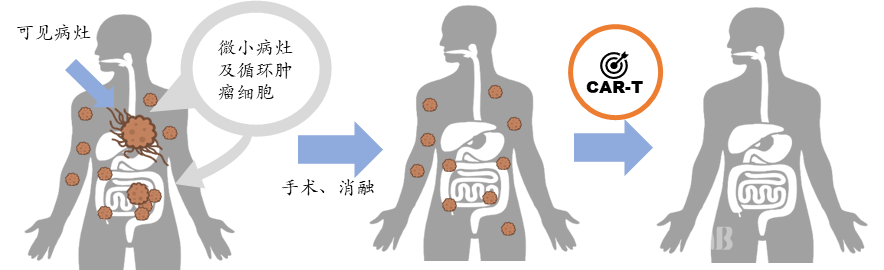
基于此,易慕峰创始团队创造性提出“化实体瘤为血液瘤”的降维打击策略,利用CAR-T药物清除较小或不可见的肿瘤组织以及循环肿瘤细胞,从而达到控制并清除转移灶、避免复发转移的目的。而较大的肿瘤组织,可以结合手术、消融等手段来治疗,部分由于发生转移而失去手术机会的患者也可以由此获得手术的机会。由于可以使用较低剂量针对较小的肿瘤组织和循环肿瘤细胞,可以保证产品的安全性。
易慕峰进一步开发了Peri Cruiser®专利技术。该技术可改变CAR-T细胞在体内的分布,即减少对正常组织的迁移,同时保持对肿瘤组织的浸润和杀伤能力,大幅提升CAR-T应用的安全剂量窗口。
在保证了CAR-T产品安全性的基础上,易慕峰还在发力研发更多的技术平台以增强CAR-T的功能,比如添加不同armor的四代CAR-T以克服肿瘤微环境、异质性和肿瘤组织浸润,以及T-Booster平台技术,通过表达CAR同源靶点至DC细胞,同时表达特定的信号分子,在体内进一步激活CAR-T细胞,大大提高CAR-T细胞的扩增、浸润、杀伤能力。
基于这些技术平台,从2020年9月启动运营至今,易慕峰在不到2年时间便建立超过10条产品管线,其中IMC001、IMC002已进入IIT研究阶段。
前不久,靶向EpCAM抗原的IMC001项目,在针对晚期胃癌和晚期消化道恶性肿瘤的两项IIT研究低剂量组试验中,呈现出良好的安全性和有效性。试验结果显示,6例受试者均通过28天安全性评价,未观察到剂量限制性毒性(DLT),其中5例呈现疾病稳定(SD)状态,疾病控制率(DCR)为83.3%。其中一例在观察到8个月时,肿瘤缩小已超过30%,腹水完全消退,达到了PR疗效,患者整体状态非常好,已恢复正常工作4月余。该项研究已受邀将在2022年9月举办的欧洲肿瘤医学学会会议(ESMO 2022)上做口头报告。
“这些数据印证了我们‘化实体瘤为血液瘤’治疗策略的可行性——不需要给患者非常高的药物剂量,就能带来既安全又有效的治疗效果”, 孙敏敏说。
IMC002是靶向CLDN18.2抗原的高特异性CAR-T产品。“我们在同步推进IIT试验和IND申报,已于7月18日获得美国FDA孤儿药资格认定,计划在今年年底完成中国与美国的IND申报,期望成为业内首批获得IND批件的CLDN18.2-CAR-T产品,我们的目标是做到Best-in-Class”,孙敏敏满怀信心地说。

孙敏敏提到,“我在复宏汉霖时,企业就提倡在速度与质量上做可负担的创新。”在这一企业文化的熏陶下,易慕峰非常注重产品的推进速度,以及创新与风险的平衡,每个项目在日程上都会进行紧凑的安排,也会做好可能风险发生后的Plan B。
提到易慕峰的未来,孙敏敏最希望看到的是公司产品在治疗实体瘤上取得突破,从而推动产品获批上市。但发展的脚步并不止于此,孙敏敏提到,解决实体瘤是公司发展的第一步,易慕峰希望能够将细胞治疗扩展到更多的疾病治疗领域,为更多的患者带来临床获益。





























