3月,位于美国马萨诸塞州的生物技术公司Flare Therapeutics(以下简称Flare)完成了由GordonMD Global Investments和辉瑞领投,共计1.23亿美元的B轮融资。资金将用于针对晚期尿路上皮癌的FX-909项目临床开发,推进一个新的转录因子靶点开发以及新一款候选药物。
3月30日,Flare宣布原首席运营官兼首席财务官Daphne Karydas晋升为总裁兼首席财务官,原生物学和转化科学高级副总裁Michaela Bowden晋升为首席开发官,并且任命医学博士Michael L. Meyers为首席医学官。
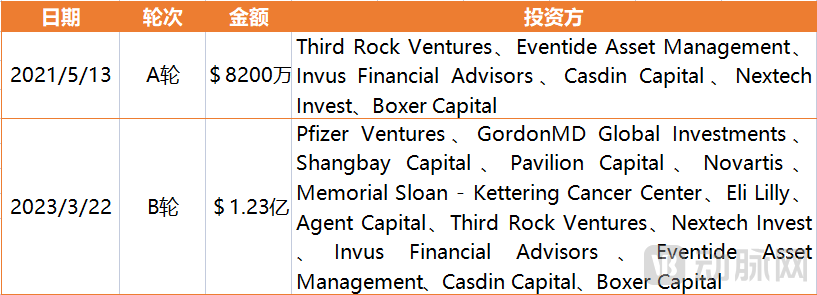
来源:公开信息整理
一系列融资和人事变动信息背后,展现着Flare的雄心壮志,那就是征服转录因子。
Flare成立于2021年,成立当年就完成了由Third Rock Ventures牵头的8200万美元的A轮融资,时任临时首席执行官的Abbie Celniker博士说:“我们创建Flare是为了完成征服转录因子的使命。”
转录因子(TF)是DNA结合蛋白,可以激活或抑制DNA转录,从而控制基因表达。转录因子通常在具有相互关联的生化活性的多蛋白复合物中发挥作用,通过读取基因组并在DNA特定区域整合辅助蛋白来协调其表达。
长期以来,转录因子一直都是药物开发人员的理想目标,因为转录因子突变可能是许多疾病的驱动因素。尽管转录因子有着如此“神威”,但是能成功用于治疗的转录因子不足1%,原因是以往药物设计的常规规则并不适用于它。
靶向小分子药物的研究需要蛋白质内的一部分可以与小分子结合并且干扰蛋白质的功能,而TF的结构和相互作用是高度无序乃至紊乱的,故靶向TF的主要挑战之一便是缺乏结构化的结合部分,即无法系统地将TF的生化功能与小分子药物发现的靶向位点联系起来。
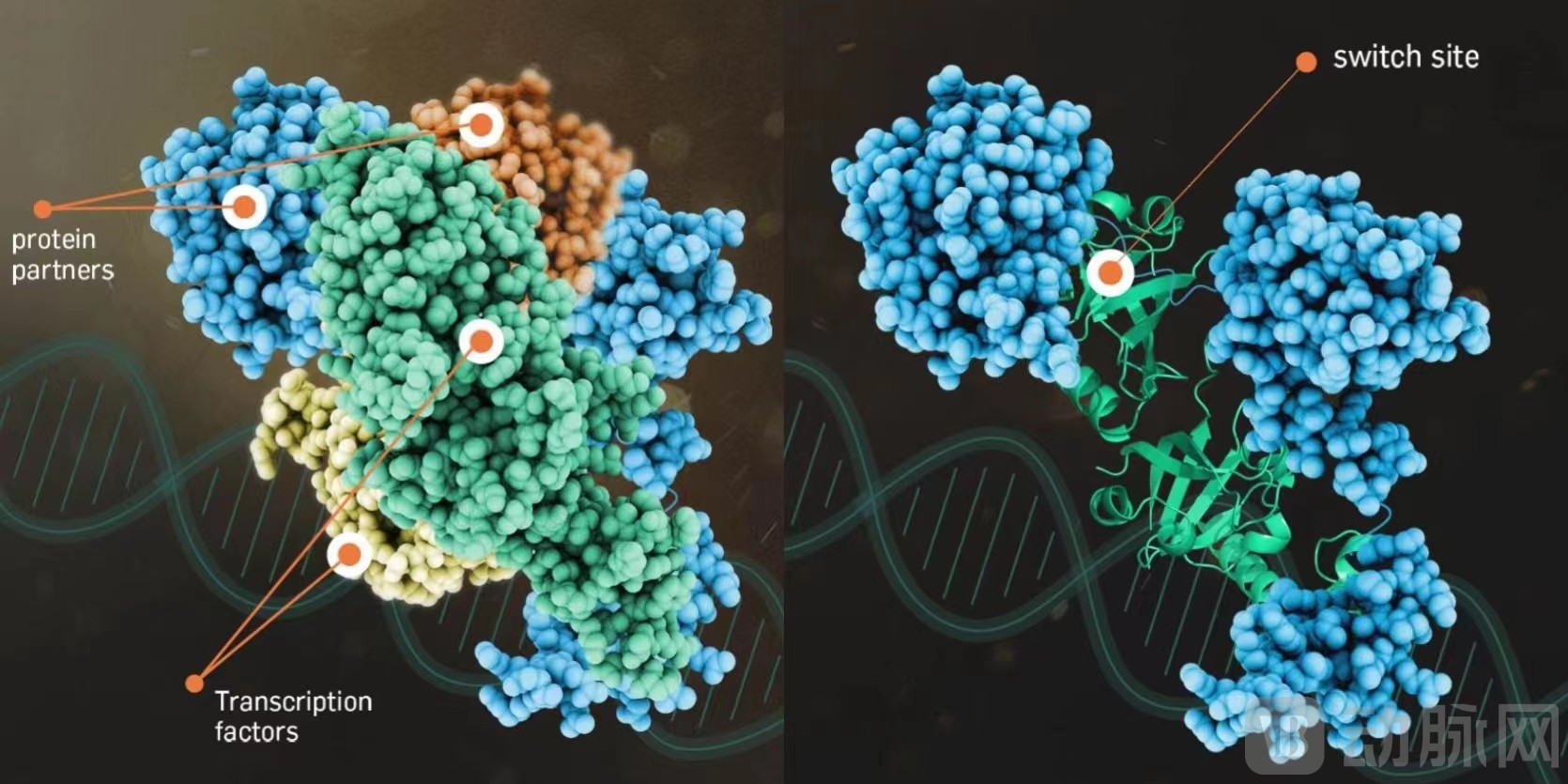
基因表达的主要调控因子及“转换位点”
来源:Flare官网
Flare团队受到了牛津大学Fraydoon Rastinejad博士小组在HIF-2转录因子方面工作的启发,尝试用新颖的方式去破译转录因子的生物学特性以开发小分子药物,从而点亮了一个新的治疗领域。
在科学顾问们的开创性工作基础之上,Flare团队发现了“转换位点”,即可药物化区域。这些区域是转录因子调控和解决引起疾病突变的关键靶点,可以控制DNA转录中可预测的变化,从而控制基因表达。
可以把“转换位点”理解为一个单一的、可定义的位置,它能够主导转录因子复合体中的协同相互作用,因此发挥控制基因表达的能力。基于此,Flare开发了新兴管线,将“转换位点”范式应用于神经学、免疫学、炎症和由转录失调驱动的罕见遗传疾病的早期发现项目当中。
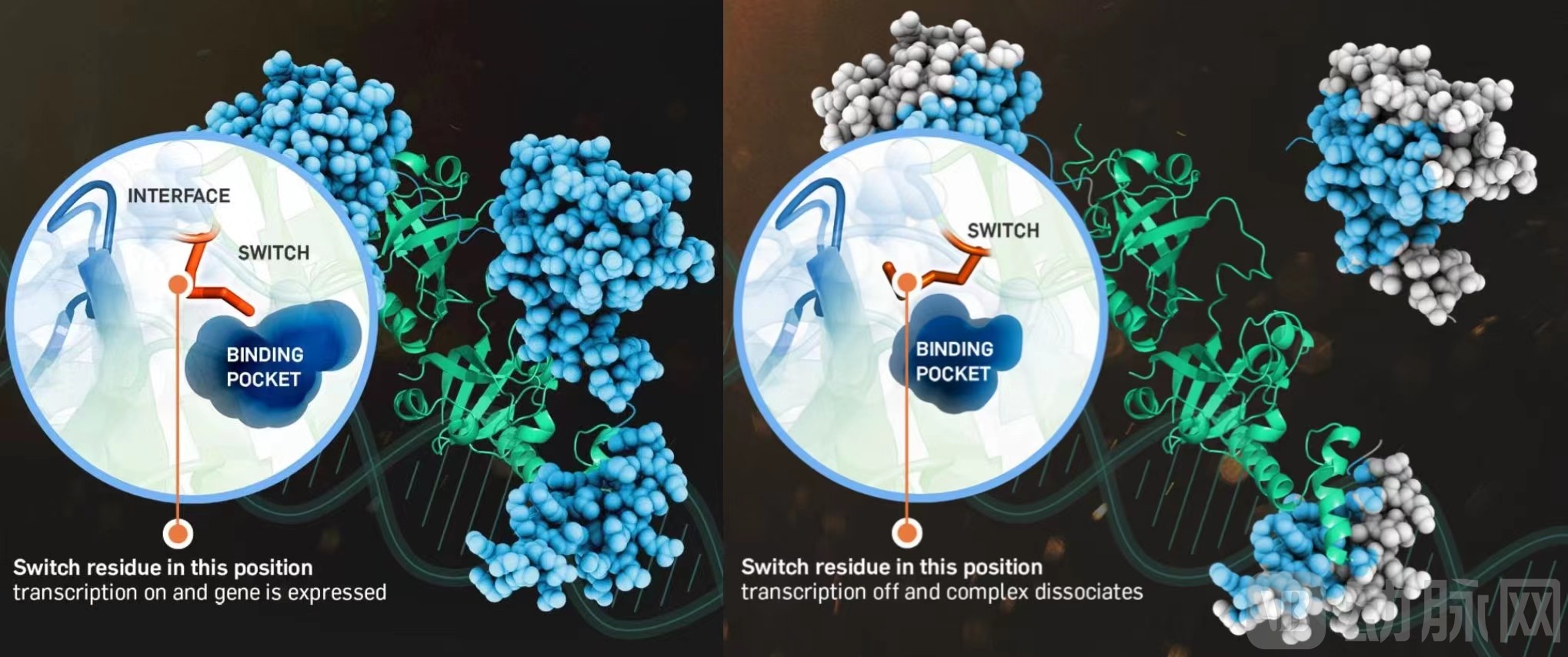
“转换位点”转换及复合物解离
来源:Flare官网
现在,团队针对“转换位点”的小分子药物发现取得了新进展,计划推动其精确肿瘤学项目FX-909于2023年进入临床试验。FX-909是一种针对PPARG的小分子抑制剂,用于治疗局部晚期或转移性尿路上皮癌(UC)。
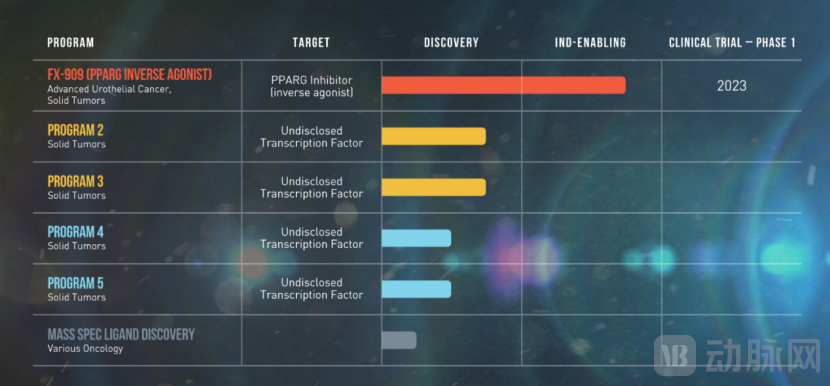
Flare的管线设置
来源:Flare官网
Robert Sims是Flare的联合创始人兼首席科学官,毕业于美国德克萨斯大学奥斯汀分校。在这所誉为“公立常春藤”之一的名校里,他获得了细胞和分子生物学博士学位和微生物学学士学位,还在《Science》《Nature》等顶刊上发表了30多篇论文。
在转录领域,Robert Sims拥有超过20年的经验,其中包括10年以上的基因控制药物发现经验。创办Flare之前,他曾在Constellation Pharmaceuticals担任研发高级副总裁,此外还是Third Rock Ventures的驻场企业家。

Flare联合创始人、首席科学官 Robert Sims
图源:Flare官网
2019年,牛津大学Fraydoon Rastinejad博士的小组发表了一项研究,确定了基因中一个敏感的“控制开关”,这个开关调节一种称为缺氧诱导因子-2(HIF-2)的转录因子,该因子在某些癌症中过度活跃,但在慢性肾病中不活跃。当时的Robert Sims对这项研究及其对转录因子用药的影响感到震惊且萌生了兴趣。

Flare联合创始人、牛津大学博士Fraydoon Rastinejad
图源:Flare官网
2020年,在新冠致使世界各地的研究实验室关闭之前,Robert Sims特意飞往牛津会见了Fraydoon Rastinejad,并与之讨论转录因子的相关实验,也正是这些实验构成了Flare创立的基础。
一开始Flare的公司规模很小,只有十几个人,许多实验依赖外包,但经过两年发展,现在公司团队人数近四十人,吸引资金总额达2.05亿美元。
对于转录因子的探究,Flare并非“第一个吃螃蟹的人”。
成立于2017年,总部位于英国剑桥的Azeria Therapeutics便是针对肿瘤开发FOXA1等转录因子抑制剂,其于2018年和2019年顺利完成了A轮和B轮融资,总额达3600万英镑。
融资完成后,Azeria Therapeutics团队在随后的临床前研究数据中,未达预期。最终,2020年公司决定停止运营,并将大量资金返还给投资者。
Azeria Therapeutics已迎来结局,但并不意味着这条赛道已经走不通了。
2022年10月,在第34届EORTC-NCI-AACR研讨会上,Flare发表了一篇题为“Peroxisome Proliferator-Activated Receptor Gamma (PPARG) status defines the luminal lineage in molecular profiles of advanced urothelial cancers (UC)”的报告。
在临床前实验中,Flare使用PPARG抑制剂FTX-6746在UC细胞系中进行了治疗测试,包括UMUC9(PPARG扩增)和HT1197(RXRA-S427F热点突变)。
数据显示,用药后第2天UMUC9异种移植肿瘤组织中的靶基因抑制高达80%,第21天肿瘤生长抑制超过100%;而HT1197异种移植肿瘤靶基因抑制在第2天超过了45%,第42天肿瘤生长抑制效果为85%到112%。停止治疗后也没有肿瘤再生长。
现有数据表明,FTX-6746可有效抑制PPARG靶基因,并在耐受性良好的剂量下实现了持久的肿瘤消退。这些数据也促成了其治疗局部晚期或转移性UC的FX-909管线于2023年进入临床试验。
在2023年4月14日至19日于佛罗里达州奥兰多举行的 AACR 年会上,Flare又以口头介绍和海报形式强调了其主要化合物 FX-909的首次临床前数据。口头报告显示,在 UC 的动物模型中给予 FX-909引起持久的肿瘤消退。预计50毫克/千克的人体起始剂量也具有药理活性。
Robert Sims博士说: “我们渴望继续推进 FX-909,这将在今年晚些时候开始的第一阶段试验中得到进一步评估。这对于 Flare 来说将是一个里程碑式的时刻,因为我们是第一家将要进入临床的公司。”





























