2023年4月20日,专注核药研发的加拿大初创公司Abdera Therapeutics宣布获得1.42亿美元的A轮和B轮融资。B 轮融资由 VenBio Partners领投,A 轮融资由Amplitude Venture Capital, Versant Ventures领投。Abdera Therapeutics本轮所获得资金将用于推进其基于抗体的新型核药研发。
Abdera Therapeutics成立于2021年。成立之际,这家公司便获得800万加元的种子轮融资。至今,Abdera共获得1.483亿美元的融资。
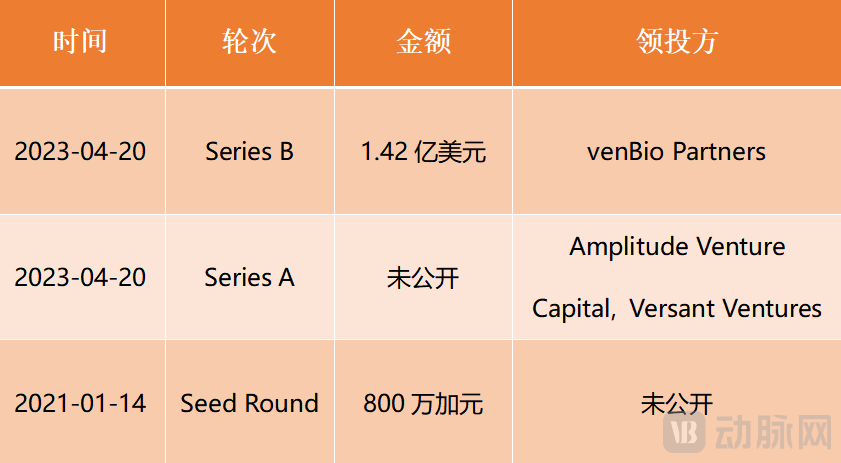
Abdera融资轮次 数据来源:Crunchbase
想要了解Abdera发展的始末缘由,首先得从它诞生的故事讲起。
2021年,加拿大风投公司adMare BioInnovations和关注抗体生物技术的上市公司 AbCelera于温哥华共同成立了Abdera Therapeutics,试图在放射性同位素疗法方面实现突破。
Abdera的创始团队由三名生物制药领域高管组成。联合创始人兼研究部高级副总裁Adam Judge博士在伯明翰大学医学院获得细胞免疫学博士学位,他深耕免疫学、RNA疗法等领域,开发了30多项相关专利。在Abdera之前,Adam Judge博士在Genevant Sciences、Tekmira Pharmaceuticals担任技术高管,任职期间他将肿瘤项目顺利推进到临床试验阶段。
Lana Janes博士拥有20余年的药物开发专业知识,也是Abdera的联合创始人之一。Janes博士在麦吉尔大学攻读了生物化学博士学位之后,在adMare BioInnovations等企业担任高管职务,负责多个领域的药物FDA获批工作。
另一位联合创始人Michael Abrams是麻省理工学院的化学博士,拥有超过 35 年的药物开发经验。在加入Abrams之前,他曾在多家企业担任高管职务。Abrams博士还是AnorMED的创始人兼CEO,该公司开发了 FDA 批准的干细胞动员药物Mozobil,被健赞(Genzyme)以超过 5 亿美元的价格收购。此外,Abrams博士在放射性药物显像剂Cardiolite的开发工作也获得美国核医学会颁发的核能先驱奖。

Abdera三位联合创始人,从左往右:Adam Judge、Lana Janes和Michael Abrams
图源 Abdera官网
三位创始人各擅其长,推动Abdera行稳致远。
针对一些已被临床验证的肿瘤靶点,他们利用AbCelera的抗体发现平台开发全新的放射性同位素偶联药物,希望为核药市场带来变革。
Abdera的核药设计都基于其平台——ROVEr平台,要详解它的价值,首先得聊聊放射性配体疗法。
近年来,放射性配体疗法成为肿瘤精准治疗领域的一个重要方向,与传统的肿瘤治疗方法相比,放射性配体疗法具有杀伤力强、精准靶向、损伤有限的优点。其所需的放射性同位素偶连药物(核药)常由四部分组成:配体、连接体、螯合剂以及放射性核素。配体可以是抗体或者肽类,它对不同器官或组织的亲和度不同,因此可以将放射性核素运送到靶点;螯合剂用于“困住”放射性核素;连接体用于连接配体及螯合物。
目前放射性配体疗法通常采用小分子配体或大蛋白,但无论选择哪种配体选择都有局限性。小分子配体(肽或小分子)虽然可做到肿瘤的快速吸收及排泄,但会伴随着低肿瘤蓄积,肾脏对放射性同位素的高摄取也会带来肾毒性。大蛋白可能会避免肾脏摄取,但其大体积和长半衰期可能限制肿瘤吸收,全身辐射暴露又会导致潜在的骨髓毒性。
因此,如何达到药物吸收和代谢的平衡一直是这种疗法的难题。
针对这个痛点,Abdera研发了ROVEr平台,该平台可定制设计具有可调药代动力学 (PK) 特性的药物,以增强肿瘤对药物的吸收和渗透,同时避免高肾脏摄取,减轻全身放射毒性。
ROVEr平台从配体入手,多方面突进。
高级抗体工程
ROVEr平台的细胞靶向载体是仅重联抗体,专为放射性同位素的递送所需的药理学和PK特性所设计。它由高亲和力的抗原结合域和人Hc片段融合而成,生成具有最佳大小和PK特性的抗体(VHH-Fc)。这种抗体可以避免肾脏的滤过,减少血液循环中的放射性物质,并增强肿瘤对药物的吸收和渗透。
值得一提的是,ROVEr平台的模块化抗体形式支持将不同的抗原结合域切换到平台中,以创建具有可预测PK和药理学的新型抗体。
螯合剂库
ROVEr平台的螯合剂与一系列治疗性放射性同位素兼容,包括锕-225、镥-177以及成像同位素(比如铟-111),确保放射性同位素与抗体结合稳定。
强放射性同位素
放射性同位素的选择取决于所需的癌症靶点和适应症。ROVEr平台设计的药物包括发射α或β粒子的放射性同位素,比如锕-225和镥-177,它们都有较强的肿瘤杀伤能力。
图像和治疗
ROVEr平台支持与相应的成像同位素配对、评估健康组织暴露(剂量测定)、选择合适的患者并指导临床开发。显像剂利用相同的抗体-螯合剂偶联物作为治疗方案,支持直接数据比较并简化开发。
通过这个平台,核药能选择性地破坏肿瘤细胞,健康细胞能被最大程度保留。强效放射性同位素的递送和治疗指数因此被优化。
Abdera研发的精准靶向药物都是基于ROVEr平台所设计的,走在最前面的要数针对小细胞肺癌的药物ABD-147。
据WTO统计,肺癌是全球发病率第二高的恶性肿瘤。虽然在肺癌中,小细胞肺癌仅占15-20%,但其手术效果差,化疗复发率高,治疗方式选择有限。近年来,靶向治疗和免疫治疗成为小细胞肺癌备受瞩目的治疗手段。
Delta样配体3(DDL3)是Notch通路中的一种蛋白质。包括小细胞肺癌(SCLC)在内,一些高级别神经内分泌癌中DLL3上调并在细胞表面呈低水平特异性表达。相反,DLL3在非恶性细胞中不存在或很少表达。ABD-147就是瞄准了这个靶点,精准打击肿瘤。
其实早在2016年,艾伯维(AbbVie)在收购Stemcentrx时就获得了DDL3这一靶点,但相关临床试验以失败告终。Abdera称他们是由于药物的细胞毒性问题而失利。
目前,Abdera的正在推进ABD-147的临床前研究,他们预计在2024年向美国FDA提交IND申请。
另外,Abdera还有4条基于ROVEr平台的管线。有2条在先导物优化中,2条在药物发现阶段。
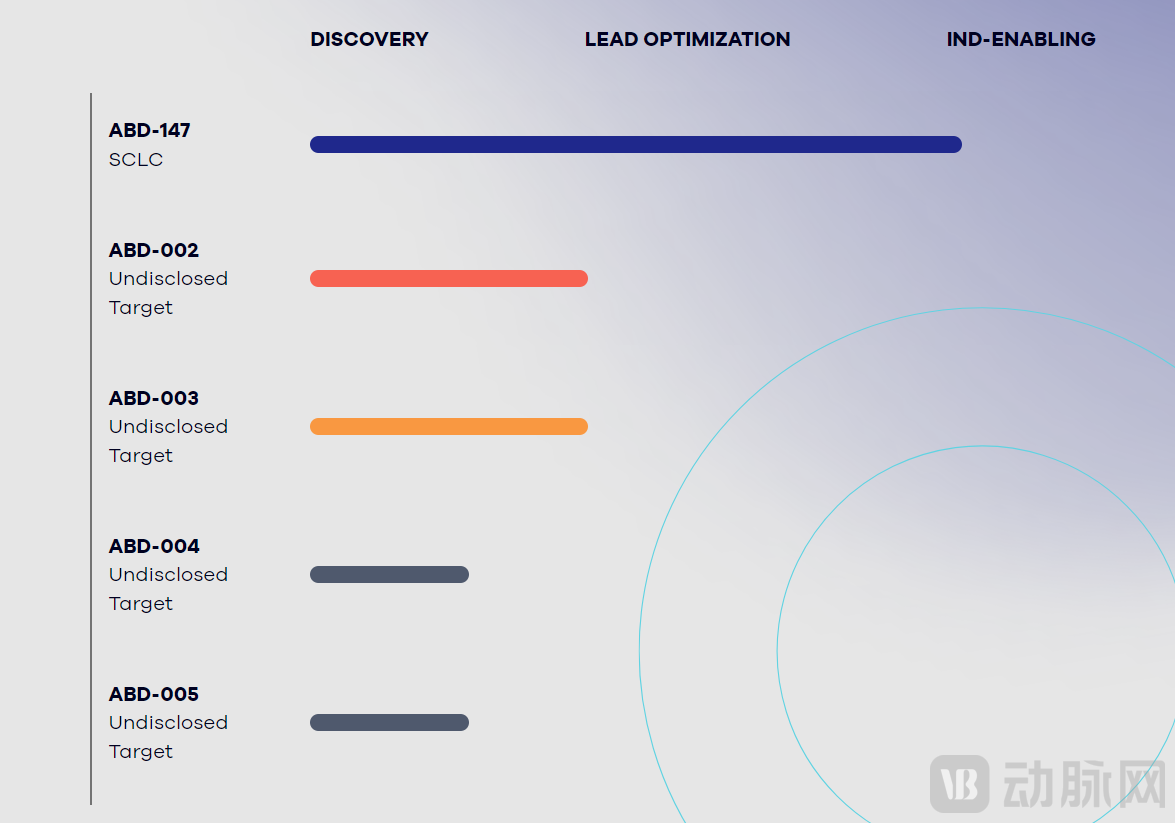
Abdera在研管线进展 图源:Abdera官网





























