提到上世纪最让人印象深刻的biotech企业,我们难免会想起曾经制药行业横空出世的“黑马”——福泰制药(Vertex Pharmaceuticals)。这家公司在创始人Joshua Boger的带领下,仅仅用了三年时间就完成了从诞生到上市的过程,创造出了大获成功的商业传奇。
这位履历丰富的创始人自哈佛大学化学系博士毕业后即任职于药企巨头默沙东,之后放弃默沙东基础化学部门高级主管的职位到一手创立福泰,从1000万美元的起步资金到打造出三款年销售额超过10亿美元的药物,Boger本人也是制药企业发展历史上耀眼的启明星。
令人感到惋惜的是,自2017年Boger从福泰卸任之后,其本人就再未在其他biotech任职过。然而,6月,美国一家处于临床阶段的眼科初创公司Alkeus却宣布Boger将出任执行主席,这家公司究竟有什么独到之处,能吸引Boger再度出山?
Alkeus由Leonide Saad博士和Ilyas Washington博士于2010年共同创立。公司创立的目标是以一种全新的方式治疗退化性眼疾,减少维生素A在眼睛中二聚化时产生毒性的可能性。
对于此次任职,外界在惊讶的同时也不免有质疑的声音,以Boger的资历出任这样一家初创公司,真的不是空有虚职吗?对此,Boger表示:“我到Alkeus非常认真,我想如果我不做这份工作,那就相当于我是在浪费我过去经历中获得的一切知识。”
与任职消息同时发布的还有Alkeus成功完成1.5亿美元B轮融资,本轮融资由Bain Capital Life Sciences领投,TCGX、Wellington Management和 Sofinnova Investments跟投。
Alkeus CEO、总裁兼联合创始人Leonide Saad博士说: “本轮融资所筹资金将用于支持治疗遗传性眼病 Stargardt 在研管线 gildeuretinol(ALK-001)尽快提交 NDA 申请并获得 FDA 的批准,以及团队规模的扩张。”
他还强调,Joshua在领导药物的开发和商业化方面有着非常丰富的经验,这对 Alkeus 未来有组织的发展,对gildeuretinol的成功上市具有巨大的价值。

▲ Joshua Boger博士(图源Alkeus)
目前国内外常见的眼科疾病市场主要集中在老年性黄斑变性(AMD)、糖尿病视网膜病变(DR)、干眼症(DE)、青光眼四大领域。过去十余年,不少专业人士在临床前和临床层面上都做了大量眼科治疗的开发工作。除了FDA批准的药物治疗(基因治疗、FDC、小分子药物等)外,现代眼球给药(ODD)系统也在着力发展眼内植入物、穿刺塞、水凝胶、脂质体、纳米颗粒等技术。
然而由于某些眼病引起的眼睛结构的病变具有不可逆性,且病理机制尚未明确,目前药物治疗的整体痛点在于无法根治眼部疾病,而长期使用药物仅能起到延缓疾病进程、控制病情恶化和降低严重并发症发生的作用。因此手术治疗仍是某些眼病治疗的一线方案。
在已开发的适应症有限,成药技术壁垒高的种种困难下,Alkeus仍旧做出了获得FDA 突破性疗法认定和孤儿药认定的gildeuretinol(ALK-001)。这也是临床开发中第一个也是唯一一个通过减少眼睛中维生素 A 二聚化且不会对正常视力产生任何影响的 Stargardt 病治疗药物,这也使得gildeuretinol同时具备了成为first-in-class和best-in-class药物的潜质,Alkeus计划在2024年提交 NDA 批件。
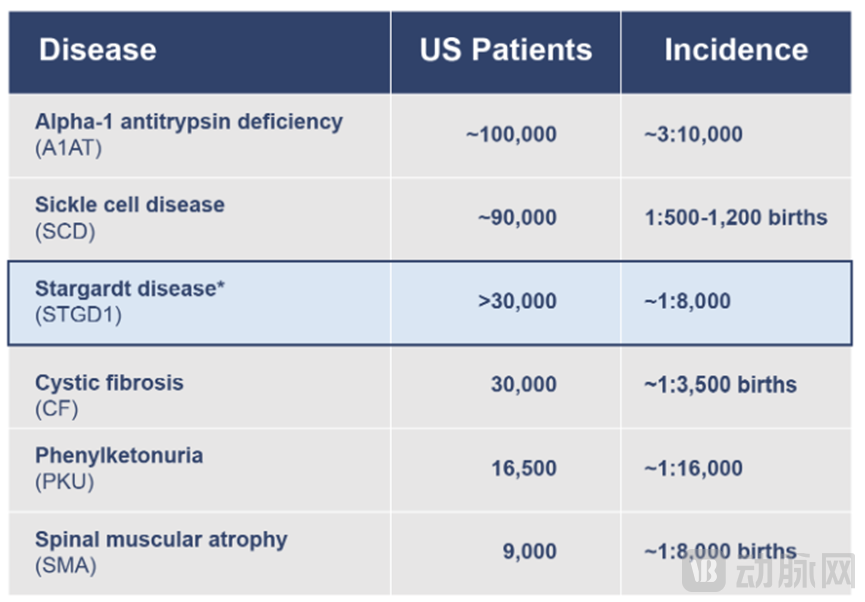
▲ 美国不同眼部疾病人数表(图源Alkeus)
Stargardt病是一种常染色体隐性遗传的黄斑萎缩型变性类疾病,临床特征表现为视网膜细胞(视杆细胞和视锥细胞)退化。这种疾病是导致儿童和年轻人失明的主要原因,在美国已经影响超过3万人,全球已经影响了超 15 万人。患者出生时通常视力正常,但ABCA4基因突变会导致眼睛中维生素A加速二聚化或结块,从而导致视网膜受损和后续的进行性视力丧失。
针对包括Stargartd病在内的单基因视网膜疾病的基因疗法正在开发中,但标准的AAV2载体装载能力有限,无法承载ABCA4这类较大的基因,因此也有团队在尝试双AAV策略和慢病毒进行治疗。所以虽然病理的遗传原因已经明确,但是目前为止针对Stargardt病还没有有效的治疗方法。现阶段,眼科医生依旧只能鼓励患者在明亮的光线下戴墨镜和帽子,以减少脂褐质的积累。
“Stargardt是一种进行性的疾病,这种疾病不可避免地会导致毁灭性的视力丧失,令人失去生活能力。” Boger博士说。
Alkeus研发的gildeuretinol被设计成一种新型的氘化形式维生素 A,其中三个氢原子被氘原子取代。这种修饰可以明显降低维生素A二聚化速率,有望在不扰乱视觉周期的情况下减缓或阻止 Stargardt 病患者视力丧失的过程。目前已经完成临床II期试验。
自2017年FDA批准了第一个氚化药物氘代丁苯那嗪以来, 氘在药物中的应用就呈爆炸式增长。氘化药不仅仅可以改善药物的药代动力学性质,而且有可能改善代谢介导的毒性,解决口服利用度低的问题。诸如辉瑞、诺华、默克、阿斯利康、罗氏等制药界巨头也开始应用氘代技术来研发新药。
目前研发重点已转向将氘代技术应用于新型药物,FDA于2022年批准了开创性的新型氘化药物德卡伐替尼。其他的应用包括已获批用于治疗不能手术切除或转移性肝癌和晚期肾癌的多纳非尼和用于COVID-19 的 VV116,前者是通过索拉非尼的吡啶环次级酰胺上引入了三个氘原子获得的,后者GS-441524的软点被氘化获得的。
在临床前体外试验中,gildeuretinol能将维生素A的二聚化速率减慢4-5倍。在体内试验中,gildeuretinol使维生素A二聚化降低了80%以上,并在该疾病的遗传动物模型中预防了失明。
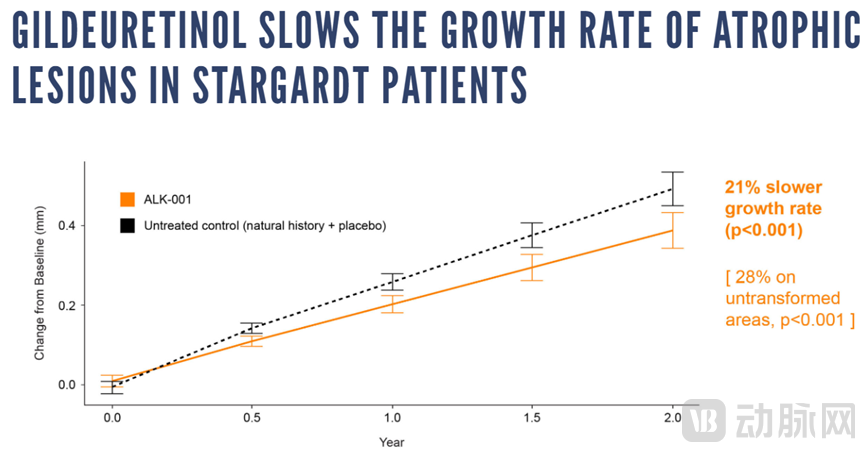
▲ gildeuretinol临床II期安慰剂对照试验(图源Alkeus)
Alkeus还完成了为期2年、双盲、安慰剂对照的“TEASE-1”(ALK-001二期临床试验代号)研究,试验中共有50名Stargardt晚期疾病患者参与随机分配ALK-001(30名)及安慰剂(20名)。这些患者被安排接受每日1粒的gildeuretinol药片治疗,持续24个月,在进行一年后,随机选择安慰剂组中的10名患者切换至治疗组。该研究的主要疗效终点是定义明确的萎缩性病变的生长速率。
试验结果显示,治疗组患者的生长速度比安慰剂组患者慢21% (P < 0.001),这是基于通过眼底自发荧光(FAF)测量到的萎缩性病变的生长速度。这相当于两组患者每年平均生长面积估计相差0.35 mm2。
而且,重要的是,gildeuretinol在安全性上与天然维生素A相当,且治疗过程中没有观察到黑暗适应延迟、夜盲症或视力的显著变化。这比采取对视觉循环进行干预的方案要更好。在患早期Stargardt病的儿童和年轻成人中,gildeuretinol表现出能够阻止疾病的进程,防止进一步的视网膜损伤和视力丧失。
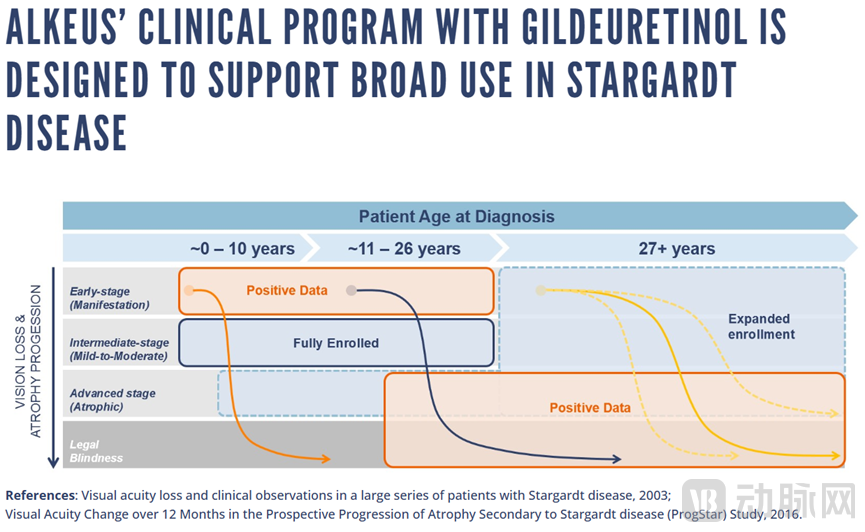
▲ 四项gildeuretinol在Stargardt病中的临床试验正在进行或已完成,前两个数据读数显示出积极的临床治疗数据(图源Alkeus)
此外,gildeuretinol的其他临床试验也正在进行中,包括在Stargardt病中期患者中开展的一项完全纳入、随机、安慰剂对照临床试验(n = 80),这项研究预计将在2025年获得管线数据。
另一项关于gildeuretinol治疗干性年龄相关性黄斑变性(AMD)继发地图样萎缩(GA)患者的3期研究(n=200)已经完成全部受试者入组,但这项测试需要更多的时间,预计将于2023年晚些时候得出结果。
面对这样一个基数庞大但尚未出现有效疗法的市场,通过gildeuretinol的临床试验结果似乎就能预测出它疗效的卓越性,即便未来出现可操作的基因治疗,昂贵的治疗成本也会让它的推广受限。Boger显然看出了gildeuretinol商业化的潜力,一旦申请NDA审批通过,Alkeus或许会拿下Stargardt市场的龙头位置。
“我其实不是一个创业者,”Boger说,但是他对于Alkeus的未来他充满信心:“我可以看到患者未来治疗的清晰路径,而在数据的佐证下这条路径变得更加清晰。我们现在已经做好准备,使gildeuretinol这种变革性的药物,未来能让治愈所有的 Stargardt患者成为现实。”
值得注意的是,和大多数生物科技初创公司声势浩大的明星创始人团队不同, Alkeus在其成立之后的大部分时间里一直由Saad一个人经营,这位前风险投资家和咨询顾问在2010年为前哥伦比亚大学教授Ilyas Washington发明的一种药物颁发了许可证,之后他们便围绕该药物一起成立了Alkeus。

▲ Alkeus创始人Leonide Saad博士和Ilyas Washington博士(图源Alkeus)
一款成功的药物开发注定充满艰辛,尤其是在没有前人经验参考的情况下。想要做出first -in-class药物,就要面对新的适应症,新的临床试验需求,这个过程意味着“基本上不间断的工作,没有假期,没有个人生活和连续几年没有收入,”Saad说,“我不会再有精力经历一遍这样的过程了。”
随着临床试验顺利进行,公司迫切需要扩张自己的员工数量。Saad表示公司规模很快就会扩大到5名员工,而一旦gildeuretinol申请NDA成功,可能会扩大到50人甚至更多。





























