2023年07月12日,国家药监局药品审评中心(CDE)官网显示,沙砾生物科技有限公司(以下简称沙砾生物)自主研发的GT201注射液(受理号:CXSL2300290)正式获得国家药品监督管理局(NMPA)的临床试验默示许可。
 GT201是国内首款进入注册临床试验的基因编辑型TIL药物
GT201是国内首款进入注册临床试验的基因编辑型TIL药物
GT201为沙砾生物自主研发的表达膜结合细胞因子的下一代基因编辑型TIL(肿瘤浸润淋巴细胞)产品。沙砾研发团队在临床前研究中对比和选择了最优化的结构设计,并为工程化TIL疗法量身定做了逆转录病毒系统StaViral®,可实现在多批次、不同瘤种来源的TIL细胞稳定表达目标基因。
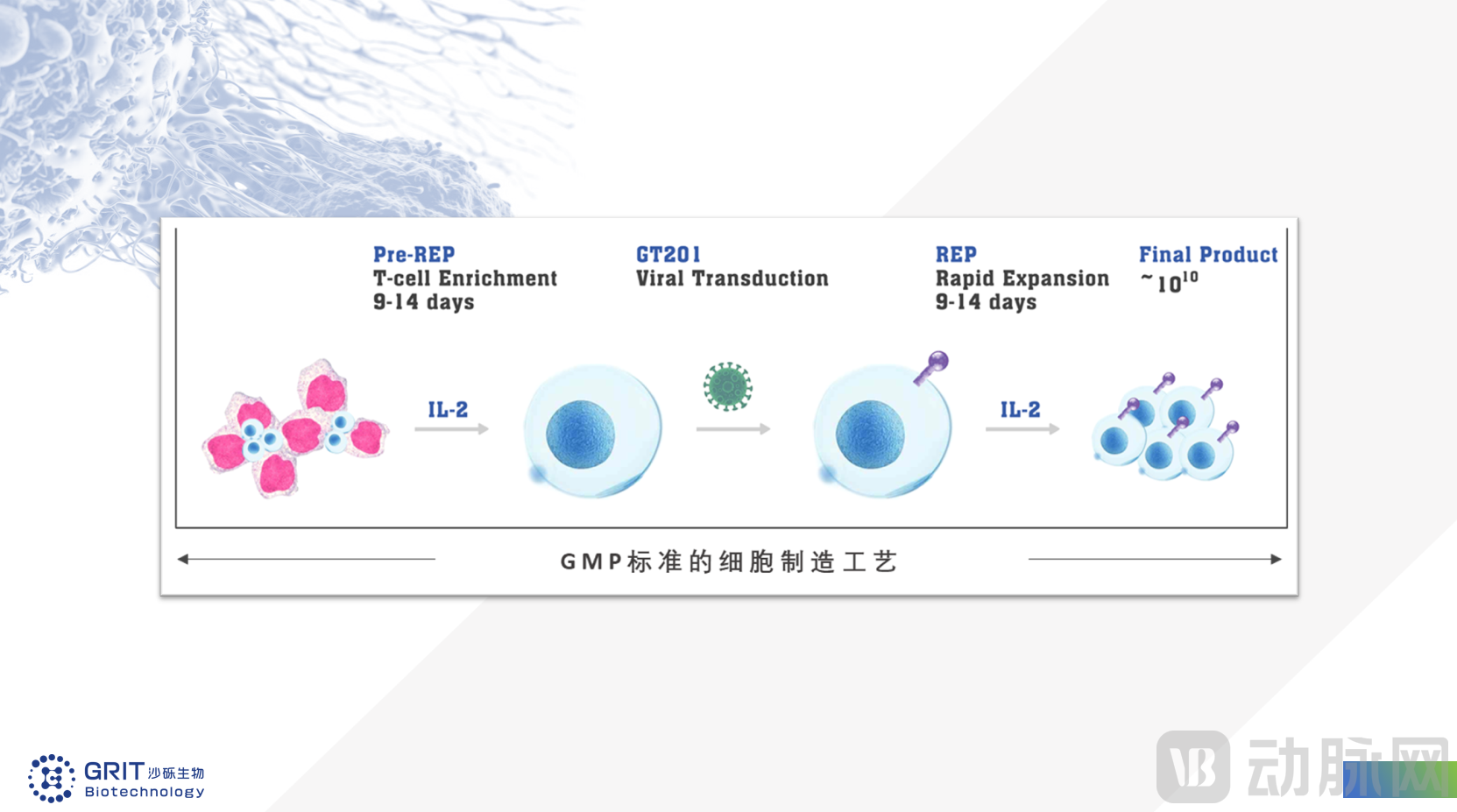 GT201是基于自研病毒编辑平台StaViral®的下一代TIL管线
GT201是基于自研病毒编辑平台StaViral®的下一代TIL管线
GT201在体内外均表现出较传统TIL更强的增殖能力、肿瘤杀伤、细胞因子释放和更好的存续性,并可以降低对于IL-2的依赖性,潜在降低临床应用中IL-2的使用剂量,从而克服传统TIL药物所面临的挑战。在研究者发起的临床试验(IIT)中,GT201药物在治疗多名晚期实体瘤患者的过程中表现出了良好的安全性,并展示出稳定地扩增和初步临床疗效。
沙砾生物即将正式启动GT201的一期临床试验,届时将面向社会招募实体瘤患者。

沙砾生物成立于2019年,是一家致力于肿瘤浸润淋巴细胞的研发及临床应用的综合型细胞治疗公司。沙砾生物已完成多轮股权融资,得到了国内外多家知名创投基金的支持。
沙砾生物自主研发的GT101注射液是国内首个获批注册临床的肿瘤浸润淋巴细胞药物。公司的核心研发平台包括StemTexp®干性TIL扩增技术平台、StaViral®病毒稳转株工艺、ImmuT Finder®免疫调节靶点发现平台、KOReTIL®高效基因敲除系统,并依托平台开发了一系列下一代基因编辑型TIL药物。沙砾生物拥有国际领先的技术储备和产业资源,旨在打造开创性的实体瘤细胞药物,为广大肿瘤病患带来新的希望。




























