2024年8月28日获悉,专攻创新药配方和递送技术的生物技术公司Lindy Biosciences宣布与诺华子公司诺华制药公司(Novartis AG)达成多目标独家全球许可协议和战略合作。此次合作的重点是利用Lindy Biosciences的专有技术,将诺华产品组合中的部分创新药物转变为更为便捷的自行皮下注射药物。据悉,通过提供高浓度的生物制剂,Lindy Biosciences自有的技术平台显著增加了单次皮下注射的最大剂量,有望降低医疗成本,同时提高患者的舒适度、便利性和治疗依从性。
根据协议,Lindy Biosciences将获得2000万美元的预付款,并有资格获得高达9.34亿美元的里程碑付款和分级版税,累计金额接近10亿美元。
目前,临床环境中超过一半的抗体治疗剂都是通过静脉注射给药的,这主要是因为治疗所需的剂量通常较高,无法配制成适合皮下注射的体积。而Lindy Biosciences专有的平台技术有望改变这一模式,让患者能够在家中通过预填充注射器或自动注射器自行给药。
杜克大学科研成果转化项目,直击单抗给药痛点
据Lindy Biosciences官网信息,公司成立于2016年,总部位于美国北卡罗来纳州莫里斯维尔,由北卡罗来纳生物技术中心提供贷款启动资金(20万美元的小型企业研究贷款),并根据杜克大学的一项专利技术孵化成立。起初,公司在创新实验室Southeast TechInventures 进行核心技术平台的进一步开发,并获得了美国国家科学基金会和美国国立卫生研究院超过 80万美元的小企业创新研究(SBIR)资助。
当前,Lindy Biosciences已完成160万美元的A轮融资,融资由Alumshares和BlueTree Allied Angels领投,IAG Capital Partners、Next Act Fund参投。
Lindy Biosciences的创始人兼首席执行官Deborah Bitterfield博士拥有杜克大学材料学博士学位,并有超过10年的制药/生物技术行业从业经验,业务涉及生物治疗和医疗设备等广泛的战略和运营领域。值得一提的是,在2017年创立Lindy Biosciences之前,Bitterfield加入了Southeast TechInventures,与高校科研人员合作,进一步开发有应用前景的生物技术。随后,她顺理成章地在杜克大学发起项目,并通过成立新兴公司Lindy Biosciences将科研成果转化落地。
Lindy Biosciences的成长过程恰好见证了全球生物基治疗应用的显著增长和内部技术转型趋势,制药公司和制造商的药物开发和制造流程正在发生重大变化。但这些生物制剂面临的主要挑战是难以保持保质期或储存稳定性。
根据Lindy Biosciences研发团队在Journal of Pharmaceutical Sciences(药学杂志)发表的论文,尽管生物制药行业普遍使用冻干和喷雾干燥技术,但生产固态生物制剂仍然是一项艰巨的任务,其中的挑战包括蛋白质稳定性(温度应力)、高资本成本、颗粒设计/可控性、缩短加工时间和制造难度因素(可扩展性、产量提高、无菌操作等)。因此,研发团队必须不断努力改进现有方法并探索新型脱水/粉末成型技术。
而Lindy Biosciences的自研平台Microglassification™正是一种脱水技术平台,它使用溶剂萃取在环境温度下快速脱水蛋白质制剂,消除了生物制剂在传统冻干和喷雾干燥过程中遇到的温度应力(又称热应力),可温和地从蛋白质或其他生物制剂溶液中除去水分,形成固体、球形、无定形的微珠。在这种干燥状态下,生物制剂足够稳定,可以长期储存、运输或加入药物输送配方中。
此外,与冻干等保存方法不同,Microglassification™对加工条件没有要求,几乎能普遍适用各种场景。与此同时,又与沉淀过程或结晶不同,在Microglassification™脱水过程中,蛋白制剂的颗粒大小、脱水速率和密度不会受到分子溶解度的显著影响。Lindy Biosciences的研发团队还比较了通过冻干处理的单克隆抗体制剂与使用Microglassification™处理的相同制剂的分子稳定性。两种粉末均在40°C下放置3个月,在25°C下放置6个月。两种脱水方法均表现出相似的化学稳定性,包括单体百分比、电荷变体和抗原结合。这些结果表明 Microglassification™可用于生产稳定的固态单克隆抗体制剂。
当前,Microglassification™已经能确保高浓度生物制剂的生产。以单抗为例,将抗体溶解在足够小的体积中以进行皮下注射会导致溶液太过粘稠而无法通过针头注射,或者太不稳定而无法维持合理的保质期。而Microglassification™平台通过结合固体mAb的稳定性和可注射悬浮液的有益特性,可以大大改善生物治疗药物的给药。
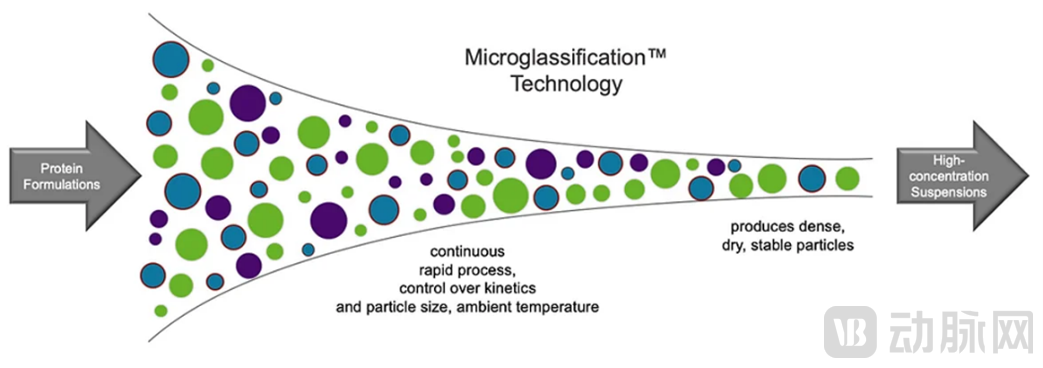
Microglassification™技术平台原理示意,图片源自Lindy Biosciences官网
如此一来,更为便捷且普适的皮下注射规模化地替代静脉注射成为可能。Lindy Biosciences希望通过公司的核心技术平台,使大量抗体疗法能够在家中通过自行注射的方式完成,而不是在急症护理环境中使用缓慢的静脉(IV)输液。这样做将降低给药成本,提高患者的舒适度和依从性,并使新的高剂量分子能够进入市场。
给药途径改良加入竞争,诺华自行注射药物成新增长点
目前,单克隆抗体已成为最重要的治疗性蛋白之一,并被用于治疗多种疾病,如肿瘤、炎症和自身免疫性疾病等。然而,新的药物靶点的识别是抗体开发所面临的巨大难题。并且单抗药物也有影响其临床使用的局限性。其中,最突出的挑战是单抗在制造、运输和储存过程中的短药代动力学特性和稳定性问题,可能导致聚集和蛋白质变性。然而,蛋白制剂、尤其长效蛋白质制剂的开发必须保持蛋白质的稳定性,并能够长时间地提供足够大的剂量。因此,探索多种策略来改进抗体的配方和剂型、以提高疗效,并增加单抗临床应用范围,成为创新药研发中的又一趋势。
截至目前,全球累计约200种抗体疗法被至少一个国家的药品监管机构批准,其中大多数采用静脉注射的方式给药,有部分通过腹腔给药(如:卡妥索单抗注射液)、肌内给药(如:帕利珠单抗注射液)或是玻璃体给药(雷珠单抗注射液)。值得注意的是,近几年在越来越多的药物中,皮下注射被证实是安全有效的给药方式。
从患者用药便利的角度来看,皮下注射节省了患者接受治疗的输液时间,具有相对较低的医疗成本。不仅如此,皮下给药还能够促进患者居家用药,缓解医疗体系压力及患者负担。
从制剂的微创新角度来看,皮下注射也是药企专利布局的重要一环。
在诺华营收占比最高(达到42.71%)的肿瘤治疗领域,单抗皮下给药制剂研发已成为热门趋势,并有望推动居家治疗的开展。已有研究表明阿替利珠单抗皮下给药剂型居家治疗极具潜力,特别是在远离医院的偏远地区。这一预期有望主导未来抗肿瘤药物的研发趋势。
在自免领域,诺华的司库奇尤单抗与礼来的依奇珠单抗占据了主要地位。特别是司库奇尤单抗自上市以来,就成为诺华创新药重点销售产品之一。这款IL-17A单抗最初的剂型就是皮下注射剂,并借此一路过关斩将,顺利获FDA批准治疗多种疾病,一度制霸自免市场。
与此同时,诺华也推出了一些可自行注射的药物,其围绕司库奇尤单抗布局的其中一款产品是一款名为Sensoready的自动注射笔,患者经过适当培训后即可自行注射。此外,诺华公司快速增长的多发性硬化症药物Kesimpta(奥法妥木单抗)也采用了同样的设备技术,其上市初期的宣传亮点便在于:长效和在家注射。而无论司库奇尤单抗还是奥法妥木单抗,于2024年第二季度的销量都超过预期,并间接导致诺华上调了全年盈利预期,奥法妥木单抗的年销售额有望达到40 亿美元。
在改良给药途径成为重要创新方式之一的当下,制剂开发是药物产品开发的一个组成部分,无论药物物质形式是什么,它必须与最终容器和药物输送方法密切配合,以增强活性成分和结构材料之间的相容性。考虑到诺华现有产品梯队清晰,且重磅品种未来可期,持续专注四大领域的创新药研发并强化给药技术无疑与其战略细则吻合。




























