3月初,一笔大额融资轰动了整个医疗器械行业。经导管二尖瓣置换(TMVR)领域的创新企业——美国4C Medical完成总额1.75亿美元的D轮融资,波士顿科学和HHF赋远投资作为唯二的新投资人联合投资,现有股东亦持续加码,是器械领域罕见的超大额融资事件。
自成立以来,4C Medical便因其在TMVR领域的大胆创新而颇受关注,但也受到诸多质疑。此次波科的注资,无疑是对4C Medical原创创新的坚定看好。
4C Medical所深耕的TMVR赛道,堪称全球医疗器械的一大“修罗场”,临床需求巨大、痛点明确,但壁垒高筑、难度之高使不少械企望而却步。即使雅培、美敦力、爱德华等巨头加码,数十家企业前赴后继,目前也尚无一款产品获批FDA。在此情况下,4C Medical却开辟出了一条没有跟随者的差异化创新路线,其勇气和底气何在?
近日,动脉网有幸对4C Medical的战略顾问JC Sun进行独家专访,探究4C Medical的创新思路与产品技术。

4C Medical 战略顾问JC Sun
JC Sun,PhD MBA,上海交大学士、硕士,后赴美国获PhD及MBA。JC在医疗创新商业化和资本化方面经验丰富,在医疗科技领域拥有20多项专利,并领导过新产品在美国、欧洲和亚洲的上市;他曾作为核心团队成员,在瑞士参与负责美敦力对英泰克5亿美元的收购和整合;同时,他也是通过股权融资和战略合作帮助全球先进医疗科技企业进入亚洲资本市场和临床市场的先驱之一。
自2003年以来,JC一直深耕医疗科技行业,曾担任过数十家企业的战略顾问,联合创立过数家医疗科技公司,如Big Sky Biomedical、Crossfire Medical、Mavin Wear。自2019年以来,JC担任斯坦福大学医疗创新转化平台SPARK Stanford顾问。2021年,他联合创立了FastWave Medical。2024年,他联合创立了斯坦福大学SPARK Global在中国的分支机构——SPARK China。
1经导管二尖瓣置换术:破解复杂MR治疗困境的潜在“兜底”方案
二尖瓣反流(MR)是指左心室(LV)的血液因二尖瓣的病变而逆流进入左心房(LA)。随着时间推移,反流造成的容量负荷过重会导致左心室扩张、二尖瓣环增宽等情况,进一步加剧二尖瓣反流,引起充血性心力衰竭、肺淤血、肺水肿等严重临床症状。[1]
由于解剖位置、血流动力学压力及多种病因等因素,二尖瓣反流是目前最常见的心脏瓣膜疾病。根据其产生的病理机制,二尖瓣反流可分为原发性二尖瓣反流(PMR)与继发性二尖瓣反流(SMR);前者由瓣膜本身结构病变所致,后者为心脏本身或瓣膜支撑结构病变所致。
目前,二尖瓣反流的治疗方法主要涵盖药物治疗、外科修复、外科置换、经导管修复、经导管置换几大主流技术路线。
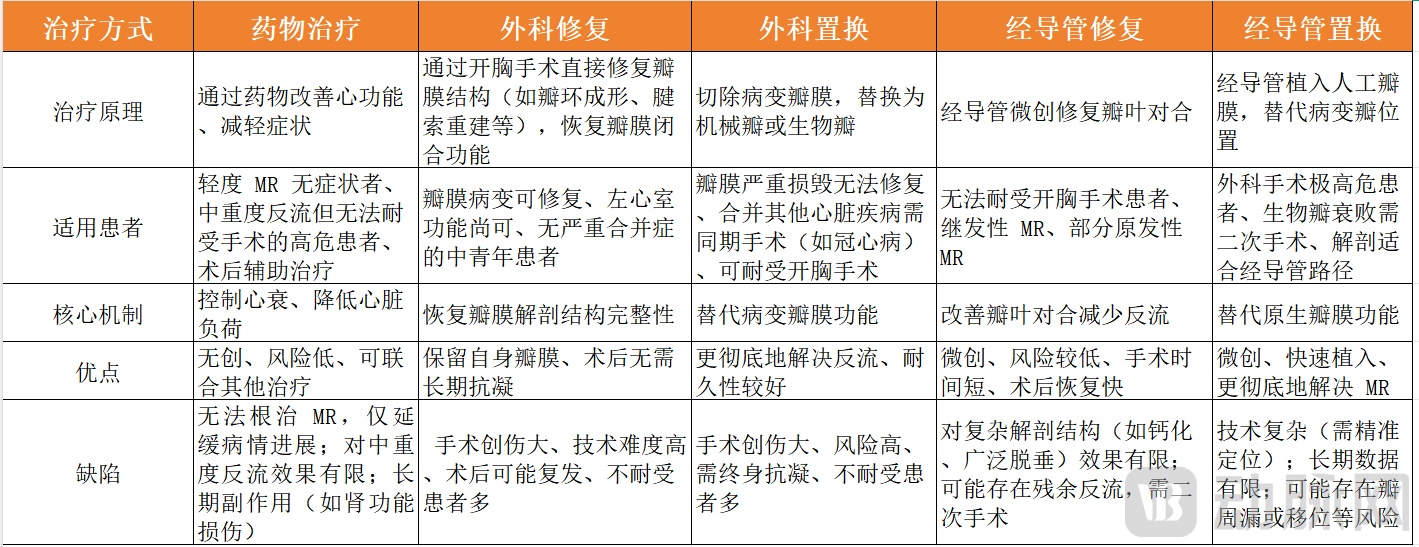 二尖瓣反流主要技术路线对比 动脉网制图
二尖瓣反流主要技术路线对比 动脉网制图
药物治疗仅作为辅助手段,无法逆转瓣膜结构病变。并且,药物治疗虽然可以延缓继发性 MR 发展,但目前尚无足够证据表明可降低原发性MR严重程度。当药物疗效不佳时,手术便成了最佳选择。
但在MR手术治疗中,关键痛点在于,由于患者选择意愿低、手术不耐受、技术难度大等原因,外科手术能覆盖的患者群体十分有限。“根据目前流行病学相关数据进行粗略估算,全球中重度二尖瓣反流患者超1亿人,但由于高龄与合并症、心功能严重受损等因素影响,约三成的患者不适宜进行开胸手术,而且由于患者选择意愿低,实际接受外科手术的比例低于1%。”JC介绍道。据估计,中国需干预的重症 MR 患者达 550 万,但仅 0.5%的患者接受了外科治疗。
未进行手术干预的MR生存患者,5 年内因心力衰竭住院率呈现大幅上涨的趋势。根据相关文献数据,未手术患者的总体 1 年至 5 年死亡率从 20%持续增长至 50%。[2]对于这类患者,经导管二尖瓣治疗便成为理想选择,因其无需开胸和体外循环、并发症风险较低、术后恢复较快等优势,在MR治疗中影响力不断扩大,近年来获指南临床认可度不断提升。
在符合解剖条件的MR患者中,修复路径通常为首选方案,具有避免人工瓣膜相关风险、更接近生理状态、避免长期抗凝等优势。但介入修复由于瓣膜厚度、钙化、瓣环尺寸等原因不适用于相当一部分患者,而且对MR消除程度相对有限,存在一定复发风险,尤其在心脏病进展的情况下,心脏结构和瓣膜可能变化,导致修复干预效果降低。而介入置换通过替换受损的瓣膜,有可能更彻底地解决MR,复发风险更低。
经导管二尖瓣置换术(TMVR)给无法进行二尖瓣外科手术、二尖瓣外科置换术后瓣膜衰败及二尖瓣环成形术后 MR 的患者带来了新的解决方案。并且,从术前阶段的患者适应证筛选来看,理论上,TMVR能干预多种病变,成为MR治疗潜在的“兜底方案”。随着TMVR技术进步,修复与置换的适应症可能进一步细化,二者将互补而非替代。
2开发兼具低输送剖面、操作便捷性与锚定稳定性的TMVR系统,4C Medical引领赛道差异化创新
目前,与以经导管缘对缘修复术(TEER)为代表的经导管二尖瓣修复(TMVr)相比,介入置换的进展相对缓慢。
从技术难点来看,与TMVr相比,TMVR赛道缺乏兼具低输送剖面、操作便捷性与锚定稳定性的成熟技术方案,这主要源于以下几方面:
第一,二尖瓣解剖结构复杂性较高,难以实现稳定锚定。二尖瓣瓣环呈马鞍形且具有动态伸缩性,不同于主动脉瓣的刚性结构,使得人工瓣膜难以实现稳定锚定,易导致瓣周漏或移位;并且,二尖瓣的瓣下结构复杂,周围存在腱索、乳头肌等精细结构,置换过程中需避免损伤上述组织,否则可能引发严重并发症;此外,二尖瓣承受左心室收缩期的高压力,对瓣膜的耐久性和稳定性要求更高。
第二,输送系统微型化挑战。相较于TMVR技术,TMVr系统往往剖面较低、操作相对简单,医生学习曲线较短,临床操作可行性更高,促进了该技术的普及。而TMVR系统需完成瓣膜置换,由于瓣膜整体体积较大,输送系统外径也较大。“如果不能降低输送剖面,不仅将限制血管入路的选择范围,更会直接导致部分解剖条件复杂的患者被排除在适应证之外,会极大程度影响该术式普及。”JC解释道。
第三,入路选择的局限性。经心尖入路创伤较大,并发症风险高;而经股静脉-房间隔入路虽微创,但技术难度大,需克服血管迂曲、房间隔穿刺定位等问题。并且,TMVR术式操作难度大,术者需长期训练才能掌握操作技巧,也在一定程度限制了技术普及。
从市场格局来看,在TMVr领域,雅培作为龙头企业已经进行了较为系统完善的市场教育,而置换赛道则缺乏类似的重磅先驱引领行业发展,入局者大多都处于探索期。
雅培的MitraClip 作为唯一一款获得 FDA/CE/NMPA 三方认证的TEER产品,推动了TEER装置真正走向临床。在此基础上,国内外企业不断入局,进一步推动该赛道发展。而反观TMVR领域,产品大多都处于临床试验阶段,仅有一款产品获 CE 认证(雅培的经心尖入路 Tendyne),尚无产品获批FDA。
上述因素叠加,使TMVR成为不折不扣的“高风险研发领域”。JC坦言,TMVR赛道可谓“尸骨累累”,诸多初创企业曾尝试入局,但受限于产品设计缺陷及临床验证障碍,不得不反复进行技术、方案迭代,导致临床转化进程普遍迟滞或惨遭折戟。即便行业巨头持续布局,高筑的技术壁垒也导致取得的实质性突破有限。
那么,可行的发展路径到底在哪里?4C Medical的差异化创新道路给行业提供了一种新思路。在入局企业大多保持谨慎的情况下,其颠覆式创新实属罕见。
一众企业中,4C Medical之所以能够脱颖而出,有两大关键点:从发展路径上,4C Medical拒绝惯性思维,开辟出一条没有跟随者的原创创新之路,并持之以恒深耕下去;从技术突破上,凭借独创设计,4C Medical开发出全球唯一在支架完全释放后仍可完全回收的低外径TMVR系统,解决了输送系统外径大、锚定困难、操作复杂的技术难题。
自成立之初,4C Medical便是一个十分引人注意的创新公司,凭借独创的二尖瓣置换思路,揽获了诸多创新大奖,很快引起行业广泛关注。

JC和4C CEO Saravana Kumar及团队
“4C Medical在TMVR领域的创新性在整个行业都毋庸置疑,但也从一开始就备受争议——这样前所未有的创新产品设计,是否真的可以在患者体内正常工作?”JC坦言。
面对质疑,4C Medical用实际行动回复——在公司正式招聘雇员、成立团队后仅一年多,便以极强的团队执行力在一位70多岁的加拿大患者身上开展了其核心产品AltaValve的第一例人体临床试验。试验采用经心尖入路方式,在AltaValve植入体内的三年后,这位起初连一句话都讲不完整的老人心脏恢复到了五十岁左右的状态。JC强调,这一经心尖病例的试验结果意义非凡,它证明了AltaValve系统的植入物长期表现良好,安全性、有效性得到了初步验证。自此之后,AltaValve的植入物设计都没有变化,后续的创新均围绕输送系统进行。目前,4C Medical已经启动覆盖美国、日本及欧洲地区的多中心临床试验计划。
3坚持“摒弃惯性思维”的研发思路,产品已在美、欧、日开展多中心临床试验
4C Medical创始人Jeffrey Chambers是一位心内科临床医生,对于复杂心脏病变的理解远超一般创业者,这决定了公司的创新探索从最初便带有“以临床需求为主,以科技工具为辅”的浓厚底色。JC表示,4C Medical给行业的一大启示是,在医疗器械开发过程中,要十分警惕“惯性思维”。
“在惯性思维影响下,当遇到相似问题时,人们总倾向于从以往经验中寻找解决方法。在医疗器械尤其是创新领域,这会导致高昂的试错成本,包括金钱和时间成本。”JC举了一个十分通俗形象的例子来说明,“当人们通过榔头成功固定钉子后,就容易形成思维定式,以后只要遇到钉子便会想起用榔头敲击。但如果遇到的是螺丝钉,榔头的冲击作用便是无效的,而需采用适配螺纹结构的螺丝刀。”
JC坦言,他认为,目前一些TMVR企业之所以花费大量时间和资金却收效甚微,一大重要原因便在于受惯性思维束缚,没有真正从问题本身出发。“而4C Medical在充分理解并利用二尖瓣解剖学差异的基础上,进行了真正意义上的创新思考与设计,我认为这是它与其他公司在路径选择上的最大不同。”
JC认为,一个好的医疗创新,在概念验证的初期阶段,应当纯粹地基于“以临床需求为主,以科技工具为辅”的原则,尽可能不要受到资本、财务、政治等因素的干扰及惯性思维的禁锢。而在概念验证中期确定具体设计方案时,则需要考虑到知识产权、法规、市场时机、竞争、医保、商业化和资本化等要素。在这一过程中,应将“简单易用、成本易控、法规易行”作为重要衡量标准。4C Medical便是采用了这样的创新路径。
首先,一个技术不论如何先进,如果全球只有极少数医生能够掌握,那么该术式及相关技术便不可能大规模普及。而4C Medical围绕“简单易用”这一核心对AltaValve的输送系统做了不下于4轮改进,使其完全可回收,且许多设计沿用了雅培的MitraClip输送系统的设计元素,使操作者更易上手;在“成本易控”方面,构造简单的产品更容易实现规模化生产并迅速降低成本,比如AltaValve的球形支架虽然有几个不同的尺寸,但其瓣膜都是统一尺寸和标准,使其更适合规模化生产并降低成本;“法规易行”上,4C Medical 采用HBD路径,在美国、欧洲和日本同步开展多中心临床试验,实现三大主要市场的注册批准同步推进,避免分阶段申报模式可能导致的冗长审批周期,缩短产品全球上市时间。
4全球唯一在支架完全释放后仍可完全回收的低外径TMVR系统,平衡技术创新与临床操作安全性
装置锚定的稳定性向来是TMVR系统的一大难点。传统 TMVR系统通常将瓣膜锚定在二尖瓣环上,但瓣环钙化、解剖变异等问题常导致固定困难,且易进一步加剧左心室流出道狭窄。同时,二尖瓣环根部有许多神经节,若装置对其产生过度压迫,可能导致心脏电生理紊乱。而AltaValve系统采用了独特的心房固定设计,有效化解了这一难题。
AltaValve 系统采用了创新的球形支架设计,有望成为全球首个仅需心房固定即可解决二尖瓣反流问题的治疗方案。该设计将血管腔内治疗中支架的力学支撑原理移植至心脏解剖结构中,并针对心房结构的特殊性,通过多模态影像学分析筛选出最常见的解剖学参数,采用适度尺寸过盈设计,使球形支架在目标区域形成稳定的力学锁定。
具体而言,AltaValve系统采用球形镍钛合金支架,支架扩张后能与左心房顶部及后壁紧密贴合,自适应左心房的解剖形态,均匀分散压力,避免局部应力集中。该设计利用心房组织的自然弹性提供支撑,无需依赖瓣环的机械锚定。
这使得AltaValve能为因瓣膜或瓣环钙化而无法使用瓣环锚定式TMVR系统的患者提供新的治疗选择,且无需考虑左心室流出道狭窄这一制约因素。此外,支架底部具有高分子材料制作的裙边设计,可以有效防止瓣周漏。“因此,与目前其他的TMVR系统相比,AltaValve有望覆盖更广泛的病人群体,潜在市场十分可观。”JC补充道。
同时,AltaValve的心房固定设计可以动态适应心脏形态的变化。在心脏重塑过程中,传统的瓣环或瓣膜下锚定方式无法动态适应心脏变化,导致系统适用性降低。而AltaValve的球形支架柔软且具有良好的自适应能力,在心脏重塑之后也可实现稳定锚定。
除此之外,AltaValve还有一大值得关注的亮点——无需完全取缔原生瓣膜。一般而言,TMVR系统需要取缔患者的原生瓣膜,因此自人工瓣膜植入的那一刻起便会受到血流的全载荷冲击。而AltaValve系统则是在患者原生瓣膜上方植入球形支架,采用“瓣后瓣”设计,不仅减少动载荷有助于降低瓣周漏概率,还有助于提高人工瓣膜的疲劳寿命,并可以治疗修复失败或修复后MR复发的患者。“由于心脏在重塑过程中会收缩,将进一步减少远期瓣周漏或移位发生的概率,4C Medical正是基于对心脏逆向重构进程中锚定区解剖结构动态演变的预判,用发展的眼光进行创新设计。”JC解释道。
这一方面能够提升TMVR系统的耐久性,另一方面使得原生瓣膜在与人工瓣膜互动的过程中有效减少血液滞留死角,降低血栓发生概率。并且,由于保证了患者的原生瓣膜维持解剖完整性,哪怕TMVR系统没有成功释放,AltaValve也能确保患者术后临床状态不劣于术前基线水平,这一可逆性操作优势突破了现有TMVR技术难以实现临床安全保障的瓶颈。另外,AltaValve系统采用的高分子材料较少,球形支架在植入人体一个月内便可以被内皮化,因此有效降低了TMVR系统植入后长期抗凝导致的大出血风险。
值得注意的是,AltaValve系统还是全球唯一在支架完全释放后仍可完全回收的低外径TMVR系统,这与其球形支架设计息息相关——如果锚定装置上有任何倒刺或挂钩设计,那么系统便无法实现完全回收。此外,这还得益于AltaValve独特的输送系统设计。AltaValve输送系统的远端可以实现三维精准可控,允许术者根据患者独特的二尖瓣解剖结构实时调整导管角度和位置,确保器械与病变部位的精准匹配,在应对迂曲血管或狭窄通路时优势尤为明显。
“在这种复杂高难度手术中,医生需要应对各种不确定性,而如果系统能够完全回收,不仅会增强医生操作过程中的信心、提升容错率、降低操作门槛,还能大大降低患者的手术风险。”JC补充道。
在入路方式上,AltaValve采用经股静脉-房间隔穿刺方式,有效降低了经心尖入路导致的较高死亡风险,且其24 Fr瓣架网孔能为患者后续的左心房介入手术提供可能。
5写在最后
“4C Medical为医疗创新创业从业人员提供了一个很好的榜样——如果真的能从临床需求出发,以科技工具为辅助,是可以走出一条十分具有前景、且得到临床和资本市场认可的道路的。”JC认为,4C Medical所走出的医疗器械原创创新路径,是它对于行业更有意义的价值所在,甚至大于AltaValve产品本身带来的震撼。
JC表示,“目前4C Medical临床试验进展顺畅,我也非常期待后续临床及上市能尽快完成,让这一创新技术普惠更多患者。”未来,4C Medical将加速推动AltaValve的临床试验,以钙化病变较为严重的高风险二尖瓣反流患者为切口,铺开商业化版图,实现更广泛的患者覆盖。作为TMVR领域的黑马与创新先锋,4C Medical将创造出怎样的新奇迹,我们拭目以待。
关于SPARK China
SPARK医疗创新转化平台于 2006 年起源于斯坦福大学,采用基于设计思维的方法,强调从用户需求出发,早期融入临床需求、监管要求和财务评估等因素,确保学术研究与产业现实紧密对接,提高转化成功率。该计划专注于药物、器械和诊断项目的概念验证,为项目提供资金支持与专家指导。目前,SPARK平台已在全球20多个国家的多所顶级高校机构落地,转化成功率高达50%。
2024 年 11 月,SPARK China 正式落地上海,由上海交通大学生物医学工程学院先进医疗芯片研究所与斯坦福大学合作成立。作为 SPARK GLOBAL(2015年基于斯坦福大学 SPARK 平台成立的非营利组织,覆盖全球超 40 家学术机构)的成员,SPARK China 汇聚国内顶尖科研力量,沿用 SPARK 经典模式,挖掘高校与医院创新项目,提供资金、顾问服务等支持,整合斯坦福大学 SPARK 方法论,借助 SPARK GLOBAL 全球网络,致力于加速中国本土医疗创新,推动学术成果转化为临床解决方案。
相关链接:助力医疗创新迈过死亡谷,斯坦福SPARK计划落地中国
注:本文仅代表JC Sun个人观点
参考资料:
1.Douedi S, Douedi H. Mitral Regurgitation. In: StatPearls. Treasure Island (FL): StatPearls
Publishing; April 7, 2023.
2.Goel SS, Bajaj N, Aggarwal B, et al. Prevalence and outcomes of unoperated patients with
severe symptomatic mitral regurgitation and heart failure: comprehensive analysis to determine
the potential role of MitraClip for this unmet need. J Am Coll Cardiol. 2014;63(2):185-186.
3.蛋壳研究院 《2024 经导管二尖瓣介入治疗行业白皮书——TEER 强者恒强,中国应用将驶入快车道》





























