4月11日,由中国创新企业自主研发的多模态冠脉光学相干断层成像(OCT)系统及配套导管,正式通过美国食品药品监督管理局(FDA)认证,成为全球首个获得FDA认证的多模态冠脉OCT系统,也是中国首个获得FDA批准的腔内影像设备,标志着我国在高端医疗设备领域取得重大突破。
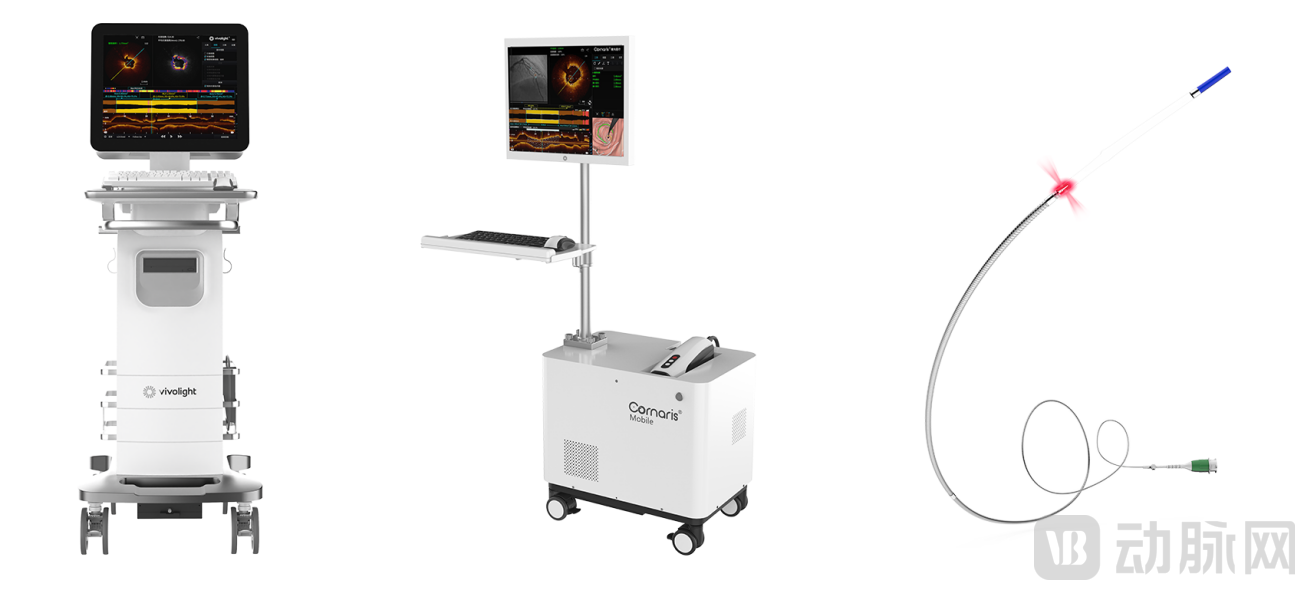
获批 FDA 的三款产品
此次获批的多模态OCT系统由深圳市中科微光医疗器械技术有限公司(以下简称“微光医疗”)自主研发,仅需一根导管单次 OCT 回拉即可获取血管结构、血流功能、风险斑块识别的全面诊断信息。这一技术突破,成功解决了以往多种设备难以集成的问题,也无需多条导管耗材,显著降低手术时间与耗材成本,大幅提升了手术效率和诊断精准度,为临床医生提供了更有力的诊疗支持。
据介绍,微光医疗成立于2012年,在激光医学、光纤导管及影像算法等领域拥有十三年以上的经验积累。此前,微光医疗OCT设备已经打破了跨国公司的长期主导,国内市场占有率仅次于跨国巨头雅培企业。2023年微光医疗成为进入海外市场的首家中国OCT厂商。
微光医疗创始人CEO朱锐表示:“本次通过FDA认证,不仅意味着我们打开了美国的销售通路,同时也获得东南亚、中东、拉美等超过20个国家/地区的市场准入资格,这将会极大地加速微光医疗OCT产品在多个国家的注册流程,促进企业的全球化布局,为全球输出来自中国的解决方案。”
数据显示,我国心血管疾病患者已超3.3亿人,腔内影像技术的普及将显著提升PCI手术精准度,降低术后并发症风险。2024年,欧洲心脏病学会(ESC)将OCT、IVUS(血管内超声)等腔内诊断技术升级为慢性冠脉综合征管理指南的Ia级推荐(最高推荐等级)。然而,传统 OCT设备多为单功能设计,难以满足复杂冠脉病变的精准诊断需求,同时高昂的设备和耗材成本仍是制约其普及的主要瓶颈。
值得关注的是,微光医疗自主研发的导管部件已实现全面国产化,且核心模块由机器人自动化生产,大幅降低生产成本,有效应对当前动荡外贸环境下的出口关税壁垒。
此次FDA认证不仅是企业层面的技术认可,更标志着我国高端医疗装备从 “国产替代” 迈向 “全球创新”。随着该技术加速进入国际市场,中国医疗器械正以技术创新为纽带,为全球心血管疾病防治贡献 “中国方案”,推动高端医疗装备领域从 “跟跑” 向 “并跑领跑” 的历史性跨越。





























