年龄相关性黄斑变性(AMD)是60岁及以上人群不可逆视力丧失的主要原因,全球约有1.96亿人患有此病。
不久前,密歇根大学医学中心研究团队在《细胞·干细胞》(Cell Stem Cell)期刊发表首次人体临床试验结果,通讯作者Rajesh C. Rao博士及其团队使用源自成人眼库组织的视网膜色素上皮干细胞(RPESC)治疗晚期干性AMD患者,在安全性得到确认的基础上,视力较差组患者12个月时平均视力提高21.67个字母,在晚期干性AMD患者中出现了前所未见的改善幅度。

(来源:Cell Stem Cell)
黄斑变性分为干性和湿性两种类型,超过90%的AMD患者患有干性形式。干性AMD的核心病理机制是视网膜色素上皮(RPE)细胞的功能障碍和最终丢失,而RPE细胞位于视网膜光感受器细胞下方,负责为光感受器提供营养支持、代谢废物清除和视觉循环维持等关键功能。
疾病进展过程中,RPE细胞在早期阶段出现功能障碍,晚期则死亡且不再生,大量RPE细胞丢失后形成地理萎缩(GA)区域,在眼底呈现为苍白病灶。正常的RPE细胞层在这些区域消失,RPE细胞丢失导致上覆的视网膜光感受器细胞失去支持,继而出现功能障碍并死亡,中央视力因此受损。患者的周边视力保持正常,但中央视野受到影响,阅读和识别面孔等依赖中央视力的日常活动变得困难。
目前的治疗方法可以减缓疾病进展,但没有一种能够恢复已经丢失的视力。
近年来,干细胞基础的细胞替代疗法成为研究热点,旨在将新的RPE细胞植入萎缩区域以替代丢失的细胞。多能干细胞(PSC)衍生的RPE移植已显示出一定的安全性和适度的视力改善,但由于PSC需要广泛分化以最小化肿瘤风险。其植入效率和视力恢复效果仍有提升空间。
本研究采用的成人RPE干细胞具有独特优势,它们源自眼库捐献组织的天然RPE层,已经致力于RPE谱系,无需从多能状态分化,因此缺乏肿瘤形成潜力,可以在分化程度较低的祖细胞期进行移植。
Rao博士在研究中指出:“成人RPESC的独特之处在于它们已经定向于RPE谱系,这使我们能够在更早期的祖细胞阶段进行移植,而这一阶段具有更强的运动性和植入能力。”
本研究是一项首次人体、开放标签的1/2a期剂量递增临床试验,主要评估安全性和耐受性。研究团队使用源自单个供体(73岁男性)的RPESC,经实验室培养两代后进一步分化4周,获得RPESC衍生RPE(RPESC-RPE-4W)细胞产品。
临床前研究数据表明,分化4周的中间祖细胞期细胞在植入效率和视力挽救方面表现优于其他发育阶段,这一发现与中枢神经系统其他细胞类型移植研究的结果相一致。
试验招募了6名晚期干性AMD患者,平均年龄76岁,分为两个亚组:队列1a包括3名基线视力为20/200-20/800的视力较差患者;队列1b包括3名基线视力为20/70至20/200的视力较好患者。所有患者的视力较差眼接受了最低剂量50,000个RPESC-RPE-4W细胞的移植。
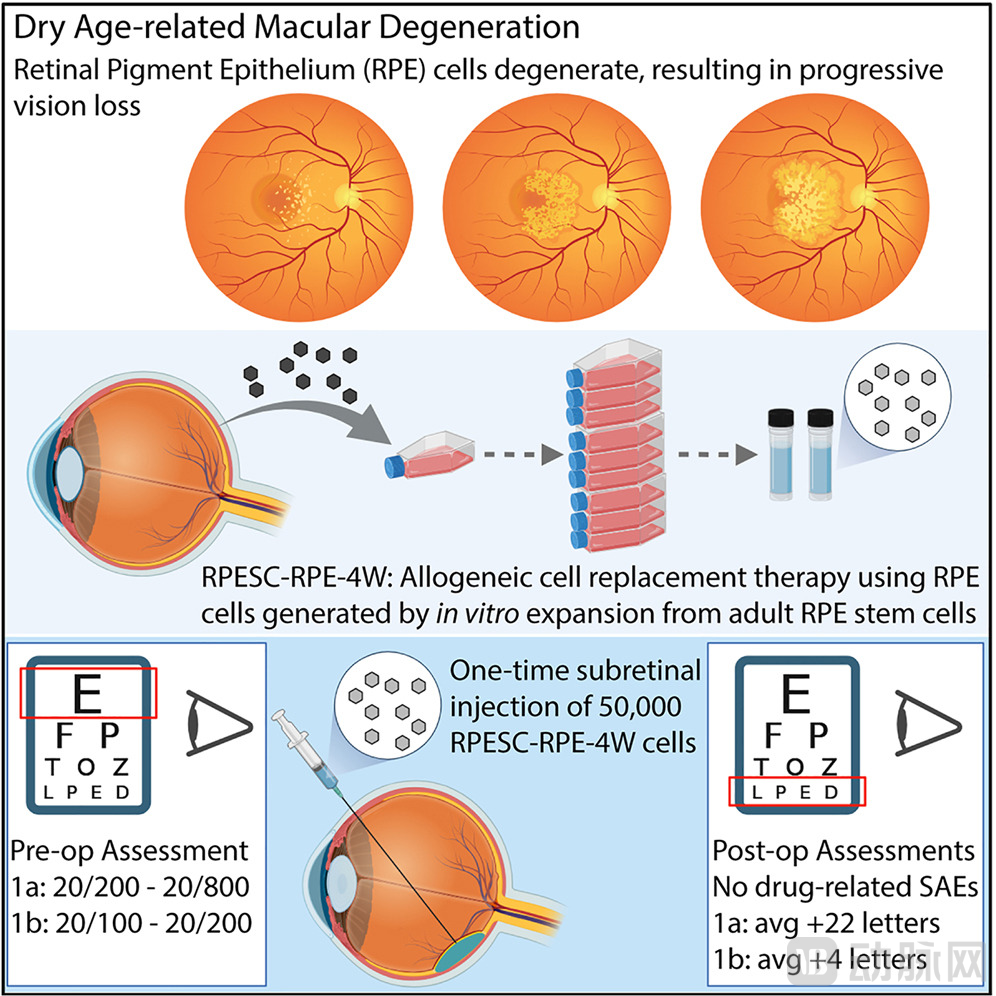
图:治疗流程示意图(来源:Cell Stem Cell)
安全性结果显示,所有6名患者在12个月随访期间均未出现肿瘤形成、显著炎症或研究产品相关的严重不良事件。术后的轻度炎症通过局部类固醇治疗得以控制。18例研究眼不良事件均为轻度(1级或2级),包括视网膜内出血和结膜下出血等常见手术并发症,均自行消退。
值得注意的是,研究未观察到PSC-RPE移植常见的视网膜前膜形成,这可能归因于RPESC形成非RPE后代的受限潜力以及较低的上皮-间质转化倾向。研究团队强调,这种安全性特征对于干性AMD患者群体尤其重要,因为这一人群通常年龄较大,对治疗相关并发症的耐受性较低。
疗效数据方面,视力较差的队列1a患者的视力出现了显著改善。早期糖尿病视网膜病变治疗研究(ETDRS)视力表测试结果显示,这些患者治疗眼的平均最佳矫正视力(BCVA)在1个月时增加21.0个字母,这一改善维持到12个月时为21.67个字母。未治疗眼在同期平均下降1.33个字母,两眼之间的差异达到23.0个字母。
个体数据显示,受试者-002从基线29个字母提高到12个月时的43个字母,受试者-004从35个字母提高到50个字母,受试者-005从32个字母提高到68个字母。视力较好的队列1b患者在6个月随访中平均增加3.0个字母,未治疗眼下降1.0个字母。
研究者指出,这种程度的视力增加在晚期干性AMD患者中此前未见报道,超过了其他干性AMD RPE替代试验的结果。Rao博士对此表示:“我们对接受成人干细胞衍生RPE移植的最严重受影响患者的视力增加幅度感到惊讶。这种视力增加水平在晚期干性AMD患者中从未见过,这为那些几乎失去所有中央视力的患者带来了希望。”
本研究的结果在多个方面具有临床意义。首先,成人RPESC-RPE-4W细胞展现出良好的安全性特征,未出现肿瘤形成和显著炎症,也未观察到视网膜前膜形成,这些特征将其与PSC基础的RPE替代疗法区分开来;其次,视力较差患者的视力改善数据为理解晚期疾病的治疗潜力提供了新的视角。
研究者提出,晚期疾病中天然RPE细胞堆积较少,为移植细胞提供了更多植入空间,同时RPE细胞替代比例更高。研究团队分析认为:“这一发现挑战了我们对晚期干性AMD治疗潜力的理解。即使在疾病晚期,通过提供功能性RPE细胞支持,休眠的光感受器细胞仍可能被挽救并恢复功能。”
研究团队目前正在跟踪接受150000和250000个细胞的中剂量和高剂量患者,以探索剂量-效应关系。该试验在2025年初获得美国FDA的再生医学先进疗法(RMAT)指定,独立审查认为其具有“解决干性AMD患者未满足医疗需求的巨大潜力”。
Rao博士表示:“获得RMAT指定是对我们研究潜力的重要认可。这表明FDA认为这项技术有潜力为干性AMD患者带来重大临床获益。”如果更高剂量队列继续显示良好的安全性和疗效,将进入后续的关键性临床试验,扩大样本量并采用随机对照设计以确定确切疗效。
未来研究还需要优化细胞递送技术,探索GA病灶覆盖程度、疾病亚型和形态特征对治疗反应的影响,以及确定最佳治疗时机和患者选择标准。研究团队指出,随着更多数据的积累,他们将能够更好地理解哪些患者最有可能从这种治疗中获益,以及如何优化治疗策略以获得最佳效果。
作为一项小规模的早期阶段试验,密歇根大学医学中心团队的这项首次人体临床试验为干性AMD治疗提供了新的数据,其结果为后续更大规模研究提供了基础,也为全球近2亿AMD患者带来了视力恢复的潜在选择。随着中高剂量队列数据的陆续公布和后续关键性临床试验的开展,这一创新疗法有望为干性AMD患者提供新的治疗选择,改变目前只能延缓疾病进展而无法恢复已丢失视力的治疗困境。




























