日前,北京协和医院发布科技成果转化公示,医院拟将“一种针对RDH12突变的基因治疗药物”相关专利技术,以专利权转让方式成功转化予北京因诺惟康医药科技有限公司。本次转让的拟交易价格为168万元人民币,并附加未来销售额5%的提成。
该专利技术的发明人为北京协和医院睢瑞芳教授领衔的研发团队。团队长期致力于遗传性眼病,特别是视网膜变性疾病的临床诊疗与基础研究,在基因治疗领域积累了深厚的专业基础。
睢瑞芳教授是北京协和医院眼科学科带头人,担任主任医师、教授及博士研究生导师,专注于遗传性眼病诊疗与科研工作。
她在中国首次报道Stickler综合征、家族性晶状体异位等多种罕见眼病,牵头研发X连锁视网膜劈裂基因治疗药物IVB102注射液并推动其进入临床试验。睢瑞芳于华西医科大学本科毕业,后获北京协和医学院博士学位,并在美国Iowa大学等机构完成眼遗传病博士后研究。她承担多项国家级科研项目,发现多个视网膜变性及高度近视致病基因,荣获北京市科技进步二等奖等荣誉。
本次专利技术的受让方北京因诺惟康 (InnoVec Biotherapeutics Inc.or InnoVecBio)是一家致力于解决人体所有组织和器官基因递送难题的公司,致力于通过开发精准安全高效的组织靶向性载体,使基因治疗能够被广泛地应用到各种疾病人群当中。
公司围绕腺相关病毒(Adeno-associated virus, AAV)人体应用未解决的问题,用AI辅助,打造EASI-AAV平台,开发了针对视网膜,神经系统和肌肉的载体。基于这些载体的基因治疗药物,已经或者将要陆续进入临床。
本次转化的成果聚焦于RDH12基因突变,该突变是导致Leber先天性黑蒙(LCA)及遗传性视网膜病变(IRD)的重要原因之一。团队创新性研发的基因治疗药物,旨在从根源上修复致病基因缺陷,为罹患此类致盲性眼病的患者带来重见光明的希望。
遗传性视网膜疾病是一组由基因突变导致的疾病,这些疾病造成视网膜结构和功能进行性受损。该类疾病具有高度的临床和遗传异质性。目前已知有近300个基因与之相关,这类疾病是不可逆性致盲性眼病的最主要原因。视黄醇脱氢酶12(RDH12)基因突变是导致严重视网膜退行性病变的重要原因,该基因编码的RDH12蛋白在视觉循环中扮演关键角色。
视觉循环是维持视觉功能必不可少的生化过程。在光线刺激下,视网膜光感受器细胞内的视色素分子会发生异构化,这个过程会释放出全反式视黄醛,同时产生视觉信号。
为了维持视觉的持续,全反式视黄醛必须被还原为全反式视黄醇。接着,它被运送到视网膜色素上皮细胞中重新异构化为11-顺式视黄醛,最后返回光感受器细胞与视蛋白结合,再次形成对光敏感的视色素。RDH12是催化“全反式视黄醛还原为全反式视黄醇”这一步骤的关键酶。
当RDH12基因发生致病突变时,其编码的酶活性会显著降低或丧失,这导致视觉循环中断。全反式视黄醛具有细胞毒性,其长期积累会引发光感受器细胞的代谢紊乱和氧化应激,最终导致细胞凋亡和视网膜进行性变性。
临床上,RDH12基因突变可引起多种严重表型。这些包括Leber先天性黑蒙、早发严重性视网膜营养不良、视网膜色素变性和锥杆细胞营养不良等。
大多数患者在儿童时期视力即严重受损。他们伴有显著的黄斑萎缩。随着病情持续进展,患者视野会逐渐缩窄,导致夜盲症状明显,最终多生活难以自理。
目前,针对由RDH12突变导致的视网膜疾病,临床上尚缺乏有效治疗方法,现有手段无法阻止或逆转疾病进程。现有的临床方案主要以对症支持和低视力康复为主,例如为患者配戴助视器、提供遗传咨询、进行定向行走训练等。
这些方法旨在利用患者的残余视力,提高其生活质量,但它们无法解决疾病的根本病因,即RDH12蛋白的功能缺失。
因此,患者的视网膜光感受器细胞仍在持续死亡,视力能不可逆转地丧失。这种无药可医的现状给患者及其家庭带来沉重负担。同时也凸显了开发根本性治疗方法的紧迫性。基因治疗技术为这类单基因遗传病带来了希望。其核心思路是向病变细胞中递送正确的基因拷贝,从而补偿突变基因的功能缺失。
然而,开发此类疗法面临巨大挑战。这需要选择高效且安全的病毒载体将治疗基因递送到目标细胞,还需要确保基因在体内能够长期、稳定且安全地表达出正常功能的蛋白质。
面对以上关键问题,团队提供了一种针对RDH12基因突变的基因治疗药物,其核心技术是利用重组腺相关病毒作为基因递送载体。
AAV是一种非致病性的微小病毒。经过人工改造后,可剔除自身遗传物质,装载治疗性基因片段。它成为一种安全高效的基因递送工具。该专利构建的AAV病毒内部装载经过密码子优化的人类RDH12基因互补DNA。密码子优化是一种生物工程技术,它在不改变蛋白质氨基酸序列的前提下,对基因核苷酸序列进行重新设计。
这类似于将指令改写为细胞更熟悉的高效语言。通过优化可显著提高RDH12蛋白在人体细胞内的表达效率,这是确保治疗效果的关键步骤。
该药物采用三质粒包装系统在HEK 293T细胞中制备病毒。此系统能高效、特异地生产只携带治疗基因的重组AAV病毒。这些病毒不具备自我复制能力。更重要的是,本发明选用了人工设计的AAV衣壳血清型IVT13。
衣壳是病毒的外壳,如同递送系统的钥匙。血清型IVT13这把钥匙能有效识别并进入视网膜光感受器细胞,从而将正常RDH12基因精准递送到病变靶细胞中。
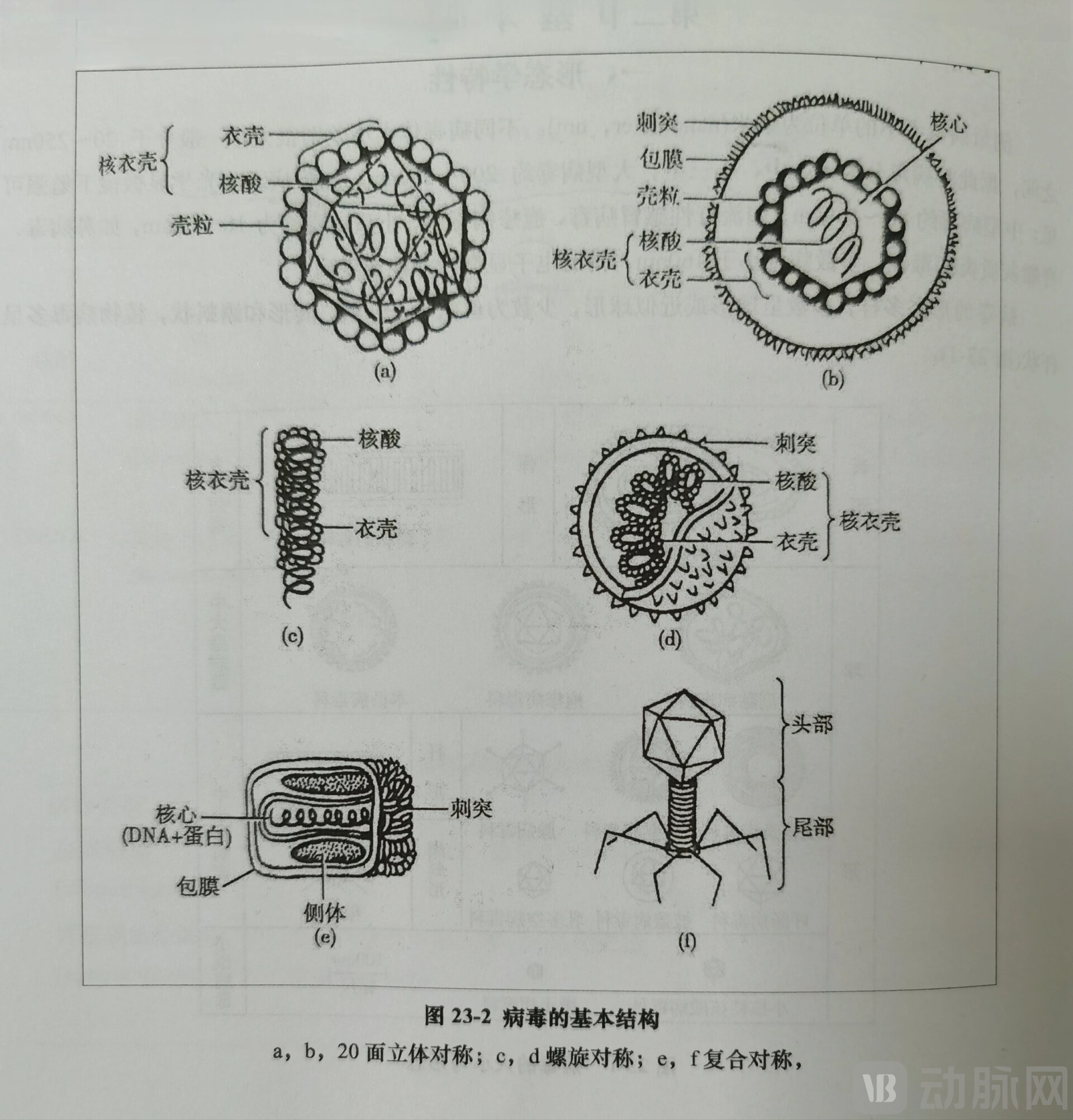
图片来自《陈阅增普通生物学》
在给药方式上,该发明创新性地采用玻璃体腔注射途径,玻璃体腔是眼球内部充满透明胶状物质的空间。
与传统视网膜下注射相比,玻璃体腔注射是一种微创操作。它只需将药物注射至玻璃体腔内,无需直接接触和剥离脆弱的视网膜结构。
这种方法显著降低了视网膜医源性损伤风险。它减少了出血、视网膜脱落等严重并发症的可能,同时使手术操作更简便安全,更易于临床推广。
一旦注射进入眼内,AAV病毒载体便会感染视网膜光感受器细胞。病毒载体携带的优化人类RDH12基因会在细胞核内持续稳定存在,它会指导细胞合成完整的、具有正常生物活性的RDH12蛋白。
RDH12是视觉循环中的关键酶。它负责将全反式视黄醛催化还原为全反式视黄醇。在RDH12基因突变患者中,该酶功能缺失或大幅降低。这导致视觉循环中断,有毒性的全反式视黄醛堆积,最终引起光感受器细胞死亡。
因此,该基因治疗药物的根本作用机制是通过一次性给药实现的,它在患者视网膜细胞内建立长期、稳定的功能性RDH12蛋白生产源头。
这些新产生的正常蛋白能弥补基因突变导致的功能缺陷,它们重新启动停滞的视觉循环,清除有毒代谢物,从而从根源上挽救濒临死亡的光感受器细胞,最终达到改善患者视功能或显著延缓疾病进展的治疗目的。
这为目前无药可医的RDH12突变患者提供了首个有望改变疾病进程的根治性疗法。
当前,由RDH12基因突变导致的遗传性视网膜疾病始终面临着无有效根治手段的临床困境,这一严峻现状正推动全球创新力量竞相布局基因治疗这一前沿赛道。
健达九州专注中枢神经系统疾病和眼科疾病基因治疗创新,该公司在眼科基因治疗赛道的核心在研产品为GA001注射液,这款药物主要针对视网膜色素变性导致的晚期盲症展开研发。其新药临床试验申请已于2025年8月正式获得国家药品监督管理局药品审评中心受理,这标志着该药物在国内的临床研究进入规范化推进阶段。在国际层面,该药物还获得了美国食品药品监督管理局授予的快速通道资格。
辉大基因是一家专注于基因编辑技术和基因治疗药物开发的全球性生物技术公司,其研发管线涵盖眼科、中枢神经等多个关键领域。在眼科基因治疗赛道,辉大基因的核心在研产品为HG004。这是一款采用重组腺相关病毒AAV9型载体的基因替代疗法,它通过单次给药将正常RPE65基因递送至视网膜。该产品专门用于治疗由RPE65基因突变引起的Leber先天性黑蒙,尤其是LCA2型。
在研发阶段方面,HG004已取得显著进展。2023年10月,其首个临床研究“LIGHT光”结果显示所有受试者均实现视网膜感光度改善。研究中未观察到视网膜脱离等严重不良事件。同时,HG004是国内自主研发的首个获得美国FDA授予孤儿药及儿科罕见病药物双认证的AAV眼科基因疗法。其国际多中心临床研究申请已获中国国家药品监督管理局药品审评中心与美国FDA的新药临床试验许可。
在国际赛道上,Opus Genetics是一家以患者为中心的基因治疗公司,该公司核心聚焦遗传性视网膜疾病领域。它致力于通过创新的腺相关病毒载体基因治疗技术,为这类罕见致盲性疾病患者开发治疗方案。
在眼科基因治疗赛道,该公司的核心在研管线包括两款AAV载体介导的基因治疗药物。OP-GX-001针对LCA5基因突变导致的Leber先天性黑蒙,OP-GX-002则针对RDH12基因突变引起的Leber先天性黑蒙。二者均通过视网膜下递送AAV8载体,将正常的目标基因递送至患者视网膜以实现基因增补治疗。目前这两款管线均处于临床前阶段,已开展支持新药临床试验申请的试验。
从整体研发态势来看,RDH12相关治疗方案的开发已经形成了多元化的技术路线。除了基因替代疗法外,还包括不同血清型载体的探索与应用。这些研究为解决该致病基因导致的视力损伤问题提供了更多可能的选择。
展望未来,随着更多研发项目的推进和临床数据的积累,RDH12靶点的治疗策略有望进一步完善。该领域的持续发展将为遗传性视网膜疾病患者带来新的治疗希望,并推动眼科精准治疗领域的整体进步。




























