近日,翱锐生物自主研发的利为平®—TSPYL5、RASSF1A、DAB2IP、OTX1、PTPN18、HIST1H3G 6基因甲基化检测试剂盒(PCR荧光探针法)以及配套AI模型分析软件,正式获得国家药监局(NMPA)批准上市(国械注准20253402195/国械注准20253212452)。这一里程碑式的突破,标志着肝癌早诊早筛技术迈入“精准化”“数智化”的新阶段。
01
肝癌早诊:中国癌症早诊突破口
中国肝癌发病率居高不下,疾病负担沉重。据国家癌症中心2024年最新发布的中国恶性肿瘤疾病负担情况,2022年中国癌症新发病例及死亡病例数居全球之首[1]。尤为引人注目的是,肝癌发病率已攀升至我国第四位,死亡率更是超越胃癌,位居第二位,成为消化系统恶性肿瘤之首。
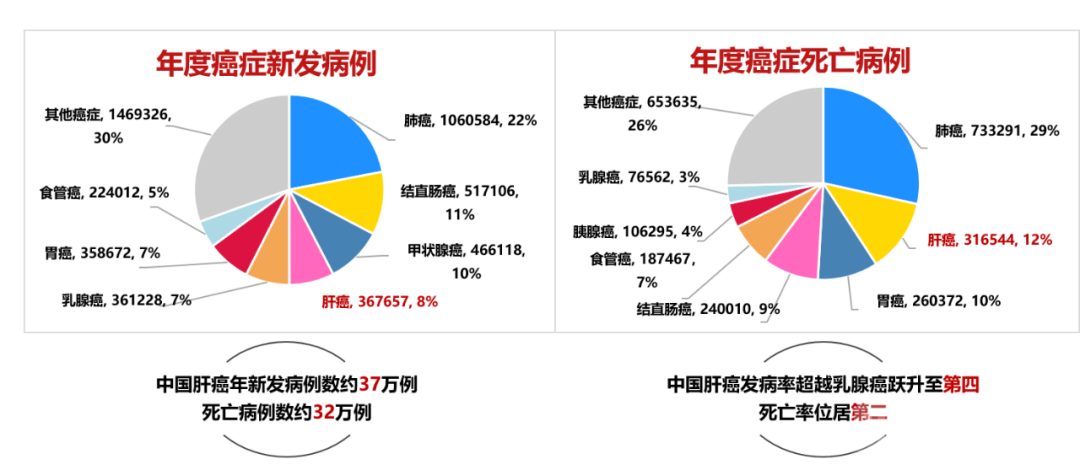
肝癌起病隐匿,发展快,恶性程度高,确诊时一般已达中晚期。研究表明,早期发现并提前治疗能够显著提升肝癌患者的五年生存率。然而,我国肝癌五年生存率不足15%,肝癌早诊率仅为21.4%,与日韩等邻国存在显著差距[2-6],肝癌防治形势严峻。对肝癌高危人群进行高效早筛早诊,是实现诊断与治疗分期前移、提高生存率、降低治疗费用的关键所在。
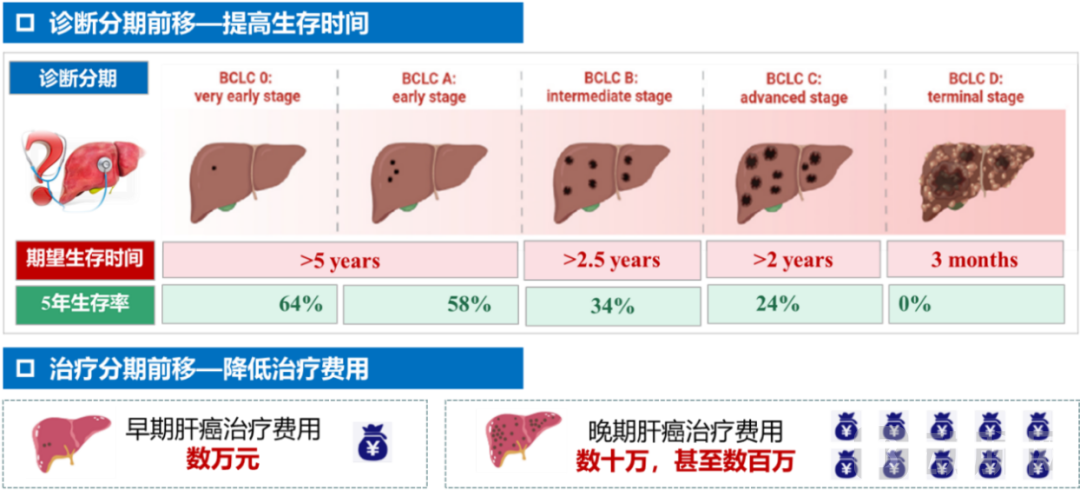
现有肝癌早诊手段:局限性明显
● 甲胎蛋白失灵:30%-40%患者的甲胎蛋白(AFP)始终阴性,早期灵敏度不足50%;
● 超声局限:在肥胖人群及不断增加的非酒精性脂肪肝病(NAFLD)人群中对肝癌的检出率显著下降,对小肝癌灵敏性不足;
● 影像滞后:特定人群难检测,对操作者经验依赖性强,价格高,难以用于大规模早筛早诊;
● 靶点覆盖局限:现有甲基化产品仅检测2-3个基因,遵循单阳性法则,难以全面覆盖检测窗口期以及癌症作为复杂疾病的分子层面多通路改变。
02
翱锐生物利为平®:直击痛点,精准升级
■ 6基因协同检测 | 多通路覆盖,检测性能提升
肝癌的发生通常伴随多基因甲基化异常,利为平®基于全球前沿肝癌甲基化研究,通过同步分析 TSPYL5、RASSF1A、DAB2IP、OTX1、PTPN18、HIST1H3G 6个肝癌驱动基因的甲基化异常,精准捕捉极早期肝癌的“分子踪迹”,为肝癌高危人群提供更高灵敏度、更高特异性的精准早诊方案,为患者争取更早干预和更佳治疗时机。
● 敏感性93.08%——更精准识别风险人群中的肝癌患者
● 特异性93.70%——有效降低假阳性,减少不必要焦虑
■ AI赋能 | 试剂 + 软件 双三类医疗器械,检测稳定可靠
利为平®创新性地结合AI智能分析模型,实现检测全流程标准化、数智化。
● AI数据分析——基于大数据人工智能模型,优化阈值判定,提高检测准确性;
● 自动化解读——减少人为误差,提升结果一致性,避免主观判读偏差;
● 兼容性强——可适配主流PCR平台,医院、体检机构快速落地;
这一突破使得肝癌早筛早诊不再依赖单一试剂盒,而是通过智能化分析,让检测更高效、更精准,推动肝癌早筛早诊迈向“智能诊断”时代。

03
临床表现 | 六大医学中心、1600+样本实战答卷
由中国人民解放军空军军医大学第一附属医院牵头、中国人民解放军空军军医大学第二附属医院、广西医科大学附属肿瘤医院、首都医科大学附属北京佑安医院、郑州大学第一附属医院、赣州市第五人民医院等6家机构参与的多中心临床研究显示:
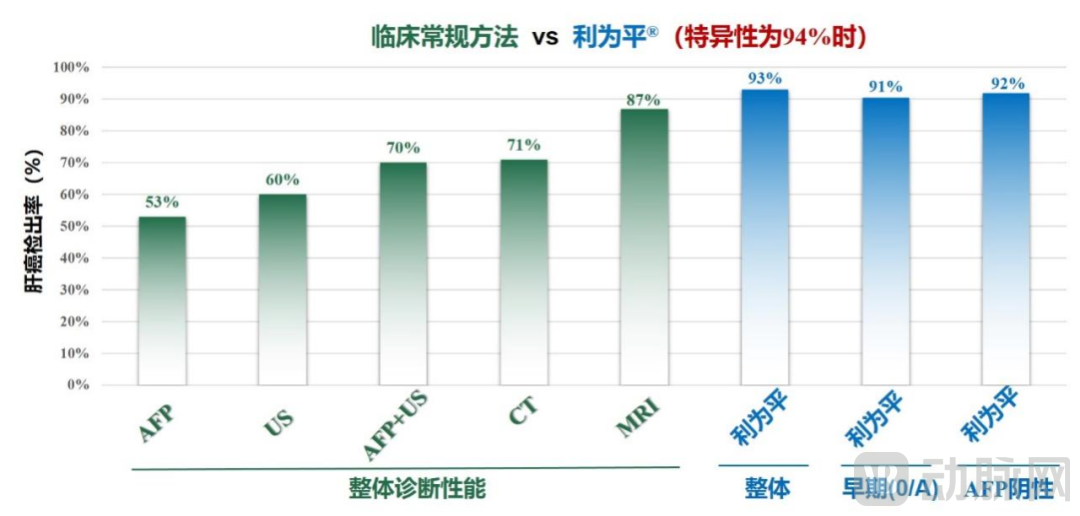
● 多中心临床研究表明,利为平®对肝癌尤其是早期肝癌的敏感性显著优于超声、AFP、CT或MRI等传统肝癌临床检测方法,能够更早期发现癌变,为高危人群提供更可靠的检测工具,其总体敏感性为93.08%,总体特异性为93.70%;
● 对于I期肝癌以及2cm以下的小肝癌,利为平®检测敏感性分别达到90.88%和91.07%;
● 对于AFP阴性肝癌,利为平®检测敏感性达到91.88%,对于超声及AFP漏检的2cm以下小肝癌,利为平®的检出率为89.47%;
● 检测特异性达到93.70%,对肝癌良性疾病具有良好的区分性能;
● 术后复发监测中,甲基化水平较CT/MRI提前3-6个月预警微转移灶,为患者争取二次手术机会。
■ 适用性广 | 无创便捷,覆盖全周期健康管理
利为平®适用于以下人群,助力肝癌早筛早诊:
● 40岁以上人群;
● 乙型肝炎病毒(HBV)和/或丙型肝炎病毒(HCV)感染的人群;• 各种原因引起的肝硬化患者;
● 长期酗酒或食用被黄曲霉素污染食物的人群;
● 有肝癌家族病史人群;
● AFP阴性影像诊断不明的患者。
同时,利为平®不仅可用于肝癌早诊,还在复发监测方面表现出优异的潜力。患者在治疗前采样建立基线,并在术后定期检测,利用甲基化标志物的动态变化预警复发风险,相较传统影像学检查提前捕捉复发趋势,为治疗决策提供关键依据。
■ 标准认可 | 甲基化技术获多部权威指南推荐
近年来,肝癌甲基化检测已获得国内外多项权威指南和共识的认可,并被逐步纳入临床筛查和诊断体系。
● 《原发性肝癌诊疗指南(2024年版)》指出:“利用特定基因表观遗传修饰特征,如甲基化,5-hmc等也可以用于肝癌早期诊断。”
● 《中国临床肿瘤学会(CSCO)原发性肝癌诊疗指南 2024》提出:“DNA甲基化在肝癌筛查和早诊中显示出较高的灵敏度和特异度,可以在影像学检查表现异常之前发现肝癌的存在,协助诊断早期肝癌,提升肝癌筛查效能。”
● 《原发性肝癌二级预防共识(2021年版)》强调:“ctDNA甲基化在诊断 HCC上有其特定的优势。”

《中国人群肝癌筛查指南(2022,北京)》
《中国肿瘤整合诊治指南(CACA)-肝癌部分》
《中国肝癌早筛策略专家共识(2021年)》
《血液标志物用于临床肝细胞癌早期筛查的专家共识(2021版)》
《原发性肝癌的分层筛查与监测指南(2020版)》
以上指南的推荐充分肯定了甲基化检测的临床价值,利为平®作为全球首款6基因甲基化+AI模型分析的肝癌早筛产品,将引领这一领域的技术创新和标准升级。
04
翱锐生物 | 让肝癌筛查更精准、更普及
翱锐生物始终致力于肿瘤早筛技术的研发与临床转化,作为全球肿瘤早筛技术创新者,翱锐生物已累计申请50余项发明专利和软件著作,服务网络覆盖全国数十家大型三甲医疗机构。2025年3月21日,美国食品药品监督管理局正式授予翱锐生物利为安®—肝癌多基因甲基化+蛋白多组学筛查试剂及配套分析软件 “突破性医疗器械”认定。该产品适用于多种高风险人群的肝癌监测,覆盖慢性肝炎、过度饮酒、非酒精性肝病、肝硬化以及有肝癌家族史等群体,显示出在复杂风险背景下的广泛适用潜力。利为平®的上市与利为安®的国际认可,均基于翱锐生物在液体活检、表观遗传及生物信息分析方面的核心技术积累;两者形成良好的协同效应:前者聚焦临床辅助诊断场景,后者拓展至更前端的大人群风险筛查。此次“试剂+AI软件”双认证产品利为平®的上市,标志着我国肝癌早筛正式迈入 “数智精准时代”!未来,翱锐生物将以甲基化诊疗为利刃,持续突破癌症早诊技术壁垒,赋能“早诊黄金窗口”前移。让潜伏的癌细胞无处遁形,让亿万国人享有与生命赛跑的主动权。
精准甲基化检测,早筛一步,健康一生!
关于杭州翱锐生物科技有限公司

杭州翱锐生物科技有限公司位于杭州市钱塘新区,是一家专注于肿瘤“精准医疗”与消化道健康整体解决方案的“国家级高新技术企业”。公司核心技术团队汇聚中美知名医学院及癌症中心的专家,拥有“肿瘤无创早筛早诊省级高新技术研究开发中心”。公司紧跟肿瘤精准治疗与全程管理的时代潮流,通过持续的技术创新与优化,不断拓展肿瘤诊断全流程产品的研发与应用,包括早期筛查,辅助诊断,用药指导,疗效评估,治疗监测,复发耐药检测和预后监测等。依托强大的生物技术和信息分析团队,公司采用无创液体活检技术,结合新一代测序技术及独创的基于大数据人工智能分析的双层机器学习分析核心算法,针对早期癌症病人的拷贝数变异及甲基化等肿瘤多组学特征在全基因组的水平上进行分析比对,构建了覆盖多癌种的早筛早诊技术体系。目前,公司产品已布局多种恶性肿瘤的早筛领域,包括肝癌、肠癌、胃癌、胰腺癌和食管癌等,为推动癌症的早诊早治提供全面解决方案。
使命:让每一个癌症患者发现于早期
愿景:做世界一流癌症诊断产品
* 参考文献
[1] Han B, Zheng R, Zeng H, et al. Cancer incidence and mortality in China, 2022[J]. Journal of the National Cancer Center, 2024, 4(1): 47-53.
[2] Park J W, Chen M, Colombo M, et al. Global patterns of hepatocellular carcinoma management from diagnosis to death: the BRIDGE Study[J]. Liver International, 2015, 35(9): 2155-2166.
[3] Marrero J A, Kulik L M, Sirlin C B, et al. Diagnosis, S taging, and M anagement of H epatocellular C arcinoma: 2018 P ractice G uidance by the A merican A ssociation for the S tudy of L iver D iseases[J]. Hepatology, 2018, 68(2): 723-750.
[4] Zeng H, Chen W, Zheng R, et al. Changing cancer survival in China during 2003–15: a pooled analysis of 17 population-based cancer registries[J]. The Lancet Global Health, 2018, 6(5): e555-e567.
[5] Kudo M. Management of hepatocellular carcinoma in Japan as a world-leading model[J]. Liver Cancer, 2018, 7(2): 134-147.
[6] Wang C, Li S. Clinical characteristics and prognosis of 2887 patients with hepatocellular carcinoma: A single center 14 years experience from China[J]. Medicine, 2019, 98(4): e14070.




























