今日,华芢生物科技(青岛)股份有限公司(以下简称“华芢生物”)成功登陆港交所,股票代码为2396.HK,联系保荐人为华泰国际、中信证券。
成立于2012年的华芢生物,是港股首家以血小板衍生生长因子(PDGF)药物为核心的创新生物制药上市公司。目前,全球PDGF药物市场仅有Regranex一款药物获得美国FDA批准上市,国内尚无PDGF药物商业化,该赛道尚属蓝海。华芢生物所在的蓝海赛道也获得了资本的支持,2021年至2023年,其累计完成了3轮融资,融资总额为4.05亿元,投资方包括青岛高科、鼎晖投资等。在2023年完成B轮融资后,华芢生物的投后估值达到33亿元。
本次IPO,华芢生物开盘价33.8港元,截至上午10点,其总市值约40.83亿港元。招股书显示,其所募资金的约61.8%,将用于其核心产品Pro-101-1(治疗烧烫伤)和PRO-101-2(治疗糖尿病足溃疡)的持续临床开发及商业化,这也是华芢生物上市募资的主要原因;其余资金将用于购置与研发及质量控制活动相关的专业设备、仪器,其他PDGF产品及非PDGF候选产品的临床前研发,以及日常运营。
企业主事人为母子俩
华芢生物的历史可追溯至2012年,其前身为北京中宏赛思生物技术有限公司,该公司由华芢生物创始人、董事会主席、执行董事及控股股东之一贾丽加与华芢生物另一位控股股东李葛卫以及当时的两位少数股东共同成立。2020年,中宏赛思更名为北京华芢生物技术有限公司。2023年,进一步更名为华芢生物科技(青岛)有限公司,并同步将注册办公地址从北京变更至青岛。
成立以来,华芢生物的主攻方向一直是发现、开发和商业化伤口愈合的疗法,尤其是PDGF药物。PDGF是血小板在损伤后分泌的生长因子之一,其能促进(其中包括)新血管的生成、调节炎症并刺激细胞增殖和迁移,最终加速伤口的愈合。根据弗若斯特沙利文报告,中国伤口愈合药物的市场规模从2018年的人民币828亿元增加至2024年的人民币957亿元,预计2033年将达到人民币1,180亿元。
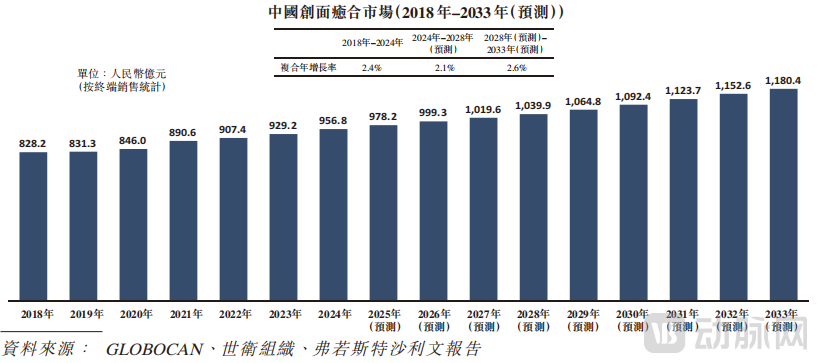
中国创面愈合市场,图源招股书
目前,PDGF是唯一获FDA批准用于外用的重组生长因子,用于糖足的临床已有20多年的历史,但该药物市场主要集中在美国,中国尚无商业化的PDGF药物用于该领域,未来市场潜力巨大。
除了华芢生物主攻的伤口愈合、压疮、放射性溃疡、干眼症、角膜损伤、日光性皮炎、脱发、痔疮及胃溃疡等适应症外。根据弗若斯特沙利文报告,PDGF药物还有望在多个医学专科的近20个其他适应症得到广泛应用,如普通外科(如静脉曲张溃疡、静脉炎和下肢静脉溃疡)、放疗(如放疗后的皮肤修复)、皮肤科、医学美容(如整形手术后的创面护理)、眼科(如角膜炎、屈光手术、屈光不正、白内障和青光眼)、骨科(如网球肘、筋膜炎、骨关节炎和骨质疏松症)、牙科(如牙龈萎缩、牙周病和牙槽骨缺损)以及妇产科(如剖腹产创面护理)等等。
华芢生物能够如此精准地聚焦市场蓝海,离不开企业背后的掌舵人。其创始人贾丽加自2012年4月华芢生物成立以来,一直担任董事兼董事会主席,并于2024年4月调任为执行董事。其主要负责领导和治理董事会,负责该集团的整体业务策略和管理。
贾丽加拥有超27年的医药行业经验。在成立华芢生物之前,贾女士于1997年1月至2004年9月担任牡丹江灵泰药业股份有限公司(北京办事处)的销售经理。随后,于2004年10月至2010年12月担任北京盛宏业医药科技发展有限公司(一家主要从事医药技术开发的公司)的副总经理,主要负责销售及运营管理。
与大多数科研出身的新药创始人不同,贾丽加擅长的领域是医药销售与运营。此外,华芢生物的另一位核心管理人员,也非医药科班出身,且是贾丽加的儿子——华芢生物董事会副主席及本公司总裁王轲珑,自2020年10月起担任董事,并于2024年4月调任为执行董事,主要负责监督执行华芢生物的整体策略、业务发展、管理和融资。
王轲珑拥有九年的企业运营和管理经验。加入本集团之前,他曾任职于Berkshire Hathaway Automotive(美国最大的汽车经销商集团之一)。随后,他成立北京绿汽科技有限公司,并于2017年4月至2020年9月担任该公司的首席执行官,负责该公司的整体运营。
虽然王轲珑非医药行业出身,前期在其他领域的成就也引起了颇多关注。曾入选2019福布斯中国30岁以下精英榜、2024财富中国40岁以下最具潜力的商界精英榜、2018胡润30×30创业领袖、2024胡润中国医疗青年企业家及2025财富中国40位40岁以下的商界精英。此外,他还是多篇网络智能及药物递送方面的论文的合著者。
医药行业内,母子组合的领导模式较为少见,可能吸引投资者关注,但也可能引发市场对公司治理结构和专业性的讨论。但贾丽加的医药行业经验和王轲珑的年轻精英形象,的确为华芢生物塑造了独特的市场形象。
建立蛋白质/多肽及核酸平台,核心人员曾主持SARS及H1N1项目
尽管有一部分核心成员非医药科班出身,但华芢生物的科研实力却不容小觑。目前,该公司已建有蛋白质╱多肽医药平台以及核酸医药平台。
· 蛋白质╱多肽医药平台:基于该平台,华芢生物具备了新药制剂开发及适应症扩展的能力。该平台在其管线发展过程中发挥着重要作用,尤其是在开发PDGF疗法方面。该平台拥有真核及原核表达技术。其一,基于毕赤酵母系统的真核表达技术对于确保PDGF产品的质量及产量至关重要;其二,原核表达技术则采用大肠杆菌系统,具有培养条件简单、生长及繁殖迅速、安全性高、成本效益高、效率高及可扩展性强等特性,这些特性使其成为生产重组蛋白质及肽的理想表达系统,预计将丰富企业基于该表达系统的蛋白质╱多肽治疗管线。
· 核酸医药平台:该平台以mRNA分子设计及LNP递送技术为基础,可开发针对实体瘤、脑胶质瘤及TNBC等适应症的mRNA及ASO候选产品。其中,mRNA分子设计技术有助于确保mRNA药物实现高水平表达,并减少潜在副作用。同时,LNP递送技术则可帮助华芢生物设计及筛选可电离脂质,以确定其专有候选分子。此外,华芢生物还打算进一步开发生物分子治疗药物开发平台,以支持其候选产品更多的应用场景。
核心团队背后,是一支具有丰富药物开发经验的专业研发团队。
例如,华芢生物总经理翟俊辉,在生物医学科学研究方面拥有约30年的经验,主要研究领域包括微生物学及病毒基因组学、新兴传染病中新病原体的发现以及新型病毒检测技术的开发。他获得军科院预防保健学博士学位,并于哥伦比亚大学公共卫生学院(感染与免疫中心实验室)担任微生物学博士后研究员,其博士后导师是有“病毒猎人”之称的生物医学专家Walter Ian Lipkin教授。
翟俊辉曾担任军科院一家研究所的研究员,主持并参与了多项国家级及其他重大医学项目,如基于核酸的SARS及H1N1疫苗体外诊断试剂的研发。他曾担任联合国伊拉克生物武器视察员及2008年中国奥运会生物安全小组副组长。其已发表100多篇关于微生物学、病毒基因组学及新型病毒检测技术的科学论文,拥有多项国家发明专利。此外,截至目前,翟俊辉是华芢生物27项专利申请(其中十项已获批准)的共同发明人。
华芢生物的首席研发官赵兴卉,则在生物医学科学研究方面拥有约20年的经验。她主要的研究领域为蛋白质工程药物、病原体感染机制、肿瘤分子标志物及表观遗传调控和造血干细胞衰老,并精通各种表达系统,包括基于大肠杆菌、毕赤酵母及CHO细胞的哺乳动物表达系统。截至目前,赵兴卉发表SCI论文37篇,被引用约1,000次,H指数为19。此外,截至目前,赵兴卉为华芢生物35项专利申请(其中七项已获批准)的共同发明人。
背靠研发团队及强劲的专利矩阵,华芢生物基于蛋白质╱多肽医药平台以及核酸医药平台,已建立了PDGF管线及mRNA及ASO管线等10款候选产品,涵盖14个适应症。其中,7款为PDGF药物,适用于广泛的创面愈合适应症,包括烧烫伤、糖足、新鲜创面、压疮、放射性溃疡、干眼症、角膜损伤、日光性皮炎、脱发、痔疮及胃溃疡,其剂型也丰富多样,包括外用凝胶、喷雾剂、滴眼液及口服,以及医疗器械支持的给药途径。
 华芢生物产品管线,图源招股书
华芢生物产品管线,图源招股书
仅两条管线获批临床,近三年亏损4.5亿
目前,华芢生物有两款核心产品,包括用于治疗深二度烧烫伤的Pro-101-1,已完成IIb期临床试验的统计数据分析,用于治疗浅二度烧烫伤的,已完成最后一例患者出组,但统计数据暂未得出;以及用于治疗糖尿病足溃疡(糖足)的Pro-101-2,现处于Ⅱ期临床试验阶段。
根据弗若斯特沙利文报告,Pro-101-1是中国治疗烧烫伤临床开发进度最快的PDGF候选药物。在治疗深二度烧伤方面,Pro-101-1已完成IIb期临床试验的统计数据分析,计划于2026年第一季度启动IIIa期临床试验,并于2026年第二季度完成。在治疗浅二度烧伤方面,Pro-101-1已完成最后一例患者出组,数据统计分析预计于2026年第一季度完成,后续是否进入Ⅲ期临床试验将取决于IIb期试验结果及与药审中心的沟通。
在商业化布局上,华芢生物已启动Pro-101-1的Ⅲ期临床试验筹备工作,计划2026年提交新药上市申请。市场拓展方面,华芢生物组建了覆盖伤口护理、医学美容等领域的复合型商业化团队,并与多家三甲医院建立临床研究合作网络。
华芢生物还计划在立足中国市场的同时,在美国推出Pro-101-1,开启国际化布局。该公司曾于2021年12月就Pro-101-1治疗烧烫伤向FDA提交了IND前沟通申请,FDA同意该公司开展临床试验的建议及通过创新生物制剂审批途径提交Pro-101-1治疗烧烫伤的BLA。
华芢生物另一款核心管线Pro-101-2,最初则是与军科院联合研发。2021年7月,Pro-101-2的IND批准,军科院仍为联合申办者。但自该管线获批之后,军科院就不再参与其临床研究及相关药物研发工作。因此,招股书显示,预计临床开发完成后,华芢生物将成为Pro-101-2 MAH许可的唯一持有人。此外,军科院已将与项目相关的技术资料转让予华芢生物,且后者享有两项PDGF相关专利的独家使用权及商业化权利,因此未经华芢生物同意,军科院无权将与项目相关的技术资料或PDGF相关专利授权第三方。
目前,PRO-101-2处于Ⅱ期临床试验阶段,预计于2027年第二季度完成Ⅱ期试验,并于2027年第三季度启动Ⅲ期临床试验。计划在美国、日本同步推进国际多中心临床试验,以加速全球商业化进程。
除了PRO-101-1与PRO-101-2之外,华芢生物其余八条管线均处于临床前阶段。因此,该公司目前仍处在临床推进与研发投入阶段,尚未形成稳定的产品商业化销售收入,预计未来较长一段时间也将持续进行研发投入。
招股书显示,华芢生物在2023年、2024年以及2025 年前 9 个月,净亏损分别为人民币1.05 亿元、2.12 亿元、 1.34 亿元(合计约4.5亿元)。其中,绝大部分亏损由研发费用及行政开支导致。截至 2025 年 9 月 30 日,华芢生物现金及现金等价物余额为 7379 万元。
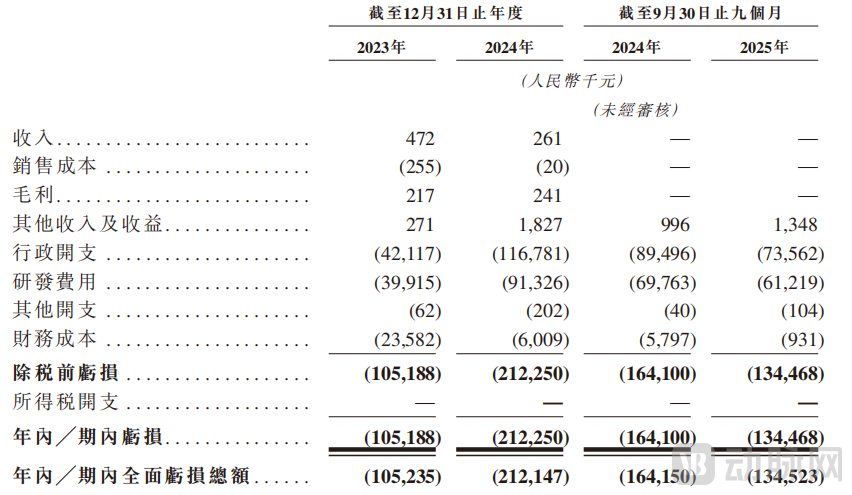
华芢生物财务数据,图源招股书
不难预见,随着管线的推进,华芢生物技术平台已验证、关键Ⅱ期数据已锁定,接下来这家企业更应该在真实世界与支付端证明自己。创面用药虽非肿瘤热点,却是慢病管理入口,谁能把愈合天数缩短一天,谁就把医疗成本降低一分。期待在钟声落定之后,华芢生物在国际资本平台的助力下,早日为国内创面修复赛道补上PDGF空白的一块拼图。





























