今日,香港上市公司德琪医药(Antengene,股票代码:6996.HK)宣布,与比利时生物制药公司优时比(UCB)达成全球独家授权协议,将针对B细胞介导自身免疫疾病的CD19×CD3双特异性T细胞衔接器(TCE)ATG-201的研发、生产和商业化权利授予优时比。
根据公告,德琪医药将获得8000万美元(包括6000万美元首付款及2000万美元近期里程碑付款),并有望在未来获得最高超过11亿美元的里程碑付款及基于未来净销售额的分级特许权使用费。此次合作不仅为ATG-201的全球开发打开了渠道,也进一步印证了TCE疗法正从肿瘤领域向自身免疫场景延展的行业趋势。

ATG-201:“2+1”结构结合遮蔽技术的CD19×CD3双抗
ATG-201是德琪医药自主研发的第二代T细胞衔接器候选药物,具有“2+1”二价结构:一端双价靶向B细胞表面的CD19抗原,另一端单价结合T细胞表面的CD3分子。这种设计结合了空间位阻遮蔽技术和快速结合/解离动力学的CD3序列,从而在有效清除B细胞的同时将细胞因子释放综合征(CRS)的风险降至最低。
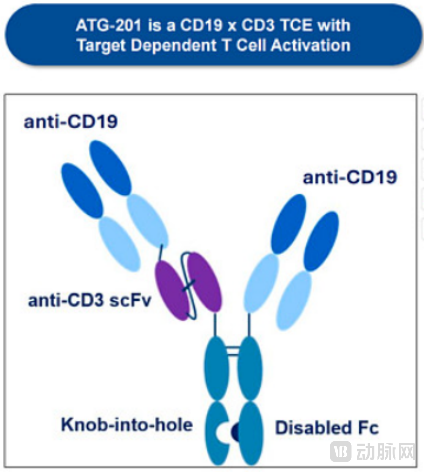
冷冻电镜结构分析显示,ATG-201未与CD19交联时,CD3结合位点被自身结构遮蔽,仅在遇到CD19阳性的B细胞时才将T细胞激活,有效避免了对健康细胞的非特异性攻击。
临床前研究结果印证了ATG-201的设计优势:在体外来源于系统性红斑狼疮(SLE)患者的外周血单核细胞(PBMC)中,ATG-201表现出显著优于对照TCE的B细胞清除能力,同时产生的细胞因子释放水平明显更低。在基于CD34+细胞的人源化小鼠模型中,单次给药即可在外周血、骨髓和脾脏中实现完全且持久的B细胞耗竭,并且细胞因子峰值远低于对照组。
值得注意的是,与第一代TCE相比,ATG-201在体外培养系统中引起的T细胞耗竭标志物(如PD-1、Tim-3)表达明显降低,这表明其对T细胞的长期过度激活问题有显著改进。此外,在自身免疫性小鼠模型(如MOG-EAE和MRL- lpr SLE模型)中,ATG-201的同源替代物显示出优异的治疗效果,显著延缓疾病进程。非人灵长类动物(NHP)实验进一步显示,ATG-201的猴子替代TCE可以实现深度、持久的初始B细胞清除,同时仅诱导低水平、短暂的细胞因子释放。
综上所述,ATG-201凭借其定点激活与低毒性的双重特征,在临床前研究中展现出“精准杀伤异常B细胞,安全留存正常细胞”的差异化优势,为进一步推进临床提供了有力依据。公司预计将在2026年第一季度启动ATG-201的临床试验。
.
从AnTenGager平台出发,适应症覆盖肿瘤和自免
本次授权背后,值得关注的还有交易双方在管线阶段、技术路径与全球化能力上的匹配关系。
德琪医药是一家研发驱动、已进入商业化阶段的生物科技公司,专注于重大未满足需求疾病的首创或优选疗法。公司拥有丰富的研发管线,涵盖临床前到商业化多个阶段。除ATG-201外,其自主发现的管线包括CLDN18.2抗体偶联药物ATG-022、口服CD73抑制剂ATG-037、PD-L1×4-1BB双抗ATG-101、针对CD24的巨噬细胞激活剂ATG-031,以及PRMT5-MTA小分子抑制剂ATG-042等。这些候选产品覆盖肿瘤和自身免疫等多种适应症。
德琪医药自主研发的第二代T细胞衔接器平台AnTenGager采用“2+1”二价结合结构和空间位阻遮蔽技术,能够靶向低表达抗原并降低CRS风险,在自身免疫性疾病、实体瘤和血液瘤领域具有广泛的应用前景。
德琪医药在推动创新药物商业化方面已有成熟经验。迄今为止,德琪医药已获得了32个美国及亚太市场的IND批件,并在亚太地区获得了10个NDA批准。其首款商业化产品希维奥®(XPOVIO®,通用名:塞利尼索)已在中国大陆、中国台湾、中国香港、中国澳门、韩国、新加坡、马来西亚、泰国、印度尼西亚和澳大利亚等9个市场获得上市批准,并在其中5个市场纳入医保目录。
作为全球合作方,优时比(UCB)成立于1928年,总部位于比利时布鲁塞尔,在全球约40个国家拥有超过9000名员工。公司长期专注于免疫系统和中枢神经系统疾病的创新疗法开发,2025年营收约为77亿欧元。
将ATG-201纳入其管线后,优时比获得了一款处于临床早期、但机制具有延展潜力的自免候选药物,用以补充其在B细胞相关疾病中的布局;而对德琪医药而言,此次合作不仅带来资金支持,更关键的是借助优时比的全球开发与商业化网络,加速项目在海外的临床推进与注册路径。
TCE进军自身免疫
近年来,自身免疫领域正从“长期慢病管理市场”逐步演变为高价值创新生物药的交易高地。根据公开交易数据,2020年以来,围绕关键靶点与差异化机制的重磅交易持续出现:2020年,强生以65亿美元收购Momenta,核心资产为FcRn(新生儿Fc受体)抗体;2022年,安进以278亿美元收购Horizon,押注IGF-IR(胰岛素样生长因子1受体)抗体管线。进入2024年之后,中国创新药企在该领域的参与度明显提升,诺诚健华、康诺亚、智翔金泰等公司相继通过自免双抗实现对外授权;2026年初,华深智药与赛诺菲达成合作,总金额达25.6亿美元。
在这一背景下,TCE开始进入自免视野。TCE本质上是一类通过双特异性或多特异性抗体,实现T细胞与靶细胞精准结合的免疫疗法,其核心机制在于绕过抗原呈递过程,直接激活T细胞对目标细胞进行杀伤。目前,全球已获批的约10款TCE产品仍主要集中在血液肿瘤与部分实体瘤领域,靶点包括CD19、CD20、BCMA及GPRC5D等。但从机制上看,TCE对B细胞的深度清除能力,为其在系统性红斑狼疮等B细胞驱动型疾病中的应用提供了现实基础。
近年来,全球多家大型药企和新锐公司纷纷押注自免TCE。2024年底,美国Candid Therapeutics一天内与多家中国企业达成三笔TCE研发合作,总潜在交易额超过13.2亿美元;和铂医药的BCMA/CD3双抗HBM7020(针对自身免疫适应症)已与大冢制药达成独家授权,总交易额约6.7亿美元。可以看到,自免TCE虽处于早期阶段,但已逐步进入产业化合作视野,而中国创新药企提供的相关分子与技术平台,也正在成为MNC外部引进的重要来源之一。
从更长周期来看,TCE在自身免疫中的应用仍处于早期探索阶段,其临床转化面临的核心问题并未完全解决。一方面,相较于肿瘤治疗,自免疾病对安全性的容忍度更低,如何通过结构设计与剂量策略降低细胞因子释放综合征(CRS)风险,仍是关键挑战;另一方面,TCE如何与现有成熟疗法(如抗CD20单抗等B细胞清除策略)形成差异化或协同关系,也将直接影响其临床定位与商业空间。
随着ATG-201等项目进入临床,行业将逐步获得关于“深度B细胞清除是否能够转化为长期疾病缓解”的关键证据。这一问题的答案,不仅决定单个产品的成败,更将界定TCE技术在自免领域的发展边界,相关进展值得行业持续关注。





























