近日,宁夏医科大学发布科技成果转化公示,拟将多项有关结核病诊断技术相关专利转让给紫耶生物科技(上海)有限公司,拟转化金额合计60万元。该专利技术包的发明人为马国荣及其团队。

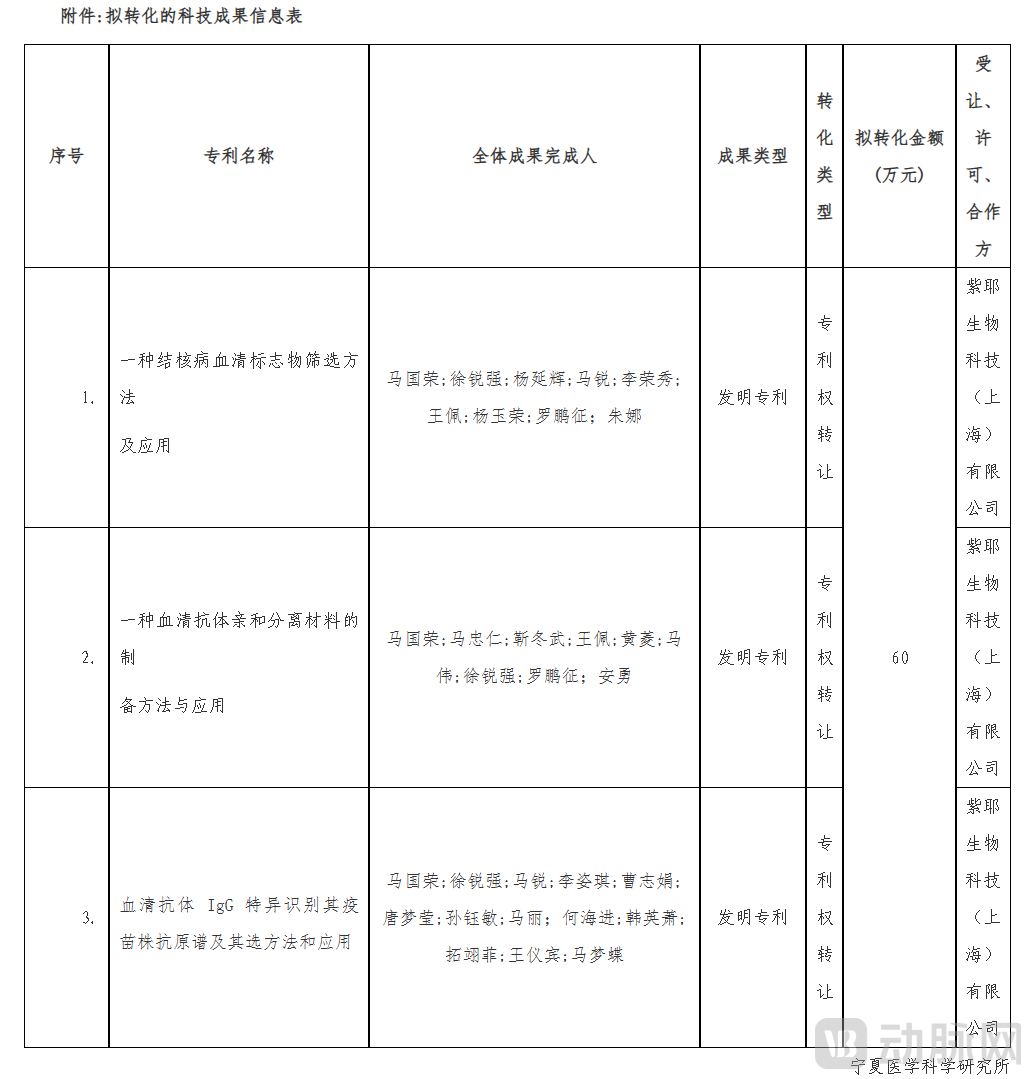
图片来自宁夏回族自治区医学科学研究所官网
专利一“一种结核病血清标志物筛选方法及应用”,针对传统方法易漏检、假阳性高等问题,采用仿生亲和色谱、抗原-抗体识别、质谱与生物信息学联用,构建高通量、高特异性筛选体系,筛选出237个初选标志物与111个高潜力蛋白,ELISA验证敏感性37.12%–56.96%,特异性最高96.67%,显著提升结核诊断准确性。
专利二“一种血清抗体亲和分离材料的制备方法与应用”,以琼脂糖为基质、环氧活化偶联重组链球菌G蛋白,摒弃剧毒溴化氰,生物安全性更高;对IgG吸附量最高15.47±1.63mg/mL,纯度与回收率均近90%,为前一专利提供高纯度抗体原料,实现抗体分离—标志物筛选全链条技术闭环。
结核病血清标志物筛选的技术瓶颈与临床需求
结核病(TB)是由结核分枝杆菌(MTB)感染引发的全球性传染病,也是单一致病死亡率最高的传染病之一,其中肺结核患者占总患者数的90%,严重威胁人类健康。在临床诊疗中,早期精准诊断是控制结核病传播、提高治愈率的关键,但现有诊断技术长期面临诸多瓶颈,难以满足临床需求。
目前临床中结核病血清标志物筛选多采用传统研究模式,核心依赖外源宿主细胞表达结核分枝杆菌蛋白,再通过血清学检测验证标志物潜力。然而这一方案存在显著缺陷:
一是外源表达系统局限性强,大部分的结核分枝杆菌蛋白无法在大肠杆菌等宿主细胞中有效表达,导致大量潜在有效标志物被遗漏;
二是重组蛋白制备效率低下,不仅表达与分离纯化过程耗时费力,且多数重组蛋白因活性受宿主性质影响,难以成为理想的血清标志物;
三是检测特异性差,传统方法直接使用患者总血清进行蛋白识别,而血清全蛋白成分复杂,非特异性结合现象普遍,极易造成假阳性结果,影响诊断准确性。
与此同时,作为血清学检测的前置关键环节,血清抗体分离技术同样存在明显短板。现有基于链球菌G蛋白(SPG)的亲和分离方法,需使用剧毒的溴化氰作为偶联试剂,对操作人员与环境均构成严重安全威胁;且配基脱落问题突出,脱落的SPG配基在临床应用中可能引发患者炎症或超敏免疫反应,限制了其在药用抗体纯化等场景的使用。
此外,部分仿生亲和或配位体-配基分离方法还存在特异性不足的问题,难以高效获取高纯度血清抗体,进一步制约了后续标志物筛选的精准度。
临床实践中,医生与患者对更安全、高效、精准的结核病诊断技术需求极为迫切:既需要解决传统标志物筛选中蛋白遗漏、假阳性率高的问题,实现早期精准识别;也需要突破血清抗体分离的安全与纯度瓶颈,为诊断提供高质量原料支撑。
因此,现在需要一套一体化结核病诊断关键技术,来解决传统诊断方法标志物遗漏、假阳性高、抗体分离不安全、原料纯度不足的临床痛点。
该专利组合的核心技术优势与创新价值,集中体现在对结核病诊断技术体系的全链条革新,其学术突破与技术创新可从以下维度深入解析:
在技术原理创新层面,两项专利构建了“高纯度抗体分离-高特异标志物筛选”的协同技术体系,突破了传统方法的底层局限。
对于结核病血清标志物筛选技术,其核心创新在于摒弃了依赖外源宿主细胞表达结核分枝杆菌蛋白的传统路径,创新性地将仿生亲和色谱、抗原-抗体特异识别、液相色谱-质谱联用(LC-MS/MS)及多维度生物信息学分析四大技术深度整合。该方法直接采用结核杆菌天然培养滤液蛋白或胞浆蛋白作为抗原来源,既规避了约50%结核分枝杆菌蛋白无法在大肠杆菌中有效表达的技术瓶颈,又最大程度保留了抗原蛋白的天然生物学活性与丰度分布,使其更贴近菌体在体内的自然生长状态。
在血清抗体预处理环节,通过19种小分子仿生亲和配基(如L-茶氨酸、氨基比林等)或特异性亲和配基(Protein A/G)构建层析柱,实现了血清抗体纯度超90%的高效纯化,显著降低了非特异性结合对后续检测的干扰,为标志物筛选的高特异性奠定了基础。
血清抗体亲和分离材料技术则针对传统链球菌G蛋白(SPG)亲和分离方法的核心缺陷,提出了双重技术革新:一是采用环氧活化技术替代剧毒的溴化氰作为偶联试剂,通过琼脂糖基质的环氧活化反应与重组SPG蛋白的氨基开环反应直接偶联,或经氨基化反应与三聚氯氰间接偶联,彻底解决了传统方法生物安全性差的痛点;
二是通过对重组SPG蛋白的密码子优化(消除大肠杆菌稀有密码子、调整GC含量等),使重组蛋白在大肠杆菌BL21(DE3)中的表达量提升约24.3%,纯度达91.2±1.72%,同时增强了配基与基质的结合稳定性,有效避免了配基脱落引发的临床免疫风险。该材料对免疫球蛋白G(IgG)的吸附量最高可达15.47±1.63mg/mL,纯度与蛋白回收率分别达88.92±2.17%和88.35±5.23%,为前序标志物筛选提供了高质量的原料支撑,形成了技术闭环。
在性能指标与学术价值层面,两项技术均通过严格的实验验证实现了关键指标的显著突破。标志物筛选技术经198人份结核患者血清和60人份健康人血清验证,筛选出237个初选标志物及111个高潜力候选蛋白(涵盖PstSI、FbpB、EsxA等已知候选蛋白),检测敏感性介于37.12±1.31%(Rv3763基因编码蛋白)至56.96±2.83%(Rv0577基因编码蛋白)之间,特异性最高达96.67%(Rv3248c基因编码蛋白),显著优于传统方法的诊断精度。
其创新采用的多维度筛选标准(包括蛋白丰度、亲疏水性、亚细胞定位、免疫原性等),为传染病血清标志物筛选建立了标准化研究范式,相关技术可拓展至其他感染性疾病的诊断研究。
血清抗体分离材料则通过正交实验优化环氧基活化条件,获得环氧基密度达111.42±7.72μmol/g的活化基质,其制备工艺无需特殊设备,操作条件温和(如pH 7.4的PBS缓冲体系),为临床实验室及生物制药领域的抗体纯化提供了低成本、高安全的技术方案,相关研究成果为亲和分离材料的绿色化、高效化发展提供了重要参考。
市场前景方面,该技术组合可直接用于结核病快速诊断试剂盒研发,满足基层医疗与高发地区防控需求,同时血清抗体分离材料可拓展至药用抗体制备、其他感染性疾病诊断等场景。
我国作为结核病高发国家,精准诊断技术需求迫切,该专利的产业化落地有望填补国内技术空白,兼具显著的临床价值、产业潜力与社会意义。
当前市场中与本专利组合形成竞争的产品及专利,主要集中在结核病诊断标志物相关技术与血清抗体分离材料两大领域,其市场布局与技术特征呈现差异化竞争格局:
北京万泰生物的结核分枝杆菌抗体检测试剂盒、上海邦奕生物科技有限公司的TB-Ab试剂盒是国内结核病血清学诊断的主流产品,已实现规模化临床应用,成为基层医疗机构、疾控中心的常用筛查工具。这类试剂盒采用ELISA原理,检测流程简便、成本较低,这类产品更多用于初步筛查,适配于基层大规模筛查与疑似病例初步分诊需求。
以Thermo Fisher(赛默飞)的蛋白质组学筛选解决方案、Orbitrap系列质谱联用系统为代表的通用型技术产品,是多传染病标志物发现领域的主流选择。这类产品依托标准化的样品处理流程、全面的蛋白质组学数据库及高灵敏度质谱检测技术,可适配结核病、肝炎等多种感染性疾病的标志物研究,通用性强,广泛应用于科研实验室与疾控中心的基础研究场景。
临床应用上,全球结核病防控需求迫切,我国作为高发国家,基层与高发地区对早期精准诊断技术需求突出。本专利组合的111个高特异性标志物,可支撑多标志物联合诊断试剂盒研发,解决传统产品检出率不足的问题,适配基层筛查与复杂病例诊断;其血清抗体分离材料无剧毒试剂、配基稳定,满足临床与试剂生产的安全合规要求。
产业价值方面,结核病诊断市场持续增长,血清学诊断领域需求稳健,生物诊断技术向“精准化、安全化、高效化”升级。本专利组合形成的技术闭环,可延伸出临床诊断试剂盒、生物制药用分离介质、科研定制化服务三类核心产品,且技术可拓展至其他感染性疾病及自身免疫性疾病、肿瘤等领域的抗体纯化,拓宽市场覆盖。




























