近日,Parabilis Medicines(原FogPharma,以下简称Parabilis)宣布完成新一轮3.05亿美元F轮融资。
本轮融资由RA Capital Management、Fidelity Management& Research Company和Janus Henderson Investors共同领投,其他参与者包括Frazier Life Sciences、Soleus Capital等明星机构。作为一家临床阶段的生物制药公司,自成立起,Parabilis便在肿瘤学领域深耕。截至目前,Parabilis已完成五轮融资,累计融资8.01亿美元。
Parabilis究竟有什么魅力,能持续吸引资本的目光?
1创立10余家Biotech的哈佛化学家,携手前强生全球研发负责人,破解“靶点可识、药物难研”困境
在癌症治疗领域,“靶点可识别,药物难开发”是一直以来困扰全球制药领域的难题。随着医学研究的不断深入,科学家们已发现大量与肿瘤发生、发展密切相关的疾病靶点,但其中超过80%的靶点被判定为“不可成药”,无法通过传统药物实现有效干预。而这些靶点之所以难以成药,核心技术瓶颈在于两方面:所在位置问题和自身结构问题。
多数关键肿瘤靶点存在于细胞内部,抗体因其分子量大无法穿透细胞膜,导致无法触及这些胞内靶点;同时,这些靶点多为蛋白-蛋白相互作用靶点,其表面平坦,缺乏小分子药物所需的“深结合口袋”,致使传统小分子药物难以实现精准、高效的结合:即便其能穿透细胞膜,也易被体内酶降解,无法发挥针对性治疗作用。
多年来,全球制药企业和科研机构都在寻找摆脱这一困境的方法,试图开发出能穿透细胞膜、精准结合胞内平坦靶点的新药。2015年,Parabilis应运而生——这家总部位于美国马萨诸塞州剑桥市的公司,拥有一支兼具顶尖科研能力与丰富产业经验的核心团队:
联合创始人Gregory Verdine博士,除了是科学家,也是企业家与投资人,35岁便成为哈佛大学化学系的终身教授。他深耕化学生物学与新药研发数十年,累计创立了10多家生物科技公司,其中5家成功上市、其中Gloucester Pharmaceuticals被生物制药巨头Celgene收购,主导开发三款药物罗米地辛(Romidepsin/Istodax®)、帕立瑞韦(Paritaprevir/ Viekira Pak®成分)和格卡瑞韦(Glecaprevir/Mavyret®成分)已获FDA批准上市。
董事长兼CEO Mathai Mammen博士,曾担任强生公司执行委员会成员兼全球研发负责人,他长期深耕生物医药领域,具备丰富的企业管理与新药研发统筹经验,主导公司融资、管线推进与全球战略布局。在其带领下,Parabilis成功完成多轮大额融资,核心管线稳步推进至临床阶段。
2由天然蛋白螺旋到可设计的“订书肽”
Parabilis的核心资产为其自主研发的Helicon™平台。其底层技术源自Verdine教授及其实验室团队的突破性研究。20世纪90年代末,该团队获得了一项长期研究的突破性进展:蛋白质α螺旋结构(the protein alpha-helix),既能嵌入细胞膜、实现高效穿膜,又能结合平坦的蛋白表面,恰好具备破解“不可成药”困境的核心特性。
α螺旋并非随意的蛋白结构,而是蛋白质的一种天然构象。它在具备一定刚性的同时,又有足够的灵活性和天然的稳定性。
2000年,Verdine团队基于这一洞见,发明了“订书肽”技术(stapled peptides),即Helicon技术雏形——通过化学交联技术,将短肽稳定为α螺旋构象,不让其结构松散,同时精准调控肽链的氨基酸序列,让它既能保持α螺旋的穿膜能力,又能精准匹配胞内靶点的结构。
具体来说,团队会选择特定的氨基酸(非天然氨基酸),通过专属连接子将其连接,形成稳定的α螺旋结构,使其在轻松穿透细胞膜的同时,还能通过表面的氨基酸侧链与胞内靶点形成紧密结合;并且,“订书”设计还能避免肽链被体内蛋白酶降解,让药物在体内持续发挥作用。
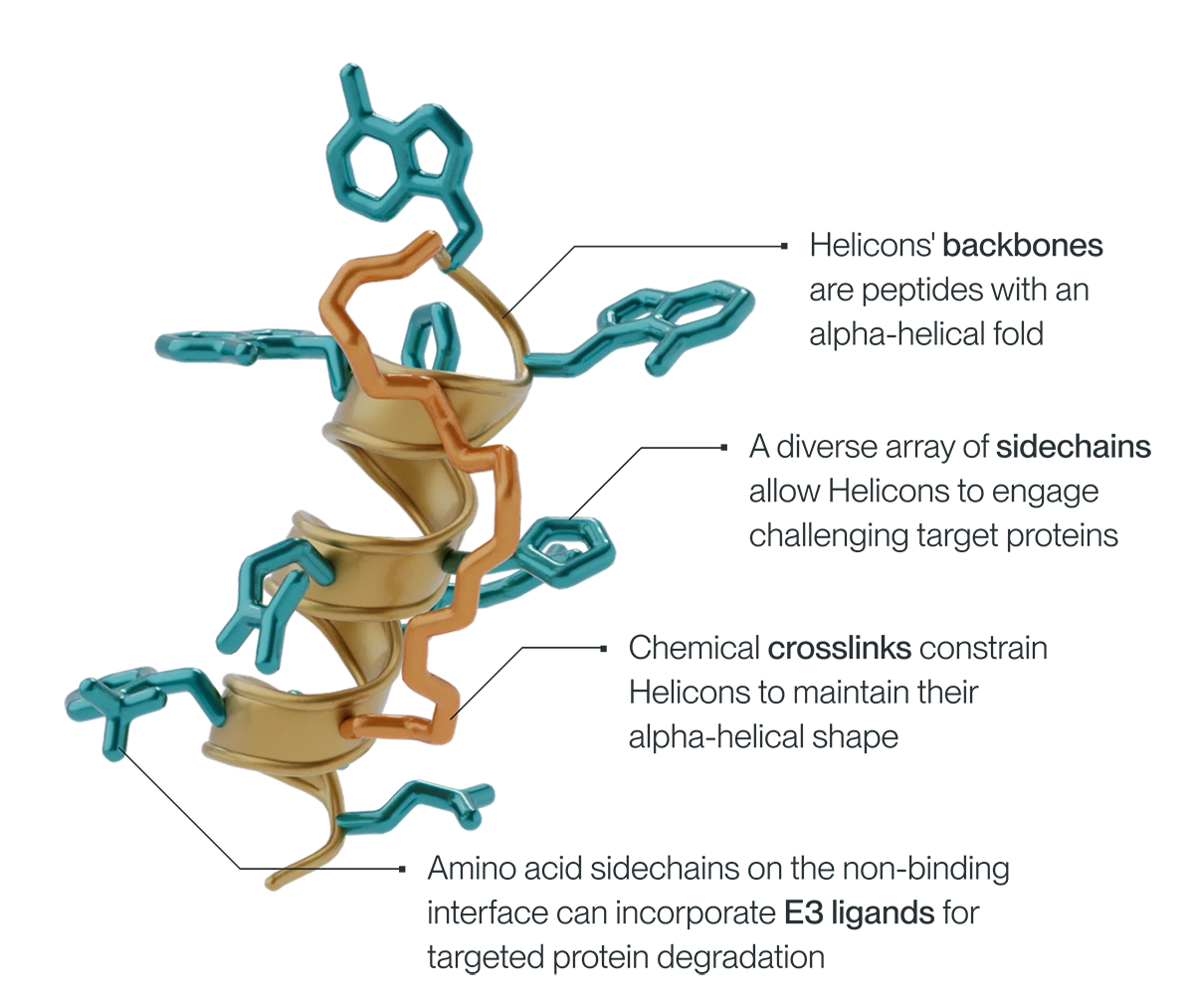
Helicon™技术原理(图源Parabilis官网)
3融合模块化学+高通量验证,打造AI+闭环平台
随着生物化学技术与计算科学的持续迭代,Parabilis在订书肽等前沿多肽技术的基础上持续深耕,最终搭建起独具壁垒的Helicon™平台。Parabilis将其定义为一套AI与实验技术融合的全新药物创造体系,以AI与物理计算、模块化学、多重实验平台三大支柱为核心,大幅提升了新药研发的效率,也让“不可成药”的靶点真正实现可干预、可治疗。
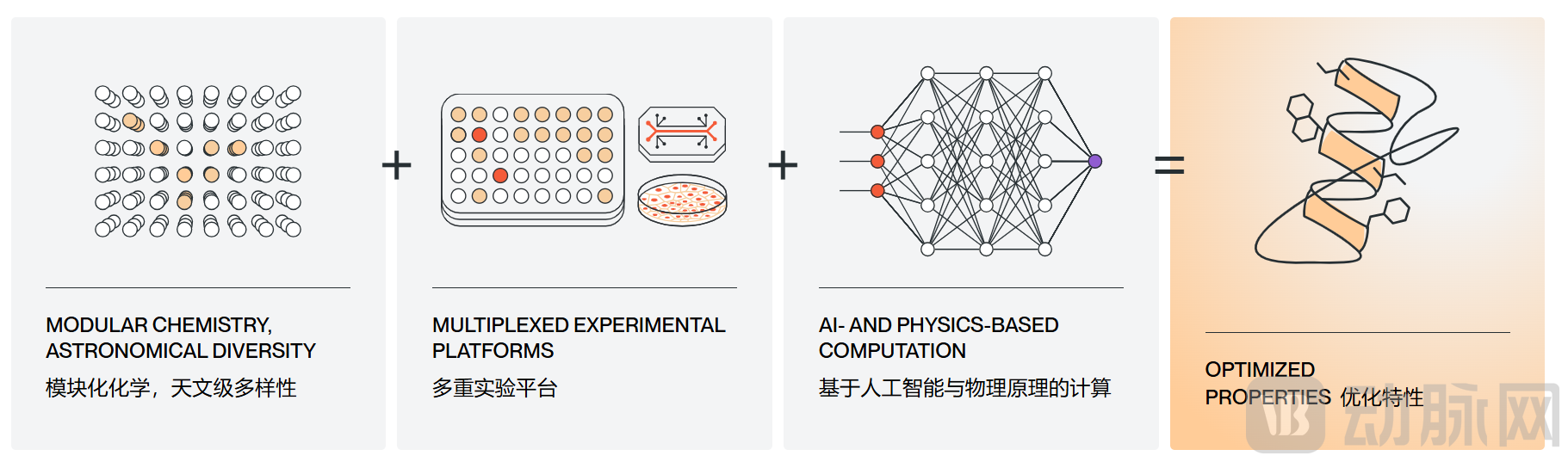 Helicon™平台三大核心(图源Parabilis官网)
Helicon™平台三大核心(图源Parabilis官网)
化学修饰模块化:以蛋白质天然α螺旋结构+独创“订书”化学交联技术为基础,Parabilis自建超过1000种定制非天然氨基酸库,搭配数百种专有连接子。平台使用模块化化学组装的方法,拥有比天然肽高出20个数量级的多样性,在保留α螺旋的穿膜能力的基础上,让肽链表面氨基酸侧链精准暴露,与胞内平坦靶点形成特异性结合,解决了传统肽链“结构不稳定、穿膜效率低、结合力弱”三大痛点。
AI物理计算模型:Helicon™平台整合了先进的AI算法与物理计算模型,构建了专属的肽设计与筛选系统。与传统药物研发的逐一筛选、穷举尝试的模式不同,Helicon™平台的AI模型以Parabilis独有的非天然氨基酸数据集为基础,结合前沿物理建模,可以实现快速预测不同氨基酸组合、不同“订书”方式所形成的α螺旋肽的关键属性,包括穿膜效率、靶点结合亲和力、体内稳定性、代谢半衰期、免疫原性、ADME性质等。
高通量验证闭环:为确保筛选出的候选药物具备临床应用价值,Parabilis搭建了完善的多重高通量实验验证体系,使用高度自动化的实验设备,可同时并行评估数千个α螺旋肽分子。AI模型还能通过自学习机制,结合高通量实验数据,持续优化预测精度,形成“实验产生数据→训练AI→AI指导设计→实验验证”的闭环。此外,AI模型结合公开的生物和患者数据集,进一步优化临床设计,缩短候选药物筛选周期,大幅降低研发成本。
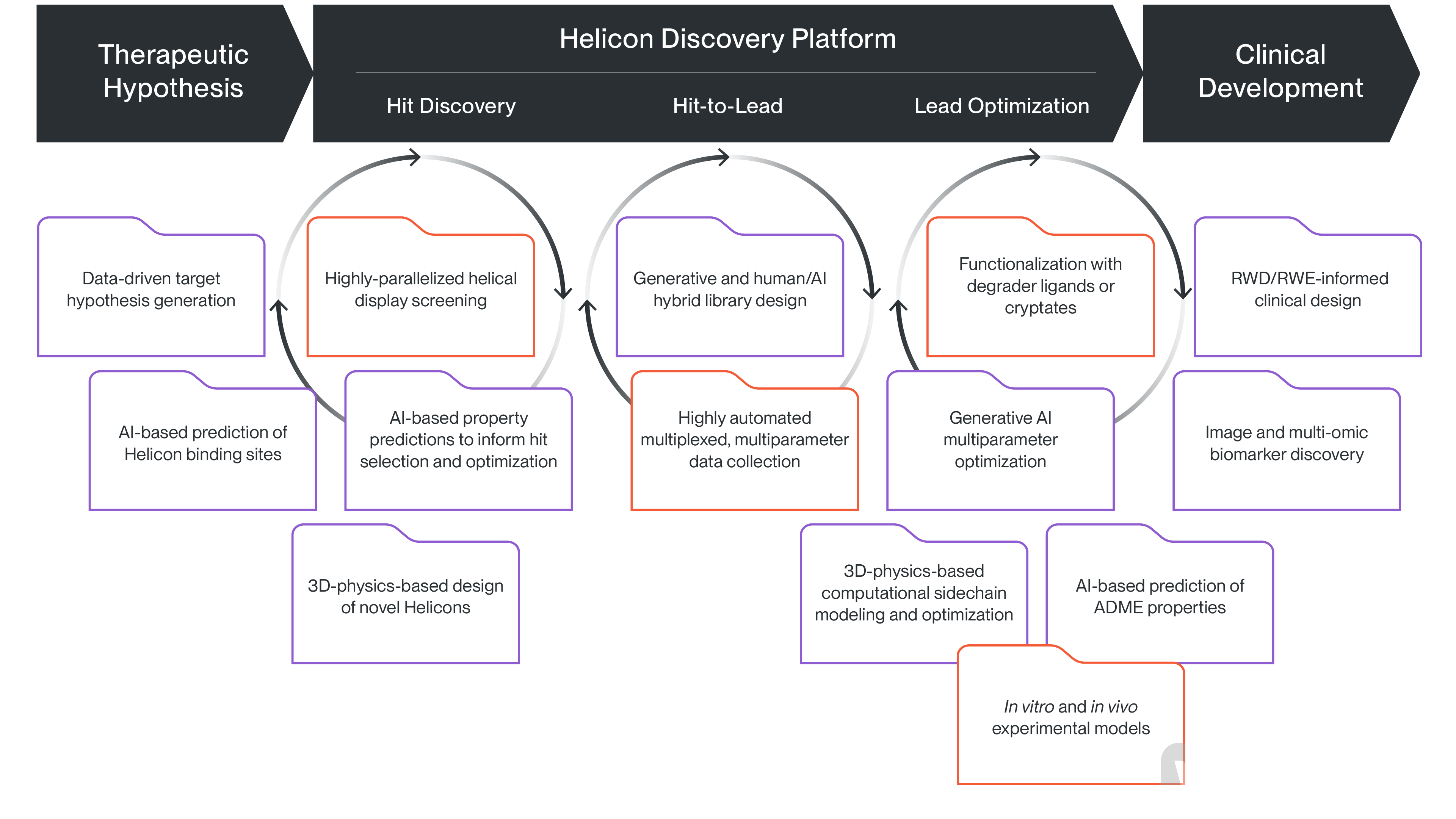 Helicon™平台运行流程(图源Parabilis官网)
Helicon™平台运行流程(图源Parabilis官网)
4自研小分子进入临床,合作研发放射性配体疗法
依托Helicon™平台的技术优势,Parabilis目前已构建了多元化的研发管线,涵盖临床阶段、临床前阶段,聚焦“不可成药”胞内靶点,覆盖了多种恶性肿瘤。
全球首个且唯一直接抑制β-catenin:TCF相互作用的在研药物zolucatetide(FOG-001)
Wnt/β-catenin(Wnt/β-连环蛋白信号通路,经典肿瘤相关信号通路)通路异常是结直肠癌、肝细胞癌、胃癌、硬纤维瘤、造釉细胞瘤等多种实体瘤的关键驱动因素,但β-catenin与转录因子T细胞因子(TCF,经典Wnt信号通路的核心转录激活复合体)家族的相互作用长期被视为不可成药靶点。
zolucatetide作为β-catenin:TCF相互作用的竞争性抑制剂,通过直接靶向该核心,阻断其相互作用,不依赖具体突变类型,即可关闭下游致癌信号,从根本上阻断了肿瘤进展。
目前zolucatetide处于1/2期临床阶段,于2025年11月和2026年3月获得FDA授予的硬纤维瘤适应症快速通道资格和孤儿药资格:
硬纤维瘤:在12名接受了zolucatetide治疗的硬纤维瘤患者中,根据RECIST 1.1标准,所有可评估疗效的患者(n=10)均出现肿瘤缩小;同时,在完成超过一次基线后扫描的患者(n=5)中,观察到80%的客观缓解率(ORR),且安全性良好,无4/5级治疗相关不良事件。
造釉细胞瘤型颅咽管瘤(ACP):三名ACP患者在接受了144 mg/m²(n=1)和360 mg/m²(n=2)剂量水平的zolucatetide治疗后,所有患者(n=3)均出现肿瘤缩小,其中两名患者达到部分缓解,肿瘤体积分别缩小56.0%和48.0%;一名患者疾病稳定,肿瘤体积缩小19.2%。
家族性腺瘤性息肉病(FAP):一名患FAP并伴有韧带样瘤的患者,在接受zolucatetide治疗60周后,获得了显著改善;与近两年前治疗前的评估相比,观察到息肉数量和大小均大幅减少,分期下调,韧带样瘤直径也减小了52.2%。
其他:在肝细胞癌(HCC)、成釉细胞瘤、涎腺癌、实性假乳头状肿瘤(SPN)均观察到单药活性。
目前,Parabilis储备多个“不可成药”靶点管线,围绕“订书肽”搭建小分子+核药产品矩阵。
多条小分子管线储备
β-catenin degrader(β-连环蛋白降解剂):采用Helicon™技术,通过双功能降解剂方法结合可溶性β-catenin,并将其靶向蛋白酶体进行降解。可与zolucatetide形成机制互补,聚焦于关闭Wnt通路,覆盖80%–90%的结直肠癌病例。
ERG degrader(ERG降解剂):靶向ERG融合蛋白(前列腺癌常见融合蛋白),精准结合ERG独特区域,并搭载E3配体,通过泛素-蛋白酶体系统特异性降解ERG,而不影响结构相似的ETS家族蛋白;可针对约40%前列腺癌存在的TMPRSS2-ERG融合,为去势抵抗性前列腺癌提供新的治疗选择。
Androgen receptor degrader(雄激素受体降解剂,非配体结合位点):靶向雄激素受体AR(结合在非配体结合区),绕过AR配体结合域高频耐药突变,直接降解活化态AR;解决转移性去势抵抗性前列腺癌(mCRPC)现有药物耐药问题。
携手ARTBIO,共创核素+靶向治疗新赛道
HEARTs(Helicon-enabled alpha radioligand therapies):与放射性制药公司ARTBIO合作,共同开发针对多个靶点的Helicon赋能α-放射性配体疗法(HEARTs)。双方充分发挥各自核心技术壁垒:Parabilis提供Helicon™平台,解决靶点结合难题;ARTBIO依托AlphaDirect™平台,提供潜在同类最优同位素铅-212(212Pb)的放射性配体开发能力。
铅- 212凭借半衰期短、精准释放大能量至肿瘤、高稳定性、可SPECT/CT成像的理想临床特征,可与Helicon™肽的靶向性结合,实现对肿瘤的精准递送与可视化治疗。
5AI+蛋白质设计重构新药研发范式,中外企业加速抢占先机
随着现代科技尤其是人工智能的发展,AI与蛋白质设计的深度融合正掀起一场产业革命。全球范围内已有多家企业聚焦与此进行研究,行业正从技术验证阶段加速迈向价值兑现阶段。
英矽智能(03696.HK)凭借Pharma.AI平台,实现了“AI发现新靶点+AI设计药物分子”的全流程闭环。其核心管线TNIK(Pharma.AI发现的肺纤维化新靶点)抑制剂Rentosertib(伦托司替)在大大降低研发成本的同时提升了研发速度,并已于2025年在《Nature Medicine》发表IIa期临床试验数据,结果显示其具有潜在的抗纤维化及抗炎作用。
晶泰科技(02359.HK)基于垂类数据应用人工智能+机器人技术打造技术平台,据晶泰科技官网披露,其PepiX™ AI多肽药物一体化平台可实现多肽从头设计,无需考虑靶点是否具有已知蛋白质-蛋白质相互作用,数月内即可产出低纳摩尔级高亲和力肽段,研发效率较传统模式大幅提升。2026年2月,晶肽科技与尧唐生物共建mRNA/CAR-T AI筛选平台,期望在降低治疗成本的同时提高药物研发的效率和成功率。
由在AI蛋白质领域由相关研究的计算生物学家许锦波教授创立的分子之心(MoleculeMind),近期携手天津大学、海南大学、南方科技大学、杜克大学等科研结构,通过自研ComplexDDG等AI蛋白质算法,实现蝎毒素LqhαIT的杀虫效力翻倍。同时,其自研的MoleculeOS大模型已完成代际升级,集成NewOrigin达尔文大模型,成功解决AlphaFold 3未覆盖的产业难题,可广泛应用于抗体设计、酶改造、多肽优化等场景。
在跨国药企阵营,礼来、赛诺菲、施维雅等龙头企业也纷纷抛出橄榄枝,通过大额战略合作,快速抢占AI+蛋白质设计赛道高地。
礼来除与英矽智能达成27.5亿美元战略合作外,还与英伟达宣布联合投入10亿美元成立AI药物研发实验室,旨在缩短新药研发周期。同时,礼来自研的AI平台覆盖抗体、小分子药物设计,重点布局肿瘤、神经退行性疾病领域,据礼来官网披露,其推出的AI药物发现模型拥有超过价值10亿美元的专有数据。
赛诺菲则聚焦自身免疫/炎症疾病领域,2026年1月与华深智药子公司Earendil Labs达成最高25.6亿美元合作,应用AI平台发现新型双特异性抗体,借助AI技术优化抗体设计、推进多肽药物研发,突破传统研发瓶颈。施维雅则深耕肿瘤领域,2026年1月与英矽智能签署多年期合作,金额最高8.88亿美元,联合开发肿瘤领域挑战性靶点药物,由英矽智能负责靶点与分子设计,施维雅主导临床与商业化推进。
从难点到蓝海,从布局到破局,全球生物医药行业正以技术创新重新定义治疗的边界。未来,随着AI制药、蛋白降解、稳定肽等技术持续突破,或将有更多靶点被逐一攻克。





























