
2019.7.22-2019.7.28,本周新药数据共9个,其中肿瘤3个,抗病毒2个,代谢2个,神经系统2个。
❖BMS 公布checkmate 227的简要结果,好消息是O与Y联用对比化疗在PDL1阳性患者NSCLC有明显获益,坏消息是O和chemo联用相比chemo,在一线治疗NSCLC中,若不考虑PDL1和TMB表达,OS没有明显获益。考虑到K 药(单药/联合化疗)在2018年便覆盖核心NSCLC患者的一线疗法,且不考虑PD-L1表达水平,O药在NSCLC领域已经面临被K药全方位胖揍的局面。国内PD1三朵金花,恒瑞、信达和君实,谁更像O,谁更像K,或者谁更能青出于蓝,让我们拭目以待。
❖安进和艾尔建宣布在美国市场推出Mvasi和Kanjinti,这两款药物分别是安维汀和赫赛汀的生物仿制药,同时梯瓦和Celltrion有望在今年晚些时候推出美罗华生物仿制药Truxima。过去20年,安维汀、赫赛汀、美罗华这三剑客开启了波澜壮阔的抗体大时代,在整个肿瘤战争史上刻下了自己的名字,现在可能终于要到谢幕的时候了。不过罗氏也不断推陈出新,Ocrevus(多发性硬化症)、Perjeta(乳腺癌)、Tecentriq(PDL1)、Hemlibra(血友病)若开发得当,应可成为下一个十年的四小龙。
BMS宣布Opdivo与CTLA-4抑制剂Yervoy
联用在PD-L1阳性的NSCLC中达到部分共同主要终点
BMS宣布剂Opdivo与CTLA-4抑制剂Yervoy联用,在治疗肿瘤PD-L1表达≥1%的非小细胞肺癌患者(NSCLC)的3期临床试验中,达到了试验1a部分共同主要终点
Opdivo和Yervoy是BMS开发的免疫检查点抑制剂
Checkmate 227分为3组。1a组评估nivo联合ipi或nivo单独用药对比化疗治疗PD-L1阳性的NSCLC;1b评估nivo联合ipi对比化疗和nivo联合化疗对比化疗一线治疗PD-L1阴性的NSCLC。2组是nivolumab联合化疗对比化疗,不考虑PD-L1和TMB,主要研究终点为OS
1a,和1b的探索性分析发现opdivo达到了共同终点,延长了OS。但是2组没有显著获益
Checkmate 227的实验设计
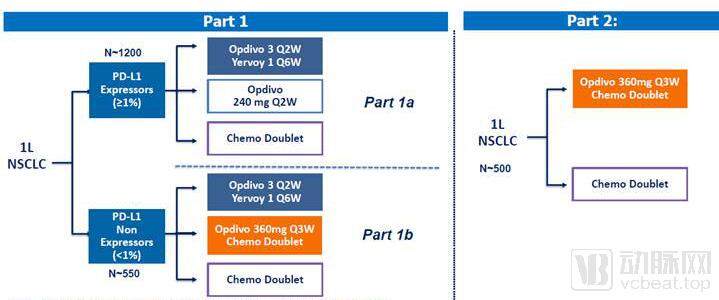
数据来源:BMS
杨森公司宣布,治疗多发性硬化的在研疗法ponesimod,
在3期临床试验中达到主要终点和多数次要终点
杨森公司(Janssen)宣布,治疗复发型多发性硬化症(MS)的在研疗法ponesimod,在3期临床试验中达到主要终点和多数次要终点
Ponesimod是一款特异性鞘氨醇-1-磷酸受体1(S1P1)调节剂
在随机双盲,含活性对照的3期优越性临床试验,包含1133名患者,疗程长达108周,主要是比较ponesimod与获批疗法teriflunomide在治疗复发型MS患者时的疗效、安全性和耐受性
ponesimod与teriflunomide相比,达到了试验的主要终点,疗效至少相当
FDA接受Epizyme在研药物tazemetostat递交的新药申请(NDA),
同时授予其优先审评资格
Epizyme宣布,FDA接受其为在研药物tazemetostat递交的新药申请(针对上皮样肉瘤),同时授予其优先审评资格
Tazemetostat是一款“first-in-class”组蛋白赖氨酸甲基转移酶(Histone-Lysine N-methyltransferase)EZH2的抑制剂
2期临床试验,治疗上皮样肉瘤患者
tazemetostat的ORR为15%,DCR达到了26%。中位OS尚未抵达。此外,tazemetostat也展示了良好的安全性和耐受性
罗沙司他在长期接受透析和未经透析的
肾脏病患者的2项3期实验达到临床终点
NEJM在线发表了两篇论著,公布了罗沙司他(roxadustat)在中国的两项3期临床试验结果
罗沙司他是一种“first-in-class”低氧诱导因子脯氨酰羟化酶抑制剂(HIF-PHI)
在透析导致贫血的实验中,实验者招募了305名终末期肾脏病患者,以2:1的比例随机分配至试验组和对照组;在肾性贫血实验中,研究者以2:1的比例随机分配了154名慢性肾病患者
在透析贫血组中,受试者在23周至27周时血红蛋白中位水平为10.4 g/dL,达到了预设的非劣效性;在肾性贫血组中,服药8周后试验组患者的血红蛋白水平有显著提升,达到了主要临床终点
Myovant Sciences宣布其在研relugolix组合疗法,
在治疗子宫肌瘤的3期临床试验达到了主要疗效终点
Myovant Sciences公司宣布,其在研relugolix组合疗法,在治疗子宫肌瘤的3期临床试验LIBERTY2中,达到了主要疗效终点和6项关键性次要终点
Relugolix组合疗法每片包含relugolix (40 mg),雌二醇(1.0 mg),以及醋酸炔诺酮(0.5 mg)
3期临床实验,主要观察患者的月经出血量
接受relugolix组合疗法治疗的患者中71.2%达到预设的缓解标准这一主要临床终点,安慰剂组的数值为14.7%(p<0.0001)
默沙东公司宣布治疗HIV感染的创新药物islatravir,
在1期临床试验中获得积极结果
默沙东(MSD)公司宣布,治疗HIV感染的创新核苷类逆转录酶易位抑制剂(NRTTI)islatravir(曾用名MK-8591),在1期临床试验中获得积极结果
Islatravir是默沙东开发的创新NRTTI,通过多种机制抑制HIV逆转录酶的功能,作用机制有别于目前获批的抗HIV疗法和传统的核苷类逆转录酶抑制剂(NRTIs)
在1期临床试验中,islatravir被装进一个火柴大小的聚合物药物洗脱植入体。它被皮下植入到健康志愿者的上臂中,在12周之后植入体被摘除
植入体能够持续12周将细胞内islatravir的浓度保持在药代动力学阈值以上
ViiV Healthcare公司宣布fostemsavir在
HIV-1 成人患者的3期临床试验中取得积极结果
ViiV Healthcare公司宣布,其“first-in-class”抗病毒疗法fostemsavir,在治疗接受过多次前期治疗的HIV-1 成人患者的3期临床试验中取得积极结果
Fostemsavir是temsavir的前体药物(pro-drug)。Temsavir能够与HIV-1包膜糖蛋白gp160复合体的gp120亚基相结合,阻断病毒与细胞CD4受体的相互作用
3期临床试验,fostemsavir与优化背景治疗(OBT)联用,治疗携带对多种药物产生耐药性HIV-1病毒的难治患者群
在接受fostemsavir与OBT联合治疗第96周,60%随机队列中的患者(n=163/272)实现病毒学抑制(HIV-1 RNA<40拷贝/毫升),与第48周的结果相比增加了6%
Vertex Pharmaceuticals公司向美国FDA提交了NDA,
申请治疗囊性纤维化(CF)的药物上市
Vertex Pharmaceuticals公司宣布,它向美国FDA提交了由VX-445(elexacaftor),tezacaftor和ivacaftor三种药物构成的组合疗法的新药申请(NDA),用于治疗囊性纤维化(CF)
VX-445是新一代CFTR蛋白矫正剂,它用于恢复携带F508del突变的CFTR蛋白的功能,从而改善CF患者的呼吸功能
在随机双盲,含安慰剂对照的3期临床试验中,VX-445与tezacaftor和ivacaftor构成的三联疗法用于治疗携带一个F508del基因突变和一个功能最小化基因突变的患者
治疗组患者与接受安慰剂治疗的对照组相比,肺功能显著提高
囊性纤维化的表现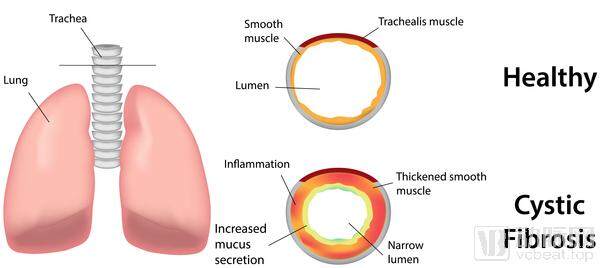
数据来源:NIH
Acadia宣布其5HT2A反向激动剂Nuplazid在
一个叫做ENHANCE的三期临床失败
Acadia宣布其5HT2A反向激动剂Nuplazid在一个叫做ENHANCE的三期临床失败
Nuplazid是高选择性5羟色胺受体2A亚型反向激动剂,但没有多巴胺受体活性、因此没有其它精神分裂药物的不自主运动副作用
这个试验招募396位中重度精神分裂患者,分别在标准疗法背景上使用6周Nuplazid和安慰剂
两组患者在阳性、阴性总评分(PANSS)无差异,错过一级终点。Nuplazid在事先设定的阴性症状分值这个二级终点显著优于安慰剂组,但因一级终点错过这个终点只能作为探索性疗效
❖美国FDA批准礼来公司开发的Baqsimi粉剂上市,作为治疗严重低血糖的紧急疗法。Baqsimi是一种胰高血糖素从鼻腔喷入的粉剂疗法,它是第一款获得FDA批准的严重低血糖非注射型紧急疗法
❖默沙东(MSD)和卫材(Eisai)联合宣布,美国FDA已经授予Keytruda(pembrolizumab)与Lenvima(lenvatinib)组合疗法突破性疗法认定,用于一线治疗不能局部治疗的晚期不可切除的肝细胞癌(HCC)患者
❖Freenome宣布完成1.6亿美元的B轮融资,至此Freenome已累计完成2.38亿美元的融资。Freenome旨在开发简单而准确的多组学血液检测方法,对早期癌症进行检测和筛查
❖德克萨斯大学西南医学中心的研究人员发现,目前一些用于治疗不到10%的乳腺癌患者的PARP抑制剂可以用于治疗更广泛的癌症类型,包括卵巢癌和前列腺癌。这项新研究还发现了一种潜在的生物标志物,可以指导在那些患者中可以使用PARP抑制剂抗击癌症
❖GSK宣布任命前诺华和阿斯利康首席财务官Jonathan Symonds为下一任董事长。GSK正面临业务上的巨大转变,目前正在寻求“通过创新的研发方法创造价值”,并计划“创建和拆分两家新的世界领先公司”,一家专注于制药和疫苗,另一家专注于消费者健康业务
❖安进和艾尔建宣布在美国市场推出Mvasi和Kanjinti,这两款药物分别是安维汀和赫赛汀的生物仿制药。安维汀和赫赛汀是全球最畅销的两款肿瘤学药物,2018年全球销售额分别为68.49亿瑞士法郎和69.82亿瑞士法郎。在美国,两款药物2018年销售额合计为59亿美元































